Malaria
Malaria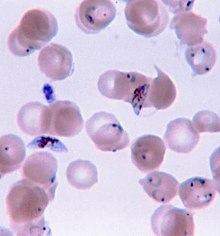 Blutausstrich, der das Vorhandensein des Parasiten Plasmodium falciparum mit der Form eines "C" oder einer Sichel in menschlichen roten Blutkörperchen zeigt .
Blutausstrich, der das Vorhandensein des Parasiten Plasmodium falciparum mit der Form eines "C" oder einer Sichel in menschlichen roten Blutkörperchen zeigt .
| Spezialität | Ansteckende Krankheit |
|---|
Die Malaria oder Malaria , auch „Sumpffieber“ genannt, ist eine durch einen Parasiten der Gattung Plasmodium verursachte Infektionskrankheit , die durch den Stich bestimmter Stechmückenarten Anopheles verbreitet wird .
Mit 229 Millionen Erkrankten und 409.000 Toten im Jahr 2019 bleibt Malaria die wichtigste Parasitose und betrifft vor allem Kinder unter fünf Jahren und Schwangere. 95 % der Fälle wurden in 29 Ländern registriert, insbesondere in Subsahara-Afrika (27 % in Nigeria, 12 % in der DR Kongo, 5 % in Uganda, 4 % in Mosambik) ( vgl. ausführlichen Abschnitt: „ Epidemiologie “) .
Der Malariaerreger wird hauptsächlich nachts übertragen, wenn er von einer weiblichen Mücke der Gattung Anopheles gebissen wird , die sich nach dem Stich eines an Malaria erkrankten Individuums selbst infiziert hat. Der Parasit infiziert die Leberzellen des Opfers und zirkuliert dann im Blut , besiedelt die Erythrozyten (rote Blutkörperchen oder rote Blutkörperchen) und zerstört sie. Viele homöothermische Tierarten werden von Plasmodiidae parasitiert , die ihnen untergeordnet sind ; Menschen können nicht durch tierische Plasmodien parasitiert werden , mit Ausnahme von Plasmodium knowlesi , einem primären Malariaparasiten, der häufig in Südostasien vorkommt. Es verursacht Malaria bei Langschwanzmakaken, kann aber auch Menschen auf natürlichem oder künstlichem Wege infizieren. Plasmodium knowlesi ist der sechsthäufigste Malariaparasit des Menschen. Von den 133 aufgeführten Arten der Gattung Plasmodium sind nur vier spezifisch menschlich: Plasmodium falciparum, das für eine große Mehrheit der Todesfälle verantwortlich ist, und drei weitere, die „gutartige“ Formen von Malaria verursachen, die im Allgemeinen nicht tödlich sind Plasmodium vivax , Plasmodium ovale und Plasmodium Malaria . Plasmodium knowlesi, das bis vor kurzem noch für Affenarten spezifisch gehalten wurde, ist heute zu den auch den Menschen befallenden Plasmodien zu zählen, die ebenfalls im Allgemeinen gutartig sind ( siehe ausführlichen Abschnitt: " Ursachen ").
Die Ursache der Krankheit wurde am . entdeckt 6. November 1880im Militärkrankenhaus von Constantine ( Algerien ) von einem Arzt der Armee Französisch, Alphonse Laveran , der den empfangenen Nobelpreis für Physiologie oder Medizin in 1907 . Es war in 1897 , dass der englische Arzt Ronald Ross (Nobelpreis 1902 ) , die bewiesen , Anopheles Mücken die Vektoren der Malaria waren (bis zu diesem Zeitpunkt die „schlechte Luft“ aus den Sümpfen ausgeht , wurde für die Ausbreitung der Krankheit verantwortlich gemacht).
Etymologie
Der Begriff Malaria kommt vom lateinischen palus , „ Sumpf “.
Das Wort Malaria leitet sich vom italienischen mal'aria "schlechte Luft" ab. Dieser Begriff wird weltweit häufig verwendet, insbesondere von Englisch- und Italienischsprechenden .
Geschichte
Aus den Ursprüngen der Menschheit
Bei Schimpansen , der dem Menschen am nächsten stehenden Gattung , kommen Malaria-ähnliche Parasiten vor . Schimpansen beherbergen einen Malariaparasiten, Plasmodium reichenowi , einen nahen Verwandten von Plasmodium falciparum ; die Gorillas beherbergen inzwischen das Plasmodium falciparum, das möglicherweise die Ursache des menschlichen Parasiten ist (die DNA-Sequenzierung von Plasmodium falciparum im Kot infizierter Gorillas zeigt durch phylogenetische Analyse, dass dieser Parasit primatophil der Vorfahre des beim Menschen gefundenen Stammes ist).
Malaria befällt den Menschen seit dem Pleistozän vor über 50.000 Jahren und ist seit Beginn der Geschichte unserer Spezies ein Krankheitserreger . Dies repräsentiert mehrere tausend Generationen von Menschen, und Malaria gilt als eine der tödlichsten Krankheiten der Menschheitsgeschichte.
Eine umstrittene Spekulation schätzt, dass die Hälfte aller Menschen, die existiert haben, an Malaria gestorben ist: 54 Milliarden Menschen sollen von insgesamt 108 Milliarden, die existiert haben oder noch existieren, gestorben sind.
Menschliche Parasiten und ihre Vektoren (Mücken) entwickelten sich gemeinsam mit menschlichen Gruppen, die sich in Afrika und Eurasien ausbreiteten. Die Übertragung von Malaria war abhängig von anthropophilen Mückenarten (vorzugsweise stechenden Menschen), deren Ausmaß immer durch Umweltbedingungen (Breitengrad, Höhe usw.) begrenzt war.
Eine der Folgen des Alters dieser koevolutionären Assoziation ist die biologische Existenz eines genetischen Polymorphismus im Blut in modernen Populationen . Die Vielfalt der Bevölkerungsbedingungen hat zu einer natürlichen Selektion von Genen für Sichelzellanämie , Thalassämie , Glucose-6-Phosphat-Dehydrogenase-Mangel , erbliche Elliptozytose (in einigen Fällen Ovalozytose ) geführt. Diese Erkrankungen, die die roten Blutkörperchen befallen, bieten einen selektiven Vorteil gegen Malaria ( siehe ausführlichen Abschnitt: „ Genetische Faktoren “).
Vor etwa 10.000 Jahren wurde die Ausbreitung der Malaria begünstigt durch den Klimawandel, den Beginn der Landwirtschaft ( neolithische Revolution ), also zur Sesshaftigkeit mit demografischem Wachstum.
Antike und Mittelalter
Periodische Fieber , die an Malaria erinnern, werden seit der Antike in chinesischen, indischen, assyrischen und griechischen Texten berichtet. Die detaillierteren Beschreibungen sind die von Hippokrates und Autoren des Römischen Reiches . Die mittelalterliche Theorie über eine Krankheit, die mit dem Miasma aus den Sümpfen verbunden ist, bleibt bis zum 19. Jahrhundert in Kraft .
In Januar 2010, bewies ein Team ägyptischer und amerikanischer Wissenschaftler durch DNA- Analysen , dass Tutanchamun zum Zeitpunkt seines Todes an Malaria litt (Vers.1327 v. Chr. J.-C.). In Indien erwähnen die Veden ("Wissenstexte") seit der Antike Malariafieber; Arzt Charaka und Sushruta (wahrscheinlich V th Jahrhundert vor Christus. ) machen es eine Beschreibung und verbinden sie bereits den Mückenstich. Symptome von intermittierendem Fieber wurden von Hippokrates beschrieben ; er verknüpft diese Fieber mit bestimmten Klima- und Umweltbedingungen und teilt sie in drei Typen ein: febris tertiana (alle drei Tage), quartana (alle vier Tage) und dailyiana ou continua (heute tropica genannt ). Gegenüber186 v. Chr. J.-C.In bestimmten Regionen Chinas erscheint die Verwendung von qing hao su (青蒿素) in Kräutertee , die später im Westen Artemisinin genannt wird und aus einer Heilpflanze gewonnen wird, die als Antipyretikum namens qing hao (青蒿) verwendet wird ( Artemisia annua .). oder „ jährlicher Beifuß “). Noch älter in Gebrauch, haben die Wurzeln von chángshān (常山) ( Dichroa febrifuga ) auch unbestrittene medizinische Wirkungen. So wir Hinweise auf Perioden von Malaria-Fieber in China und Symptomen dieser Krankheit in dem finden Huangdi Neijing ( „Der Kanon der Medizin“) aus der Zeit um den I st Jahrhundert vor Christus.
Malaria war in Teilen der Welt weit verbreitet, wo sie heute verschwunden ist, wie in den meisten Ländern Europas (die Krankheit afrikanischer Herkunft, die sich insbesondere im Römischen Reich ausgebreitet hat ) und Nordamerika.
Klassisches Zeitalter
In Teilen Englands war die Sterblichkeit durch Malaria mit der heute in Afrika südlich der Sahara vergleichbar . Obwohl William Shakespeare zu Beginn einer kälteren Periode namens " Kleine Eiszeit " geboren wurde, wusste er genug über die Verwüstungen dieser Krankheit, um sie in acht seiner Stücke zu zitieren. Plasmodium vivax war bis rife 1958 in den Poldern von Belgien und den Niederlanden .
Im frühen XVI th Jahrhundert ist es die Siedler Europäer und ihre Sklaven , die wahrscheinlich Malaria in Nord- und Südamerika gebracht (wir wissen , dass Columbus wurde von der Krankheit vor seiner Ankunft in dem neuen Land leidet). Die spanischen Missionare der Jesuiten sahen, dass die Indianer an der Grenze zum Loxa-See in Peru das Rindenpulver Chinarinden zur Heilung von Fieber verwendeten. In der medizinischen Literatur der Maya oder Azteken findet sich jedoch kein Hinweis auf Malaria . Die Verwendung der Rinde des "Fieberbaums" wurde von jesuitischen Missionaren in die europäische Medizin eingeführt, darunter Barbabe de Cobo, die 1632 damit experimentierten und sie auch exportierten; so dass das kostbare Pulver auch „Jesuitenpulver“ genannt wurde. Eine Studie im Jahr 2012 auf genetischen Marker aus Tausenden von Proben von Plasmodium falciparum den afrikanischen Ursprung des Parasiten in Südamerika bestätigt ( die Europäer selbst von dieser Krankheit durch Afrika betroffen gewesen zu ): es zwischen der Mitte des geliehenen XVI E Jahrhunderts und der Mitte des XIX E Jahrhundert die beiden Hauptrouten des Sklavenhandels , der erste im Norden des südamerikanischen Kontinents (führende Kolumbien von den Spaniern, die zweite führende weiter nach Süden () Brasilien ) durch die Portugiesen.
XVIII - ten und XIX - ten Jahrhundert: erste wissenschaftliche Studien
In 1717 , die post mortem Graphit Pigmentierung der Milz und Gehirn wurde veröffentlicht von Giovanni Maria Lancisi , der Arzt von Papst Clemens XI , in einem Werk, im Jahre 1717 veröffentlicht, auf Malaria De noxiis paludum effluviis eorumque remediis . Er legt Beweise dafür vor, dass die Krankheit durch Fliegen übertragen wird . Lancisi führt das Wort Mal'aria , "schlechte Luft" ein.
In 1820 , Pierre Joseph Pelletier und Joseph Bienaimé Caventou trennten das Cinchonin und Chinin - Alkaloide aus der Rinde Pulver des „Fieberbaumes“, so dass die Schaffung von standardisierten Dosierungen der aktiven Komponenten.
Rund 1832 , François Clément Maillot perfektionierte die kurative und prophylaktische Behandlung von Chinin. Doch erst 1881 wurde sein Beitrag auf dem Malariakongress in Algier offiziell anerkannt.
In 1848 , Johann Friedrich Meckel ( mit dem Spitznamen Meckel der Jüngere) eine große Anzahl von schwarz-braun Granulat im Blut und der Milz eines Patienten festgestellt , die gerade in einem psychiatrischen Krankenhaus gestorben war. Meckel sah wahrscheinlich Malariaparasiten, ohne es zu merken, da er Malaria in seinem Bericht nicht erwähnte, da er dachte, das Pigment sei Melanin .
In 1878 wird die D r Patrick Manson emittiert die erste Annahme , dass die Malaria durch Stechmücken der Gattung übertragen wird , Culex , die die Parasiten absorbieren und legen in dem Wasser , das die menschliche isst.
In 1879 , der deutsche Edwin Klebs und die italienische Ettore Marchiafava bekannt , dass sie die Mittel , die für die Malaria gefunden hatte Bacillus malariae , eine Hypothese , dass Laveran Entdeckungen haben uns vergessen.
In 1880 , Alphonse Laveran gegründet, in Algerien , die Beziehung zwischen den Beobachtungen von Meckel machte die jungen und den Parasiten er zum ersten Mal in dem roten Blutkörperchen von 44 Menschen an Malaria leiden , beobachtet. Als er die Exflagellation sieht , ist er überzeugt, dass bewegliche Geißeln parasitäre Mikroorganismen sind (kleine einzellige Lebewesen, die sich durch Mitose vegetativ vermehren ). Viele Ärzte der Zeit glaubten jedoch noch, dass Protozoen tatsächlich nur veränderte rote Blutkörperchen waren. Laveran wird kämpfen müssen, um seine Theorie durchzusetzen, denn es bleibt abzuwarten, wie diese Organismen in den menschlichen Körper gelangen. Da er keine Stelle erhalten hatte, die ihm erlaubte, seine Forschung fortzusetzen, ging Laveran in den Ruhestand und setzte seine Forschungen über Protozoen am Institut Pasteur als Freiwilliger fort. Es war 1898 , dass er seine veröffentlichte Abhandlung über Malaria . Er sieht auch die Wirkung von Chinin, das diese Parasiten zerstört. Er schlägt vor, dass Malaria durch dieses Protozoon verursacht wird . Dies ist das erste Mal, dass ein Protozoon als Krankheitserreger identifiziert wurde. Diese Entdeckung brachte ihm 1907 den Nobelpreis für Medizin ein . Wissenschaftliche Studien zu Malaria haben gerade ihren ersten bedeutenden Durchbruch erzielt.
In 1880 , Ettore Marchiafava und Angelo Celli , auf Antrag von Alphonse Laveran, Studie unter dem Mikroskop des Fortpflanzungszyklus von Protozoen im menschlichen Blut, und beobachtet , dass sie teilen mehr oder weniger gleichzeitig in regelmäßigen Abständen , und dass die Teilung fällt mit Fieberschüben. In 1885 , nannten sie diese Protozoen Plasmodium .
In 1881 , Carlos Finlay , ein kubanischen Arzt, den Patienten , die mit Gelbfieber in Havanna , behauptete , dass es Mücken , die die Krankheit auf den Menschen übertragen.
In den Jahren 1886 und 1892 veröffentlichte Camillo Golgi seine Ergebnisse über die Häufigkeit und Periodizität von Fieber aufgrund von Malaria und zeigte, dass es mehrere Arten von Malaria gibt, die durch verschiedene Protozoen-Organismen verursacht werden.
In 1891 , Paul Ehrlich bemerkt und Paul Guttman die Anti - Malaria - Eigenschaften von Methylenblau . Diese Entdeckung folgt der von Celli und Guarnieri, die selbst auf früheren Arbeiten von Ehrlich beruhte, die die Affinität dieser Substanz zu bestimmten Zellen zeigten. Ehrlich will die Medikamentenentwicklung vorantreiben, indem er biochemische Unterschiede ausnutzt. Es war das erste Mal, dass ein synthetischer Stoff gegen Malaria wirksam war (bereits 1849 hatte August von Hofmann jedoch bereits das Interesse an der Synthese von Chinin aus Steinkohlenteer unterstrichen ).
In 1895 , das Französisch Expedition nach Madagaskar war eine „Gesundheitskatastrophe“: von 21.600 Menschen ausgestiegen, 5.731 starben an Malaria und 25 starben im Kampf. Beachten Sie, dass sich diese Art von "Katastrophe" oft wiederholen wird, wie während des Vietnamkrieges für nordvietnamesische Soldaten (siehe Artikel über Artemisinin ).
In 1898 , Amico Bignami gelang es experimentell Malaria durch Mücken übertragen. Er zögert nicht, selbst gebissen zu werden und an der Krankheit zu erkranken.
Im Jahr 1898 war es der Brite Ronald Ross , der in Indien arbeitete und regelmäßig mit Laveran und Manson korrespondierte, sich aber schwer vorstellen konnte, warum das Insekt den Parasiten nicht direkt durch Biss übertrug, der schließlich bewies, dass Malaria durch diesen Stich übertragen wurde. Um seine Theorie zu bestätigen, seziert er zwei Jahre lang Malariavögel, die er von Hunderten von Mückenarten beißt, und erst nach diesen zwei Jahren, kurz vor der Entmutigung, bemerkt er eine Art. Mücke, die sich nur an der Oberfläche entwickelt Wasser und ist nur nachts zu sehen: die Anopheles . Dann setzt er seine Forschungen fort; es erntet und zieht die Larven auf und findet Laveran-Protozoen um den siebten Tag im Magen der Anopheles. Der Beweis ist erbracht: Es ist dieses Insekt, das den lebenden Parasiten auf seine Kosten überträgt. Er stellt fest, dass zwischen dem Biss und dem Auftreten der Parasiten im Blut eine Inkubationszeit von 10 bis 14 Tagen notwendig ist. Er hatte gerade bewiesen, dass bestimmte Mückenarten Malaria auf Vögel übertragen, indem er die Parasiten aus den Speicheldrüsen von Mücken isolierte, die sich von betroffenen Vögeln ernähren. Dies brachte ihm 1902 den Nobelpreis für Medizin ein . Nach seinem Rücktritt vom indischen medizinischen Dienst arbeitete Ross für die damals neu gegründete Liverpool School of Tropical Medicine und leitete die Bemühungen zur Ausrottung der Malaria in Ägypten , Panama , Griechenland und Mauritius . Bis in die 1930er Jahre sprachen Forscher von Anopheles maculipennis im Allgemeinen, ohne zwischen den verschiedenen Sorten klar oder genau zu unterscheiden.
In 1899 hat die italienische Zoologe Giovanni Battista Grassi hat, bezogen auf Ross Arbeit (auf Vögel), das gleiche gilt für den Vektor in Menschen und bewiesen , dass der Lebenszyklus von Plasmodium die Mücke als notwendigen Schritt muss. Grassi, Giuseppe Bastianelli und Amico Bignami beschreiben den Entwicklungszyklus von Plasmodium falciparum , Plasmodium vivax und Plasmodium malariae bei Anopheles claviger .
Im folgenden Jahr wurden die Ergebnisse von Finlay und Ross von einem medizinischen Team unter der Leitung von Walter Reed bestätigt ; und die Empfehlungen werden von William C. Gorgas während des Baus des Panamakanals umgesetzt . Die so beschlossenen öffentlichen Gesundheitsmaßnahmen retteten Tausenden von Arbeitern das Leben (da zuvor viele Tausende starben) und halfen bei der Entwicklung zukünftiger Methoden zur Bekämpfung der Krankheit.
XX - ten Jahrhunderts: aufSuche nach Behandlung
Während das Wissen über die Krankheit insbesondere durch die Praxis der Malariatherapie - eine mittlerweile obsolete Behandlung - zunimmt, kennzeichnen die Entwicklung von Malariamedikamenten und der Einsatz von Insektiziden zur Bekämpfung des Parasitenüberträgers diese Zeit. Diese Entdeckungen veranlassten die WHO 1955 , das Globale Malaria-Eradikationsprogramm ins Leben zu rufen. Während dieses Programm sein Ziel noch nicht erreicht hatte und eine latente Form der Parasitose entdeckt wurde, bewegt sich die Forschung auf die Entwicklung eines Impfstoffs zu.
EntdeckungenZu Beginn der XX - ten Jahrhunderts, vor Antibiotika , die Patienten mit Syphilis wurden absichtlich „behandelt“ , indem sie mit Malaria zu infizieren, sie Fieber zu geben. Auch die therapeutische Behandlung mit Malaria oder Malariatherapie ist eine Chance, das Wissen über Malaria erheblich zu erweitern; es ebnete den Weg für die Chemotherapieforschung und blieb bis etwa 1950 in der Praxis .
In 1922 , John William Watson Stephens (in) , identifiziert die 4 th Malaria bekannt Parasiten bei Menschen, P. ovale .
Bereits in den 1930er Jahren hatten Forscher die geringere Sensibilität der schwarzen Bevölkerung gegenüber Malaria festgestellt. In 1949 , wurde Émile Brumpt überrascht keinen Fall von Malaria in Liberia, Gabun, Lagos oder Stanleyville zu finden , wenn es Vektoren waren P. vivax .
Im Jahr 1949 schlug JBS Haldane vor, dass heterozygote Thalassemiker resistenter gegen Malaria sein würden. Im November veröffentlichten Linus Pauling , Harvey Itano , SJ Singer und Ibert Wells in der Zeitschrift Science die ersten Hinweise auf eine menschliche Krankheit, die durch ein abnormales Protein verursacht wurde . Mit Hilfe der Elektrophorese , sie zeigen , dass Personen mit Sichelzellkrankheit haben veränderte Hämoglobin , und dass heterozygote, die sowohl normale und abnormale Formen von Hämoglobin haben, sind resistenter gegen Malaria - Infektionen. So zeigt sich auch, dass die Mendelschen Gesetze die physikalischen Eigenschaften von Proteinen bestimmen und nicht nur deren Fehlen oder Vorhandensein: Dies ist der Beginn der Molekulargenetik .
Antimalariamittel (Antimalariamittel)Trotz seiner außergewöhnlichen Eigenschaften hatte Chinin, ein aus fernen Ländern importiertes Produkt, das in begrenzten Mengen erhältlich ist, den Nachteil, manchmal Nebenwirkungen zu verursachen; außerdem musste seine Verwaltung täglich erfolgen: so viele Anreize zur Adoption und zur Suche nach Ersatzstoffen, die William Henry Perkin bereits 1856 vergeblich versucht hatte . Der Erste Weltkrieg, der Deutschland von Indien und Java - den wichtigsten Chininlieferanten der Welt - abtrennte, veranlasste die Deutschen, Ersatz zu suchen, basierend auf Ehrlichs Beobachtung der Wirkung von Methylenblau .
So wurden nacheinander Plasmoquin (1926), Chinacrin /Sontochin (1930), Rhodoquin (1931) und Certuna (1935) entdeckt . Dabei basierte die deutsche Forschung auf einem 1926 von Roehl entwickelten Tiermodell .
1926 entdeckten deutsche Forscher die Antimalaria-Eigenschaften von Pamaquin / Plasmoquin / Paraquin. Die Struktur dieses ersten von Aminochinoleinen abgeleiteten Malariamedikaments wurde jedoch erst 1928 bekannt gegeben . Britische, französische und russische Forscher haben bereits die Antimalariawirkung von Molekülen der 8-Aminochinolin-Reihe festgestellt. Sie suchen nach anderen Wirkstoffen. In 1930 , Ernest Fourneau entwickeln und sein Team am Institut Pasteur von rhodoquine , wirksam bei vielen geringeren Dosen als plasmoquine.
In Algerien, die Brüder Edmond und Etienne Sergent in der ersten Hälfte des XX - ten gesetzt Jahrhunderts auf Antrag von bis Emile Roux Lehre der Grundlagen des Anti Malaria Kampfes in Nordafrika zu legen. Diese Arbeit wird zu einem allmählichen Rückgang der Malaria in Algerien führen und viele Leben werden gerettet.
In der Zwischenkriegszeit gibt es zwei Tiermodelle, die die Suche nach synthetischen Malariamitteln unterstützen; eine basiert auf Affen-Malaria, die im großen Maßstab nicht praktikabel ist, die andere, die häufiger verwendet wird, ist die Vogel-Malaria, die hauptsächlich kanarische Malaria durch verschiedene Arten von Plasmodien verwendet.
In den gleichen 1930er Jahren synthetisierten und testeten Hans Andersag und seine Kollegen in den Elberfield-Laboratorien der IG Farben in Deutschland etwa 12.000 verschiedene Komponenten und schafften es, Resochin , einen Ersatz für Chinin , herzustellen . Es ist mit Chinin verwandt, weil es einen Chinolinkern hat . Dieses Resochin (RESOrcinat eines 4-AminoCHINolins: 7-Chlor-4 - [[4-(diethylamino)-1-methylbutyl]amino] chinolin ) und ein ähnlicher Bestandteil, Estonchin (3-Methylresochin) werden 1934 in Zusammenarbeit mit amerikanischen Unternehmen durch mehr als 2000 Vereinbarungen zwischen IG Farben und ausländischen Unternehmen, wie Standard Oil of New Jersey , DuPont , Alcoa , Dow Chemical , Agfa , Winthrop Chemical Company und anderen amerikanischen Unternehmen. Dieses Medikament wird später Chloroquin genannt . Es ist ein Pigmentbiokristallisationsinhibitor und eines der besten antimikrobiellen Mittel, die jemals entwickelt wurden. Chinin befällt wie Chloroquin Malariaparasiten zu Beginn ihres Lebenszyklus, wenn die Parasiten Hämatinpigmente bilden , die aus dem Abbau von Hämoglobin stammen .
Das Proguanil wurde 1944 von Curd, Davey und Rose, britischen Forschern von Imperial Chemical Industries, entdeckt . Das Pyrimethamin schließlich wird zwischen 1950 und 1952 vom Labor Burroughs-Wellcome entwickelt. In den 1970er Jahren mit Sulfadoxin in Verbindung gebracht, bildete es Fansidar.
In den 1950er und 1960er Jahren ersetzten synthetische Antimalariamittel, deren Herstellungskosten sehr niedrig waren, tendenziell das teurere extrahierte Chinin.
Während des Vietnam - Krieges , als Reaktion auf einen ausdrücklichen Wunsch von der „ Vietcong “, eine systematische Untersuchung von mehr als 200 chinesischen Heilpflanzen wurde unter der Leitung von unternommen Pharmakologe Tu Youyou und ihrer Arbeitsgruppe in Peking in 1972 . Qing hao su (青蒿素), im Westen Artemisinin genannt , wird bei niedriger Temperatur in einem neutralen Medium (pH 7) aus getrockneten Qing hao (青蒿) Pflanzen nach Ge Hongs Anweisungen extrahiert . Dieser war die erste, in der IV - ten Jahrhundert die Verwendung von qing hao zur Behandlung von „empfehlen Wechselfieber “ in seinen Anforderungen Handbuch für medizinische Notfälle . Er empfiehlt, die Beifußblätter und -zweige über Nacht einzuweichen, den bitteren Saft auszupressen und direkt zu trinken. Derzeit werden Derivate in Kombinationen verwendet: Artemether in Kombination mit Lumefantrin , Artesunat - Amodiaquin , Dihydroartemesinin - Piperaquin.
Die ersten In-vitro- Kulturen des Parasiten in seiner Blutphase wurden 1976 von Trager und Jensen durchgeführt, was die Entwicklung neuer Medikamente erheblich erleichterte.
DDTDie insektiziden Eigenschaften von DDT (Dichlordiphenyltrichlorethan) wurden 1939 von Paul Hermann Müller bei Geigy Pharmaceutical in Basel , Schweiz, anhand von Pyrethrum aus zerkleinertem dalmatinischen Pyrethrum (Pflanze der Familie der Chrysanthemen ) festgestellt . Die Ausbringung von DDT ist eine Standardmethode des Insektenschutzes. Aufgrund der Umweltbelastung von DDT und der von Mücken entwickelten Resistenz wird DDT jedoch immer weniger verwendet, insbesondere in Gebieten, in denen Malaria nicht endemisch ist ( siehe ausführlichen Abschnitt: " Die Mittel zur Bekämpfung oder zum Schutz gegen Mücken "). Dies ist insbesondere seit 1972 der Fall, als die Vereinigten Staaten über AID und die Weltbank drohten, Importe zu verbieten und die Finanzierung von Ländern, die DDT verwenden, zu kürzen.
1948 erhielt Paul Müller den Nobelpreis für Medizin.
Simian und menschliche MalariaIn den 1920er Jahren injizierten amerikanische Forscher Blut von Affen verschiedener Arten in den Menschen, um die Möglichkeit einer Übertragung von Malaria von Affen auf den Menschen zu bestimmen.
In den Jahren 1932-33 wiesen Sinton und Mulligan die Anwesenheit von Plasmodium gonderi in Cercopithecidae nach . Bis in die 1960er Jahre war eine natürliche Infektion bei Affen in Indien nur ausnahmsweise beobachtet worden, obwohl sie bereits in großer Zahl zu Forschungszwecken genutzt wurden.
Allerdings war bereits seit 1932 bekannt, dass P. knowlesi durch infiziertes Affenblut auf den Menschen übertragen werden kann. Die Frage der Übertragbarkeit von Affen-Malaria auf den Menschen, die insbesondere im Rahmen eines Tilgungsprogramms betrachtet wurde, gewann 1960 wieder an Interesse, als die Möglichkeit der Übertragung ( über eine Mücke) von Malaria von einem Affen auf einen Menschen entstand. 1969 wurde der Chesson-Stamm von Plasmodium vivax zum ersten Mal an einen nicht-menschlichen Primaten angepasst.
Seit 2004 ist bekannt, dass P. knowlesi, das für die Affen-Malaria verantwortlich ist, für Infektionen beim Menschen verantwortlich ist, die als P. falciparum behandelt werden sollten .
Latente ParasitoseObwohl verschiedene Blutstadien und die Malaria - Vektor (die Anopheles ) werden aus dem identifiziert worden XIX ten Jahrhundert war es nur in 1980 , dass die latente Form (Exo-Erythrozyten Sekundär Zyklen , die in der Leber parasitosis für 3 bis 5 Jahre halten werden oder mehr bei P. vivax , 2 oder 3 bei P. ovale und lebenslang bei P. malariae ) des Parasiten in der Leber beobachtet. Schließlich erklärt die Entdeckung dieser latenten Form des Parasiten, warum Individuen von Malaria geheilt erscheinen, aber mehrere Jahre nach dem Verschwinden des Parasiten aus ihrem Blut einen Rückfall erleiden ( siehe ausführlichen Abschnitt: „ Hepatische Phase “).
Zeitgenössische Entwicklungen und Perspektiven
Pharmakologie- In 2004 hat das Team von D r Jonathan Venner der University of Nebraska von Omaha werden Artemisinsäure zu synthetisieren geschaffen , in umgewandelt werden Artemisinin effektiver ( in vitro ) , wie das natürlich produziert. Dieses Molekül (Arterolane, OZ-277 oder RBx11160) wurde in Kombination mit Piperaquin im Medikament Synriam verwendet.
- Im März 2006 demonstrierten zwei internationale Teams die Wirksamkeit verschiedener Anlagen, darunter auch Quassia .
- Am selben Tag entwickelten Forscher der Universität Lille I ein Molekül, Ferroquin , indem sie ein Ferrocen an einer bestimmten Stelle des Chloroquin-Moleküls aufpfropften . Ferroquin soll bis zu 30-mal wirksamer sein als Chloroquin. Die auf Ferroquin basierende Monotherapie und ihre Kombination mit Arthenusat wurden an 326 Probanden getestet, hauptsächlich an kleinen Kindern in Malariagebieten Zentralafrikas. Es wurden 3 Dosen der Kombination getestet, die in 97 bis 99% der Fälle zu Heilungen führten. Die Monotherapie hatte eine Erfolgsrate von 79 %, was in der gleichen Wirksamkeitsreihenfolge wie andere vorbestehende Monotherapien liegt.
- Im September 2006 isoliert ein französisches Team das Antimalariaprinzip ( Simalikalacton D ) der Infusion von Quassia Amara, die in Guyana gegen Malaria verwendet wird.
- In 2008 , Biologen vom Georgia Institute of Technology in Atlanta gezeigt , dass bestimmte natürliche fungizide Verbindungen der Rotalge Callophycus Sägezahnmuskel die Wirkung gehemmt Plasmodium ; obwohl der Zusammenhang zwischen antimykotischer , antibakterieller und Antimalaria-Wirkung noch nicht verstanden ist.
- 2009 (Veröffentlichung Februar 2010) identifizieren Forscher des Georgia Institute of Technology in Atlanta infektionshemmende Verbindungen, sogenannte „ Bromphykolide “, die in vitro sehr wirksam gegen Mykosen und gegen das Plasmodium falciparum sind .
- In Januar 2010, GlaxoSmithKline gibt bekannt, dass es der wissenschaftlichen Gemeinschaft kostenlos eine Liste mit mehr als 13.500 Molekülen – und ihren chemischen Strukturen – mit potenzieller Wirkung gegen P. falciparum zur Verfügung stellen wird, um die Entwicklung neuer Behandlungsmethoden gegen die Krankheit anzuregen.
- 2010 entdeckten Forscher der Johns Hopkins Bloomberg School of Public Health, Johns Hopkins University , Baltimore , dass ein Bakterium der Gattung Enterobacter, das in der Darmflora von Anopheles gambiae lebt, Plasmodium falciparum durch freie Radikale abtötet . Ungefähr 25% der Anopheles, die in der Nähe des Johns Hopkins Malaria Research Institute in Macha (südliches Sambia ) gefangen wurden, enthielten diesen Bakterienstamm. Die Studie zeigte, dass die Bakterien das Wachstum von P. falciparum in menschlichen In-vitro- Kulturen um bis zu 99% hemmten, ebenso wie im Verdauungssystem von Anopheles.
- In den Jahren 2010 und 2011 wurden zwei neue Klassen von Malariamedikamenten entdeckt und befinden sich in klinischen Studien: Spiroindolone und Imidazolpiperazine.
- Im September 2012 war die Synthese von Artemisinin erfolgreich, wodurch die Produktion von Arzneimitteln nicht mehr durch die des Beifußes eingeschränkt werden konnte.
Der Nobelpreis für Medizin 2015 wurde dem Iren William Campbell , dem Japaner Satoshi Ōmura und der Chinesin Tu Youyou für ihre Arbeiten zur Behandlung parasitärer Erkrankungen einschließlich Malaria verliehen.
ImpfungenDer erste Malaria- Impfstoff , SPf66, basierend auf einem synthetischen Peptid , wurde im Januar 1986 von Manuel Elkin Patarroyo entwickelt . Allerdings war seine Wirksamkeit gegen P. falciparum ziemlich gering oder sogar null .
Derzeit basieren drei Arten der Forschung der zweiten Generation auf Antigenen aus verschiedenen Stadien des parasitären Evolutionszyklus:
- Impfstoffe im antierythrozytären Stadium: diese zielen darauf ab, zu verhindern, dass der Sporozoit in Leberzellen eindringt oder sich dort entwickelt ;
- Impfstoffe gegen das asexuelle Blutstadium (Antimerozoiten): Diese verhindern, dass Merozoiten in rote Blutkörperchen eindringen oder sich dort entwickeln ;
- Impfstoffe, die die Übertragung blockieren: Sie induzieren Antikörper , die die Reifung der sexuellen Stadien des Parasiten bei Anopheles verhindern.
Seit 1992 wird bei GlaxoSmithKline Biologicals in Rixensart , Belgien , ein Anti-Timerozoiten-Impfstoff namens RTS, S entwickelt . Im Dezember 2005 , Dr. Pedro L. Alonso der Universität Barcelona veröffentlichte ermutigenden Ergebnisse , weil der Impfstoff von der effektiven erweist 1 st Injektion in 30% der Fälle und spart die Hälfte der Krisen. Aus 26. Mai 2009Im Jahr 2013 durchlief es klinische Phase-III-Studien, die die Überlegenheit von RTS, S / AS01 gegenüber anderen Adjuvantien zeigten. Es wird aus synthetischen parasitären Peptiden und rekombinanten Proteinen (Lage ist , mit einem anderen Protein genetische Information austauschen) oder DNA (in den gefundenen Mitochondrien und die apikal Plastiden von Plasmodium ). In dem Wissen, dass der Parasit, um die roten Blutkörperchen zu durchdringen , die Form eines Proteins annimmt und in der Lage ist, etwa sechzig Mal zu mutieren, um das Immunsystem zu täuschen, verwendet dieser Track zwei rekombinante Proteine, die er fusioniert:
- Teil des Circumsporozoiten-Proteins (CSP = Circum Sporozoite Protein ) von P. falciparum (RTS);
- das Antigen der Oberfläche des Hepatitis-B- Virus (S);
- ein Adjuvans (AS01 oder AS02 resp.) , die von 250 ul zusammengesetzt ist von Öl in Wasser - Emulsion , 50 & mgr; g von QS21 - Saponin und 50 & mgr; g von (MPL) immunostimulant monophosphoryc Lipid A.
RTS, S / AS01 erhielt im Juli 2015 eine positive Stellungnahme der EMA und wird unter dem Namen Mosquirix vertrieben. Es schützt auch gegen das Hepatitis - B . Für Anfang 2018 ist ein WHO- Pilotprojekt mit Ghana , Kenia und Malawi geplant .
Andere Forscher streben nach einer Impfstofflösung:
- Seit 2002 untersucht die Fakultät für Biologie und Medizin (FBM) der Universität Lausanne in der Schweiz einen Antitimerozoiten-Impfstoff namens PfCS102 / AS02A basierend auf einem synthetischen Circumsporozoiten- Peptid (PfCS = Peptide Circum Sporozoïte Protein ) von P. falciparum (PfCS102 ) mit einem Adjuvans verstärkt. Anfänglich wurde dieses Adjuvans durch Montanide ISA 720 ersetzt, da es durch AS02A von GSK Bio ersetzt wurde, da es eine bessere Reaktion des Immunsystems bewirkt . Die erhaltenen Ergebnisse sind vergleichbar mit RTS, S / AS02A. Seit 2005 befindet es sich in klinischen Studien der Phase II .
- Im November 2005 gab das Institut Pasteur den Beginn klinischer Phase-I-Studien am Menschen mit einem Prototyp eines auf Antigenen basierenden Antimerozoiten-Impfstoffs mit der Bezeichnung MSP3 bekannt. Um es zu entwerfen, untersuchten die Forscher die Mechanismen von Menschen mit natürlicher Immunität.
- Im Jahr 2006 forderte das US-Verteidigungsministerium (DoD) das Institute of Medicine (IOM) der National Academy of Sciences (NAS) auf, das 1986 begonnene Forschungsprogramm zur Entwicklung eines Impfstoffs gegen P. falciparum für das Militär wieder aufzunehmen .
- Von November 2006 bis Dezember 2007 testeten die Medizinische Fakultät der University of Maryland und die University of Bamako gemeinsam in klinischen Studien der Phase I einen FMP2.1/AS02A-Impfstoff. Sein Wirkstoff ist ein aus P. falciparum gewonnenes Protein (FMP2.1), das durch das Adjuvans AS02A verstärkt wird. Ein in Bandiagara in Mali an 100 Kindern im Alter von 1 bis 6 Jahren durchgeführter Test zeigte, dass die pharmakodynamische Gewöhnung an den Wirkstoff sicher war und die Immunantwort ein Jahr nach der Impfung hoch blieb. Auf dieser Grundlage ging das gleiche Team von Mai 2007 bis Juli 2009 zu klinischen Phase-II-Studien an 400 Kindern über.
- Im Januar 2010 kündigte die University of Central Florida in Orlando einen oralen oder injizierbaren Impfstoffkandidaten an, der sowohl gegen Malaria als auch gegen Cholera wirksam ist . Es zielt auf die systemische und mukosale Immunität über ein antigenes Konstrukt ab, das Epitope der Cholera-Toxin- B-Untereinheit (CTB) mit apikalen Membran- (AMA1) und Oberflächenprotein- (MSP1)-Antigenen von Merozoiten von P. falciparum verschmilzt . Die Chloroplasten von transplastomischem Tabak und Salat wurden als Reaktor zur Herstellung dieser Proteine getestet. Letztere konnten der Studie zufolge, extrahiert und in Mäuse injiziert, diese 300 Tage lang vor dem Eindringen des Parasiten in rote Blutkörperchen und vor Cholera-Toxin schützen. Die Immunantwort wäre vom Tr1/Th2-Typ. Dieses Verfahren ist patentiert und könnte – sofern es sich beim Menschen als ähnlich wirksam erweist – die Herstellung eines kostengünstigen Impfstoffs ermöglichen, der bei oraler Anwendung keine Kühllagerung erfordert.
- 2015 lieferte der Impfstoff „RTS, S“ von GlaxoSmithKline vielversprechende Ergebnisse, enttäuschte jedoch während der Phase-III-Tests mit einer Reduktion von nur 40 % der Infektionen und weniger als 30 % bei der schweren Form (wobei vier Injektionen erforderlich waren).
- Im Jahr 2021 erreicht der an der Universität Oxford entwickelte und 2019 getestete R21 / Matrix-M-Impfstoff eine Rekordwirksamkeit von 77 % über ein Jahr. An der letzten Phase der Vorabprüfungen nehmen 4.800 Kinder aus vier verschiedenen Ländern teil.
Vielmehr wollen Genetiker den Parasiten nicht beim Menschen bekämpfen, sondern bei seinem Überträger, der Mücke.
Im Jahr 2000 gelang es dem Team von Professor Andrea Crisanti vom Imperial College London , die erste gentechnisch veränderte Mücke zu erschaffen. In 2003 , erkannte sie , dass , wenn das Markergen für etwa dreißig Generationen während der Befruchtung zwischen veränderten Moskitos beharrt, es nur über 4 bis 16 Generationen bei der Befruchtung mit einer unmodifizierten Mücke überlebt.
Seit April 2001 führt ein Konsortium International die vollständige Sequenzierung des Genoms von Anopheles gambiae durch . Es wird von der Tropenkrankheitsforschung (TDR) gesponsert. Diese Sequenzierung wurde Genoscope in Évry und Celera Genomics in Alameda anvertraut . Das Ziel ist es, die Gene zu identifizieren, die an der Immunität der Mücke gegen Plasmodium- Parasiten oder an ihren Geruchs- und Geschmacksrezeptoren beteiligt sind, um letztendlich Moleküle für die Mücke anzuziehen oder abzuwehren sowie auf diese Proteasen abzuzielen, die an ihrer Immunantwort beteiligt sind.
das 15. Juli 2010, gibt Entomologie-Professor Michael Riehle bekannt, dass es ihm mit seinem Team an der University of Arizona gelungen ist , eine genetisch veränderte Anopheles Stephensi- Weibchen zu erschaffen, die in der Lage ist, Parasiten in ihrem Körper zu zerstören und daher die Krankheit nicht übertragen kann. Forscher untersuchen nun, wie man „normale“ Anopheles-Populationen in der Natur durch solche aus dem Labor ersetzen kann, in der Hoffnung, dass diese Mücken nicht durch die Übertragung anderer Krankheiten invasiv werden oder der Parasit diese Resistenz nicht umgeht.
Epidemiologie
Verbreitung in der Welt
Entwicklung der geschätzten Zahl der Todesfälle durch Malaria in der Welt.
In den 1990er Jahren verursachte Malaria jährlich 400 bis 900 Millionen Fieberfälle und zwischen 700.000 und 2,7 Millionen Todesfälle oder durchschnittlich ein Todesfall alle 30 Sekunden. Im Jahr 2012 starben zwischen 473.000 und 789.000 Menschen an Malaria. Die überwiegende Mehrheit der Opfer sind Kinder unter 5 Jahren, wobei auch Schwangere besonders gefährdet sind, da die Plazenta ein Angriffsziel für Parasiten ( Plasmodium falciparum ) ist. Trotz der Bemühungen, die Übertragung der Krankheit zu reduzieren und ihre Behandlung zu verbessern, hat sich seit Anfang der 1990er Jahre wenig geändert: Die Sterblichkeit scheint seit Ende der 2000er Jahre zurückgegangen zu sein und wird 2010 auf 1,2 Millionen Menschen geschätzt.
Eine Koinfektion mit HIV erhöht die Sterblichkeit nicht und ist weniger problematisch als eine Koinfektion mit Malaria/ Tuberkulose , wobei die beiden Krankheiten normalerweise unterschiedliche Altersgruppen befallen: Malaria tritt häufiger bei Kindern und Jugendlichen auf, während Tuberkulose mehr ältere Menschen betrifft. Malaria und HIV tragen jedoch zu ihrer gegenseitigen Verbreitung bei: Malaria erhöht die Viruslast, und eine HIV-Infektion erhöht die Wahrscheinlichkeit einer Malaria-Infektion.
Malaria ist in den intertropischen Gebieten Amerikas, in vielen Teilen Asiens und in den meisten Teilen Afrikas endemisch. In Afrika südlich der Sahara werden jedoch 85 bis 90 % der Todesfälle durch Malaria festgestellt. Die geographische Verteilung der Krankheit innerhalb großer Gebiete ist komplex, und daher liegen Malaria- und Nicht-Malaria-Gebiete nahe beieinander. In Trockengebieten lassen sich Malariaperioden mit Niederschlagskarten fehlerfrei vorhersagen. Anders als Denguefieber ist Malaria auf dem Land häufiger als in den Städten. So sind beispielsweise die Städte Vietnam, Laos und Kambodscha praktisch frei von Malaria, aber auf dem Land bleibt sie präsent. Im Jahr 2016 wurde nach Angaben der Weltgesundheitsorganisation in Sri Lanka in drei aufeinander folgenden Jahren kein Malariafall registriert ; es ist damit nach den Malediven das zweite Land in Südostasien, das Malaria ausgerottet hat. Das China wurde zum30. Juni 2021das vierzigste Gebiet, das diese Krankheit ausgerottet hat. In Afrika hingegen kommt Malaria sowohl in ländlichen als auch in städtischen Gebieten vor, obwohl das Risiko in Großstädten reduziert ist. Globale endemisch Ebene der Krankheit haben sie seit den 1960er Jahren kartiert. Doch der britische Wellcome Trust ist die Finanzierung von Malaria Atlas - Projektes , dies zu korrigieren und die Belastung dieser Krankheit in der Zukunft zu beurteilen.
Schließlich ist Malaria die weltweit häufigste parasitäre Erkrankung. Es ist die 1 st Priorität für die WHO als ihre direkten Verwüstungen ihrer sozioökonomischen Auswirkungen , einschließlich: schwache Leistungen zu führenden Unterernährung und Unterentwicklung.
Europa
Bis zum XIX - ten Jahrhundert , könnten Malaria - Epidemien nach Nordeuropa auftreten. Der Rückgang der Malaria in Europa ist hauptsächlich auf das Austrocknen von Sümpfen und die Entwässerung von Feuchtgebieten zurückzuführen . Das Verschwinden der Malaria in Frankreich überraschte die Forscher derart, dass man in diesem Zusammenhang von einem spontanen Verschwinden, ja sogar von einem mysteriösen Verschwinden sprechen könnte. Es scheint, dass dieses Verschwinden mehrere Ursachen hatte. In Regionen wie der Sologne beispielsweise haben verschiedene agronomische Innovationen, insbesondere in Bezug auf die Anbaupraktiken, dabei einen nennenswerten Beitrag geleistet und ihre Wirkung kumuliert. Die Krankheit begann sich, wie auch anderswo in Europa, vor der Einnahme von Chinin zurückzubilden, das zudem anfangs unangemessen, zu spät oder in zu geringer Dosierung eingesetzt wurde. Die Einführung von Chinin trug jedoch dazu bei, das Verschwinden der Krankheit in Gebieten zu beschleunigen, in denen sie rückläufig war.
In GriechenlandIm Jahr 2016 verbot das griechische Zentrum für die Kontrolle und Prävention von Krankheiten die Blutspende in 12 Gemeinden im ganzen Land wegen Malaria, nachdem die Infektion 40 Jahre lang als verschwunden galt.
In FrankreichAuf dem französischen Festland ist Malaria erst seit relativ kurzer Zeit verschwunden. Die Krankheit war noch im gemeinsamen XIX - ten Jahrhundert. Es war noch in 1931 in dem Marais Poitevin , Brennt , die elsässische Ebene , Flandern , Land , in Sologne , Puisaye , im Golf von Morbihan , in der Camargue ... Die ganzen Mittelalters und bis zu XV th - XVI th Jahrhunderte betrifft Malaria hauptsächlich Kampagnen; dies selbst dann, wenn eine große Anzahl von Städten entlang der Flüsse für die Bequemlichkeit des Transports errichtet wurden und trotz der periodischen Überschwemmungen dieser Flüsse an vielen Orten. Die Renaissance erlebte einen Anstieg des Fiebers, die Religionskriege zwangen die Stadtbewohner, sich in Mauern einzuschließen, die von Gräben mit stehendem Wasser umgeben waren. Auch in Paris das Ende des XIX - ten Jahrhunderts, während der großen Werke der Haussmann : in der Tat diese Werke haben verursacht erhebliche Ausgrabungen und langfristige. Die Pfützen, Teiche und andere stehende Wasserstellen hielten lange an und führten zu einer Vermehrung von Anopheles inmitten einer großen Konzentration von Menschen. Außerdem kamen viele Arbeiter aus infizierten Regionen und trugen das Plasmodium .
Die Epidemie von Pithiviers im Jahr 1802 , motiviert durch ihre Schwere, die Entsendung einer Kommission der medizinischen Fakultät; Grund war ein sehr großes Hochwasser ungewöhnlichen Ausmaßes, das die umliegenden Wiesen mehrere Wochen lang mit Wasser bedeckt hatte.
Diese Krankheit wurde von ausgerottet Korsika in 1973 . Zur Zeit der römischen Präsenz unbekannt , wurde dort bei Vandalenangriffen Malaria eingeschleppt . Von 1970 bis 1973 erlebte Korsika seine letzte Epidemie nicht importierter Fälle von Plasmodium vivax . Bemerkenswert ist, dass im Jahr 2006 ein indigener Fall von Plasmodium vivax auf der Insel aufgetreten ist . Seitdem handelt es sich bei fast allen in Frankreich beobachteten Fällen um importierte Malaria. Für die zuletzt genannten Epidemien waren Truppen aus den Kolonien verantwortlich.
Die kritischen Faktoren , die die Verbreitung oder Ausrottung der Krankheit haben Auswirkungen auf Veränderungen im Verhalten der Menschen (landwirtschaftliche Methoden vor allem Bevölkerungsteilen , etc.), den Lebensstandard ( Armut war und ist die Hauptursache für Mortalität) und Bevölkerungsdichte (die je größer die menschliche Dichte, desto größer die Dichte der Mücken).
Die Verwendung von Chinin und Chinin wird Strom zweite Hälfte der XIX - ten Jahrhundert. P. malariae , die dafür anfälliger ist, verschwand vor P. vivax . Die verwendeten Dosen reichen jedoch nicht aus, um die Entwicklung von Hämatozoen beim Menschen zu verhindern.
Ein weiterer bestimmender Faktor: Die Zuchtmethoden ändern sich. Die dauerhafte Behausung nimmt zu, was die Rückgewinnung der Gülle ermöglicht. Im Jahr 1893 waren in der Umgebung von Straßburg nur noch drei oder vier Gemeinden mehr als 12% ihrer Nutzfläche für Weiden reserviert. Die Flächen natürlicher (Nass-)Wiesen nehmen zugunsten von gepflügtem (rekultiviertem) Land ab - dies vor allem in Gebieten mit reichhaltiger Landwirtschaft. Die Zahl der Tiere nimmt zu, was die Angriffe von Mücken auf den Menschen um den gleichen Betrag verringert.
Ein dritter Faktor kommt ins Spiel: die Flächennutzungsplanung , die mehrere Aspekte umfasst. 1821 wurde ein Gesetz zur Austrocknung unhygienischer Teiche verabschiedet. Dieses Gesetz wurde im Großen und Ganzen wenig befolgt; Die Idee wurde jedoch ins Leben gerufen, und die Teiche, die den Häusern am nächsten waren, mussten am zahlreichsten gefüllt werden (weil sie leichter zugänglich waren). Erwachsene Mücken bewegen sich jedoch nicht weiter als 300 m von ihrem Ausgangspunkt entfernt. Diese Austrocknung war daher sicherlich eine wichtige Ursache für die Rückbildung der Krankheit.
Ein weiterer Aspekt der Flächennutzungsplanung ist die Erhöhung der Anzahl von Gräben und deren bessere Pflege, wodurch das Land besser entwässert werden kann.
In den Landes und der Sologne spielt auch die Wiederaufforstung eine Rolle, da Bäume das Wasser effizienter ableiten als eine kleinere Baumkrone.
Die Art des Pflug ändert: die Doppel brabant , die flach Pflug ermöglicht, niedrigere Furchen gibt (also weniger stehendes Wasser in der Mulde der Furchen in nassen Perioden) und ermöglicht auch tiefer pflügen (daher besser schwerer Erde Abwischen), begann Verbreitung ab 1850 in Brie , ersetzt den nicht umkehrbaren Pflug und seine Derivate , die das Pflügen in Graten ermöglichten . Auch das Kalken verbreitet sich, was schwere Böden auflockert und somit das Trocknen erleichtert. Der Tidenhub trägt zur Aufnahme von Oberflächenwasser bei.
All diese agronomischen Maßnahmen tragen erheblich zur Verringerung von Malaria- und anderen Fieberepidemien bei. Bis zum Ersten Weltkrieg gab es nur noch wenige sehr lokalisierte Ausbrüche.
Endemische Malaria verschwand 1960 in Frankreich vollständig.
In Frankreich haben sich in zwanzig Jahren 40 Menschen auf Flughäfen mit Mücken infiziert, die in Flugzeugen aus Malariagebieten eingeflogen sind.
Auf der Insel La Réunion und der Republik Mauritius war Malaria vor 60 Jahren die häufigste Todesursache. Die Ausrottung der Krankheit wurde 1979 von der Weltgesundheitsorganisation bestätigt .
Zunahme importierter MalariaImportierte Malaria wird hauptsächlich bei Reisenden, Migranten und Soldaten aus endemischen Ländern beobachtet. Es wird von einem Netzwerk von rund hundert freiwilligen Spitälern in Verbindung mit dem Nationalen Referenzzentrum (CNR) für Malaria überwacht.
Diese Malaria ist ein Spiegelbild der Weltlage. Aufgrund seiner Situation fungiert Frankreich als „Wächter“ für die Ereignisse in endemischen Ländern, hauptsächlich in Afrika südlich der Sahara. Nach einer deutlichen Verbesserung um den Zeitraum 1990-2010 stagniert die Weltlage. Seit 2015 verzeichneten laut WHO elf Länder einen Anstieg der Fälle.
Frankreich ist das Industrieland mit der höchsten Zahl importierter Malariafälle mit fast 5.000 Fällen pro Jahr. Im Jahr 2017 wurden 2.721 Fälle von Malaria beim CNR gemeldet, d. h. rund 5.220 Fälle , die nach der Repräsentativität des Überwachungsnetzes geschätzt werden, ein Anstieg von 10,3 % gegenüber 2016.
Auch im Jahr 2017 betrafen 82,8% der gemeldeten Fälle Personen afrikanischer Herkunft und 95% aus Subsahara-Afrika. Von insgesamt 59 Kontaminationsländern repräsentieren 15 Länder 92,4 % der gemeldeten Fälle. Die ersten drei sind Côte d'Ivoire (30%), Kamerun (20%) und Guinea (mehr als 5%). Unter diesen afrikanischen Ländern nehmen einige ab oder zu, abhängig von der Zahl der Reisenden oder des Militärpersonals aus Gebieten, in denen die Malaria zurückgeht oder zunimmt.
Insgesamt wurden 13 Todesfälle gemeldet (Letalität 0,48% für alle Fälle und 3,4% für schwere Formen). Die Nichteinhaltung von Präventionsempfehlungen (fehlender Schutz vor Mücken und Chemoprophylaxe) ist die Ursache in den meisten Fällen. Ein zusätzlicher Informationsaufwand ist bei den aus Afrika stammenden Probanden, die ihre engen Verwandten in ihrem Herkunftsland besuchen, notwendig.
Der Migrant, der neu in einem Endemiegebiet ist, präsentiert sich aufgrund seiner erworbenen Immunität selten mit Malaria. Diese Immunität verschwindet in weniger als 4 Jahren in Frankreich. Der Migrant erkrankt dann an Malaria, wenn er während der Ferienzeit in Frankreich ins Land zurückkehrt, was in Westafrika im Allgemeinen der Regenzeit entspricht, in der die Übertragung am intensivsten ist.
Hochrisikoregionen
Nachdem sie in fast der gesamten bewohnten Welt wütete, sind 90 Länder (99 Länder laut WHO-Bericht 2011) von Malaria betroffen, hauptsächlich die ärmsten in Afrika, Asien und Lateinamerika. In den 1950er Jahren war Malaria in weiten Teilen Europas und in weiten Teilen Mittel- und Südamerikas durch Versprühen von DDT und Trockenlegung von Sümpfen ausgerottet .
Walddegradation kann sie fördern; „Eine 2006 in Peru durchgeführte Studie ergab, dass die Stichrate von Mücken, die Malaria übertragen, in intakten Wäldern 278-mal niedriger ist als anderswo. "
Im Jahr 2006 erlebte Europa eine große Anzahl importierter Malariafälle, hauptsächlich in Frankreich (5.267 Fälle ), dem Vereinigten Königreich (1.758 Fälle ) und Deutschland (566 Fälle). In Frankreich sind 558 Fälle Soldaten, aber die Krankheit betrifft auch Touristen: Von Hunderttausenden von ihnen, die in ein Malariagebiet reisen, kehren dreitausend mit einer der bekannten Formen von Plasmodien infiziert in ihre Länder zurück , der Rest sind Fälle, die von Einwanderer.
- Das Afrika ist ein Kontinent , besonders von Malaria betroffen ist ; es betrifft 95 % der nach Frankreich importierten Fälle . Die Gefahr ist fast Null in Nordafrika , aber Major in Ost Afrika , Afrika südlich der Sahara und äquatorialen Afrika in ländlichen und städtischen Gebieten.
- In Asien kommt Malaria in großen Städten nicht vor und ist in den Küstenebenen eher selten. Die Gefahr ist in den ländlichen Gebieten von Kambodscha , Indonesien , Laos , Malaysia , Philippinen , Thailand , Burma (Myanmar) , Vietnam und in China in Yunnan und Hainan groß .
- Auf den Westindischen Inseln ist Malaria in Haiti und nahe der dominikanischen Grenze weit verbreitet .
- In Mittelamerika gibt es einige Mikrozonen, aber das Risiko ist relativ gering.
- In Südamerika ist das Risiko in Großstädten gering, aber in ländlichen Gebieten in Bolivien , Kolumbien , Ecuador , Peru und Venezuela real und im gesamten Amazonasgebiet groß .
Höhe und Umgebungstemperatur sind wichtige Faktoren dafür, ob in einem Gebiet Malaria entsteht oder nicht.
- Einige Anopheles (wie Anopheles gambiae ) können kaum über 1000 Meter Höhe leben, andere (wie Anopheles funestus ) sind jedoch perfekt angepasst, um bis zu 2000 m zu leben .
- Die Reifung von Plasmodium in Anopheles kann in einem Umgebungstemperaturbereich von 16 bis 35 ° C nicht betrieben werden .
WHO-Kampf gegen Malaria
Dem globalen Ausrottungsprogramm der WHO gingen die Projekte voraus, die nacheinander vom International Health Board, dann von der Rockefeller Foundation ab 1915 , insbesondere aber ab den 1920er Jahren, initiiert und geleitet wurden . Diese beiden Organisationen, Emanationen des philanthropischen Willens von John D. Rockefeller, hatten bereits die Erfahrung von Ausrottungskampagnen von Hakenwürmern und Gelbfieber . Im Bruch mit dem Konsens, der die massive Verabreichung von Chinin in Verbindung mit Maßnahmen zur Kontrolle von Mückenpopulationen - insbesondere durch Entwässerungsarbeiten - befürwortete, gründeten Forscher der Rockefeller Foundation 1924 ihre Strategie auf die alleinige Ausrottung von Mücken. Dazu haben sie das Grün von Paris , eine sehr giftige Substanz, die jedoch bei erwachsenen Mücken unwirksam ist. Italien war ab Ende der 1920er Jahre der erste Einsatzort, gefolgt von allen anderen Einsatzorten der Stiftung im Mittelmeerraum und auf dem Balkan . Trotz gemischter Ergebnisse wurde diese Vorgehensweise in Indien von 1936 bis 1942 eingeschlagen. Der Zweite Weltkrieg, der bestimmte Programme aussetzte, führte auch zu einer Erweiterung: Die Stiftung Gesundheitskommission wurde 1942 gegründet, um die Bemühungen der Streitkräfte zum Schutz ihrer Soldaten an der Front zu unterstützen. Die Entwicklung von DDT , an der die Teams der Stiftung teilnahmen, und die Verbreitung dieses Insektizids aus Flugzeugen im überfluteten Gebiet westlich von Rom ermöglichten ab dem Jahr 1946 den Start von Kampagnen zur Ausrottung der Malaria in Italien . Das berühmteste dieser Programme fand von 1946 bis 1951 auf Sardinien statt . Aufgrund des massiven Einsatzes von DDT führte dieses Programm mit umstrittenen und umstrittenen Umweltmethoden und -folgen zur Ausrottung der Mücken und damit der Krankheit, die jedoch bereits im Niedergang.
In 1952 endete die Rockefeller Foundation ihr Programm für öffentliche Gesundheit und damit anti-Malaria, aber nach der WHO (in geschaffen hatte , 1948 ) ein Programm an der Ausrottung der Mikrobe im Jahr 1955 in der Welt außerhalb Afrika südlich der Sahara und in Madagaskar sollte. Die Vereinigten Staaten, die sich gegen die Einfuhr von Malaria über Südamerika schützen wollten , waren ein wichtiger Akteur; Auch politische Erwägungen - der Kampf gegen den Kommunismus - motivierten ihr Engagement. Nach bemerkenswerten Erfolgen (Spanien war 1964 das erste Land, das von der WHO offiziell als malariafrei erklärt wurde) stieß das Programm schnell auf Schwierigkeiten; 1969 XXII - ten Weltversammlung ratifiziert seine Ausfälle , sondern behält seine weltweite Ausrottung Ziele. 1972 beschloss eine Gruppe von Ländern in Brazzaville, das Ziel der Ausrottung zugunsten eines Kontrollziels aufzugeben. Die 31 th Weltgesundheitsversammlung stimmt diese Änderung im Jahr 1978: es ist nicht mehr dann global für die Beseitigung und Ausrottung von Malaria zu zielen , aber seine Kontrolle. 1992 verabschiedete die Ministerkonferenz von Amsterdam die überarbeitete Globale Strategie zur Bekämpfung der Malaria. Diese von anderen internationalen Gremien überprüfte Strategie wurde 2001 von der WHO festgelegt.
Die WHO hat in den 1980er Jahren die Zertifizierungsverfahren für die Ausrottung aufgegeben und 2004 wieder aufgenommen.
In 1998 ein RBM gebracht (Roll Back Malaria) Partnerschaft zusammen WHO, Unicef , UNDP und die Weltbank .
Im Jahr 2007 hat die Bill and Melinda Gates Foundation ein globales Ausrottungsprojekt neu gestartet, das von einer Vielzahl von Expertengruppen und wissenschaftlichen Artikeln untersucht wurde und zu Strategieprojekten im Bereich der öffentlichen Gesundheit führte.
Aber im Jahr 2019 bleibt die Plausibilität der globalen Ausrottung umstritten. Im August gab die WHO sogar bekannt, dass die Ausrottung der Malaria nach Ansicht ihrer Experten in naher Zukunft nicht möglich ist und dass eine Fristsetzung die Bemühungen gegen die Krankheit untergraben könnte, wie es der Fall war, als die WHO sich 64 Jahre zuvor das gleiche Ziel gesetzt hatte (Die Nichterfüllung solcher Ziele kann die Geber ermüden und den politischen Willen und das Engagement schwächen, und die Frist kann die Bemühungen heimtückisch dahin lenken, wo es am einfachsten ist, "Zahlen zu machen"). Nach dreijähriger Studienzeit heißt es in einem Bericht der Malaria Eradication Strategic Advisory Group (SAGme) der WHO: „Wir dürfen die Welt nicht auf das Scheitern einer weiteren Malaria-Eradikationsmaßnahme vorbereiten“ und empfiehlt die Entwicklung neuer Instrumente und Ansätze gegen Malaria, unter anderem durch Stärkung by universelle Krankenversicherung. Die Lancet-Kommission zur Ausrottung der Malaria , die 26 Wissenschaftler aus der ganzen Welt vereint, möchte stattdessen eine Frist (2050) setzen, hauptsächlich um den Geist der Herausforderung aufrechtzuerhalten.
Schätzungen zufolge haben die weltweiten Bemühungen zur Bekämpfung und Eliminierung von Malaria zwischen 2000 und 2013 3,3 Millionen Menschenleben gerettet , indem die Sterblichkeitsrate durch die Krankheit um 45 % weltweit und 49 % in Afrika gesenkt wurde. Der Kampf gegen Malaria ist eines der Ziele des UN-Nachhaltigkeitsziels 3 .
Eine am 25. Dezember 2019 veröffentlichte Studie zeigt, dass bestimmte Insektenpopulationen in Afrika Resistenzen gegen die in Moskitonetzen weit verbreiteten Insektizide entwickelt haben. Sie zeigten, dass die Überexpression eines Proteins namens SPA2 in Mückenpfoten ihnen eine Resistenz gegen Pyrethroide enthaltende Insektizide verleiht. SPA2-Proteine binden an Pyrethroide und verhindern die Ausbreitung der giftigen Verbindung in ihrem Körper. Das SPA2-Protein "Sensory Appendage Protein" gehört zur Familie der chemosensorischen Proteine "CSP". Die Entdeckung der Wirkung dieses Proteins ebnet den Weg für die Entwicklung eines Insektizids der zweiten Generation, das SPA2-spezifische Inhibitoren enthält. Damit kann der Kampf gegen die Ausbreitung der Krankheit fortgesetzt werden.
Sozioökonomische Auswirkungen
Malaria wird häufig mit Armut in Verbindung gebracht , ist aber auch eine der Hauptursachen für Armut und ein großes Hindernis für die wirtschaftliche und menschliche Entwicklung . Die Krankheit hat in Gebieten, in denen sie verbreitet ist, negative wirtschaftliche Auswirkungen. Ein Vergleich des kaufkraftbereinigten Pro-Kopf- BIP 1995 zwischen den von Malaria betroffenen und den nicht betroffenen Ländern ergab Unterschiede von 1 bis 5 (1.526 USD gegenüber 8.268 USD). Darüber hinaus wuchs das BIP in Ländern, in denen Malaria endemisch ist, von 1965 bis 1990 um durchschnittlich 0,4% pro Jahr, gegenüber 2,4% in anderen Ländern. Dieser Zusammenhang zeigt jedoch nicht, dass die Kausalität und Prävalenz der Malaria in diesen Ländern zum Teil auch auf die verringerten wirtschaftlichen Kapazitäten zur Bekämpfung der Krankheit zurückzuführen ist.
Die wirtschaftlichen Kosten der Malaria werden allein für Afrika auf 12 Milliarden US-Dollar pro Jahr geschätzt. Ein beispielhafter Fall ist Sambia . Wenn das Budget, das das Land 1985 für die Bekämpfung dieser Krankheit aufwendete, 25.000 US-Dollar betrug, sind es seit 2008 dank internationaler Hilfe und des PATH ( Programm für angemessene Technologie im Gesundheitswesen ) 33 Millionen, verteilt auf einen Zeitraum von neun Jahren mit das primäre Ziel, der gesamten Bevölkerung Moskitonetze zur Verfügung zu stellen .
Auf individueller Ebene umfassen die wirtschaftlichen Auswirkungen die Kosten für Pflege und Krankenhausaufenthalt, verlorene Arbeitstage, verlorene Schulbesuche, verminderte Produktivität durch krankheitsbedingte Hirnschäden; für staaten werden diese auswirkungen durch rückgänge bei investitionen und tourismus verstärkt. In einigen Ländern, die besonders von Malaria betroffen sind, kann die Krankheit für 40 % der öffentlichen Gesundheitsausgaben, 30 bis 50 % der Krankenhauseinweisungen und bis zu 50 % der Konsultationen verantwortlich sein.
Ursachen
Malaria wird durch Parasiten der Gattung Plasmodium verursacht , die ihrerseits durch Stechmücken der Gattung Anopheles übertragen werden .
Plasmodium , der für Malaria verantwortliche Parasit
Malaria wird durch einen protozoischen Parasiten der Gattung Plasmodium ( Phylum apicomplexa ) verursacht. Beim Menschen wird Malaria hauptsächlich durch P. falciparum (vorwiegend in den Tropen), P. malariae , P. ovale (die seltenste Art außer Westafrika) und P. vivax (Art mit der geringsten Temperaturanforderung) verursacht.
P. falciparum ist die häufigste Infektionsursache und für etwa 80 % aller Malariafälle sowie 90 % der Todesfälle verantwortlich. Das Plasmodium infiziert auch Vögel, Reptilien, Affen, Schimpansen und Nagetiere (Warmblüter). Infektionen des Menschen wurden mit berichtete APE Arten von Malaria, einschließlich P. knowlesi , P. Inui (en) , P. cynomolgi , P. simiovale , P. brazilianum , P. schwetzi und P. simium . Mit Ausnahme von P. knowlesi bleiben diese Infektionen jedoch begrenzt und für die öffentliche Gesundheit unwichtig. Vogelmalaria kann Hühner und Puten töten, aber die Krankheit verursacht keinen nennenswerten wirtschaftlichen Schaden für die Landwirtschaft. Seit der Einschleppung durch den Menschen hat Malaria jedoch die endemische Vogelart Hawaiis dezimiert , die sich in ihrer Abwesenheit wehrlos entwickelt hatte.
Das Plasmodium ist in Form eines sehr kleinen Einzellers (1 bis 2 Mikrometer je nach Form). Die Färbung mit May-Grünwald-Giemsa , zeigt , dass sie aus einem bestehen Zytoplasma eine hellblauer umgebende Vakuole klar Ernährungs- und einen roten Kern und goldbraunes oder schwarzes Pigment (mit haemozoin ).
Der Evolutionszyklus von Plasmodium ist recht komplex und erfordert zwei Wirte, einen Zwischenwirt: den Menschen und einen Endwirt: das hämatophage Weibchen einer Mücke der Gattung Anopheles (von griechisch anôphelês Bedeutung: nutzlos). Aus streng biologischer Sicht ist der wahre Endwirt die Mücke (die sexuelle Fortpflanzung, die die Anopheles parasitiert ). Der Mensch wäre nur ein Zwischenwirt in seinem Replikationszyklus. Aus anthropozentrischen Gründen wird jedoch angenommen , dass der Vektor nicht der Mensch, sondern die Mücke ist und dass diese Zoonose daher vom Typ der Zooanthroponose ist .
Anopheles, Überträger der Malaria
Lang anhaltende Wechselwirkungen zwischen Anopheles und PlasmodiumNur die Weibchen von Anopheles sind blutsaugend . Männchen, deren einzige Aktivität in der Fortpflanzung der Art besteht und die hin und her fliegen, um sich von Pflanzensaft und Nektar zu ernähren, übertragen die Krankheit nicht.
Anopheles-Weibchen ernähren sich vorzugsweise nachts und beginnen in der Abenddämmerung, ihre Mahlzeit zu suchen, und fahren nachts fort, bis sie sie gefunden haben.
Durch Atmen und Schwitzen emittieren Mensch und Tier CO 2 , und ihr Körper gibt ständig Wärme und Feuchtigkeit ( Schweiß ) sowie einen Cocktail aus potenziell attraktiven Substanzen (wie Milchsäure ) im Körper ab: Atem, Schweiß oder Talg . Weibliche Mücken (sowie andere stechende Insekten) können einige dieser Körperdämpfe aus großer Entfernung (zB ± 20 m für CO 2 ) wahrnehmen und werden sofort von diesen Quellen angezogen. Mücken könnten häufiger nach der Einnahme von Alkohol oder durch dunkle Farben und insbesondere Schwarz (das auch Wärme sammelt) angelockt werden. Sie bewegen sich (maximal 2 km) mit ihren Sensoren ( Chemorezeptoren ).
Es wurde lange angenommen, dass manche Menschen Mücken mehr „anziehen“ als andere, und Forscher haben 2011 weiter bestätigt, dass männliche und weibliche Anopheles nicht auf die gleichen chemischen und geruchlichen Reize reagieren .
Aus ökologischer und evolutionärer oder öko-epidemiologischer Sicht hätte dieser Parasit ein Interesse daran, weibliche Anopheles für an Malaria erkrankte Menschen (oder Tiere) anzuziehen, um sich besser auszubreiten. Inzwischen ist bekannt, dass viele Parasiten das Verhalten ihres Wirts bis zu einem gewissen Grad manipulieren können, insbesondere bei Arten, die für die menschliche öffentliche Gesundheit von Bedeutung sind . Mehrere neuere Studien haben gezeigt, dass Parasiten während der Prozesse der Parasiten-Wirt- Koevolution die Fähigkeit erworben haben, den Geruch ihres Wirts zu ihrem Vorteil zu verändern, indem sie Vektoren anziehen . In den Jahren 2004 und 2005 wurde bestätigt, dass Menschen mit Malaria mehr Mücken anziehen als nicht kranke Kinder (ein Kind mit Malaria zieht doppelt so viele beißende Anopheles an wie ein nicht krankes Kind). Dies wurde 2013 auch bei Tieren (Vögeln) nachgewiesen, jedoch war nicht bekannt, mit welchem Verfahren.
Im Jahr 2014 zeigte eine Studie, dass mit einem Plasmodium ( in diesem Fall Plasmodium chabaudii ) infizierte Labormäuse einen Körpergeruch haben , der sich sehr stark verändert (solange die Maus infektiös bleibt) und der mehr Anopheles anzieht als der von Nicht-Mäusen. infiziert.
Im Jahr 2015 lieferte eine weitere Studie eine wahrscheinliche Erklärung für dieses Phänomen: Im Labor können die Parasiten ( Plasmodium falciparum ) in den von ihnen infizierten Zellen dank ihres Apicoplasten ( Organelle vererbt - von . ) einen attraktiven Terpengeruch für weibliche Anopheles synthetisieren Endosymbiose - ein pflanzlicher Organismus, Alge oder Zwischenorgan zwischen Algen und Bakterien ( Cyanobakterien ..) Diese organellnahen Chloroplasten verloren ihre Photosynthesekapazität, sind aber in der Lage, Terpene zu metabolisieren,
dies zeigt Audrey R. Odom, Washington University School of Medicine in St. Louis hatte mit ihren Kollegen (einschließlich der Yale University) in einer von der Zeitschrift MBIO veröffentlichten Studie an Apicomplexa gearbeitet und die Fähigkeit zur Biosynthese von Isoprenoid durch Apicoplasten nachgewiesen . Eine frühere Studie hatte keine Produktion von Terpenen nachgewiesen, aber es war basierend auf dir geringe Menge an Plasmodien. Das Team von St. Louis hatte die Idee, diesmal eine größere Menge an Plasmodien zu kultivieren, vergleichbar mit der, die in einem infizierten Organismus vorhanden ist. Die Kultur wurde in Chargen infizierter menschlicher roter Blutkörperchen durchgeführt, deren Gasemissionen dann mit denen identischer, aber nicht infizierter Chargen sowie mit dem Gas verglichen wurden, das in den gleichen, aber leeren Plastiktüten gefunden wurde (Kontrollen). Laut den Ergebnissen dieser 2015 veröffentlichten Studie enthielten nur die Beutel mit infizierten Blutzellen Terpene. Die Autoren haben gezeigt, dass P. falciparum dazu (wie einige Pflanzen) einen biochemischen Weg mobilisiert, der als „ plastidialer Isoprenoid-Biosyntheseweg “ bekannt ist, um zwei Terpene zu synthetisieren ( Limonen und Pinandiol , die jeweils einen Zitronenduft und einen an Kiefer erinnern .). ) und zwei weitere Moleküle (deren mögliche Rolle nicht identifiziert wurde). Jede gasförmige Probe aus einer Kultur von Blutzellen, die den Parasiten tragende Blutzellen enthielt, enthielt mindestens eines dieser beiden Terpene. Wir wussten bereits (nachgewiesen im Jahr 2012), dass diese beiden Terpene (die von Blüten produziert werden, die den attraktivsten Nektar für männliche Anopheles produzieren) männliche Anopheles anlocken (sogar bei sehr geringen Dosen).
Zusätzliche Tests haben bestätigt, dass weibliche Anopheles, die Malaria übertragen ( Anopheles gambiae ), diese Terpene gut erkennen können und darauf reagieren, da sie die "zelluläre Maschinerie enthalten, die notwendig ist, um diese Verbindungen zu erkennen und darauf zu reagieren. » , Laut Odom (obwohl auch andere Moleküle dafür bekannt sind, sie anzuziehen; CO 2wurde daher als wichtiger Anziehungsfaktor präsentiert, aber es wurde (2014) gezeigt, dass Stämme von Anopheles gambiae des CO 2 -Rezeptors beraubt sind, Hitze und Milchsäure bleiben perfekt in der Lage, einen menschlichen Wirt zu finden, der sich von seinem Blut ernährt, was zeigt, dass andere Moleküle von der Mücke "verfolgt" werden und sie bei der Wahl des Wirts leiten, wo sie eine Blutmahlzeit einnehmen soll.
Dies deutet darauf hin, dass mit Malaria infizierte Menschen (oder Tiere) eher von einer Mücke gebissen werden und sogar mehr als einmal gebissen werden, was zur Ausbreitung der Epidemie beiträgt, aber als Ergebnis dieser In-vitro-Demonstration In vivo an Mensch oder Tier muss noch gezeigt werden, dass diese Terpene effektiv über die Haut oder den Atem freigesetzt werden und dass sie in dieser Form oder in modifizierter Form tatsächlich Anopheles anlocken, was das Labor von St. Louis schnell tun will.
Diese Informationen ebnen den Weg für neue nicht-invasive Diagnosetests für Malaria, die beispielsweise auf der Analyse von Hautgeruch , Atem (wie ein Alkoholtester ) oder Schweiß basieren . Auch neue Wege zur Bekämpfung der Ausbreitung des Parasiten eröffnen sich: Durch die Manipulation des von der Mücke wahrgenommenen Geruchs könnte es möglich sein, die Anziehungskraft von Anopheles auf Malariapatienten zu begrenzen oder im Gegenteil Köder zu erzeugen Sie beißen.
| Name der Zoonose | Ursache | Übertragung | Vektor |
|---|---|---|---|
| Chikungunya | Virus | Tag Nacht |
weiblich Aedes weiblich Anopheles funestus |
| Dengue | Virus | Der Tag | weibliche Aedes |
| japanische Enzephalitis | Virus | Die Nacht | Culex weiblich |
| Gelbfieber | Virus | Der Tag | weibliche Aedes |
| Lymphatische Filariose | Parasit | Die Nacht | weibliche Anopheles |
| O'nyong-nyong | Virus | Die Nacht | weibliche Anopheles |
| Malaria | Parasit | Die Nacht | weibliche Anopheles |
Parasitärer Zyklus
Bei Anopheles
Der Vektor des Parasiten sowie seine primären Host ist die weibliche ein Moskito der Gattung Anopheles . Junge Mücken nehmen den Parasiten zum ersten Mal auf, wenn sie sich vom Blut eines infizierten Menschen ernähren (das dieses Weibchen für die Eiproduktion benötigt). Nach der Einnahme differenzieren sich die Gametozyten von Plasmodium in männliche und weibliche Gameten und vereinigen sich zu einer Zygote namens Ookinete, die die Magenwand der Mücke durchdringt, um eine kugelförmige Oozyste zu werden. Der Kern wird mehrfach geteilt, um Sporozoiten zu bilden . Die Dauer dieser Reifung hängt stark von der Außentemperatur ab. Zum Beispiel P. falciparum : keine Reifung unter 18 °C oder über 35 °C , maximal bei 24 °C . Wenn die Oozyste reißt, setzt sie die Sporozoiten frei, die durch den Körper der Mücke zu den Speicheldrüsen wandern, wo sie während einer neuen Blutmahlzeit einen neuen menschlichen Wirt infizieren können, indem sie mit dem Speichel die Haut passieren .
Menschlicher Parasitenzyklus
LeberphaseDünne 12 µm / 1 µm Spindel , der infektiöse Sporozoit , der dem Menschen während dieses Bisses einer infizierten weiblichen Anophelesin injiziert wird , zirkuliert schnell (weniger als eine halbe Stunde) im Blut zur Leber, in der er hauptsächlich dank der Klebemuster sequestriert wird das Hauptproteins von seiner Hülle, dem Circumsporozoit - Protein oder CSP = Circumsporozoit - Protein , um dann Infect Hepatozyten . Diese hepatische präerythrozytäre Krise, die bei P. falciparum 7 bis 15 Tage , bei P. vivax 15 Tage bis 9 Monate , bei P. ovale 15 Tage bis X Monate und bei P. malariae 3 Wochen andauern wird, ermöglicht die Parasit, um seinen Zyklus fortzusetzen. Sporozoiten, die die Leber nicht erreichen, werden entweder von Fresszellen eliminiert oder können ihre Entwicklung nicht fortsetzen, wenn sie andere Organe erreichen .
Eine erste Transformation rundet diese "Kryptozoiten"-Form (aus dem Griechischen κρυπτός (kruptos) für "versteckt") in ein einkerniges Element (mit einem einzigen Kern) namens Trophozoit ab, das die Möglichkeit für den Parasiten bietet, sich direkt zu vermehren (das ist es immer. also .) für P. falciparum ), durch Schizogonie , während einer Woche bis 15 Tagen, was zu einem enormen Schizonten (Name wird dem Protozoen gegeben, wenn es nach der Inkubationsphase aktiv wird) von 40 bis 80 μm führt . Dieser blaue Körper (da er bei Färbung mit May-Grünwald-Giemsa aus einem blassblauen Zytoplasma besteht ) knospen , während er seine Beweglichkeit verliert, um Bläschen zu emittieren , die die jungen Merozoiten enthalten, die in das Blut überführt werden und so die Erythrozyten initiieren Stadium, dh Infektion der roten Blutkörperchen.
Einige Merozoiten von P. ovale oder P. vivax können jedoch mehrere Jahre oder bei P. malariae sogar lebenslang in der Leber verborgen bleiben , bevor sie in aufeinanderfolgenden Wellen reaktiviert werden. Dies sind sekundäre exo-erythrozytären Zyklen , die die Parasitosen in der Leber für zwei oder drei Jahre aufrechterhalten wird P. ovale , 3 bis 5 Jahre oder mehr für P. vivax und während des gesamten Lebens für P. malariae . Diese Phase des Parasiten wird als „Ruhephase“ bezeichnet. Diese latenten intrahepatischen Parasiten werden „Hypnozoiten“ genannt (aus dem Griechischen Ὕπνος was Hypnos, der altgriechische Gott des Schlafes) ist.
TransferphaseDie Vesikel werden in den hepatischen Sinusoiden ( Kapillargefäße der Leber, die die Verbindung zwischen ihr und dem Blutnetzwerk herstellen) freigesetzt, um sich dann dem Blutkreislauf anzuschließen und eine Flut junger „präerythrozytärer“ Merozoiten zu verbreiten, die bereit sind, die roten Blutkörperchen zu infizieren . . Jede infizierte Leberzelle enthält ungefähr 100.000 Merozoiten (jeder Schizont kann 20.000 Merozoiten produzieren). Es handelt sich um eine echte „ Trojanische Pferde “-Technik, die hier verwendet wird, um von den Leberzellen ins Blut zu gelangen . In-vivo- Bildgebung zeigte 2005 - 2006 bei Nagetieren, dass Merozoiten in der Lage waren, tote Zellen zu produzieren, die es ihnen ermöglichten, die Leber für die Blutzirkulation zu verlassen und so dem Immunsystem zu entkommen ). Sie scheinen dieses "Vehikel" zu leiten und sich darin zu verstecken, indem sie die biochemischen Signale maskieren, die normalerweise Makrophagen alarmieren . Möglicherweise gibt es einen neuen Weg für aktive Medikamente oder einen Impfstoff gegen das Exo-Erythrozyten- Stadium vor dem Stadium der Invasion der roten Blutkörperchen.
BlutphaseZu Beginn der langen Blutphase: Merozoiten kleben an roten Blutkörperchen , dringen in diese ein, entwickeln sich zu Trophozoiten und teilen sich dann (Schizonten).
Im Jahr 2011 entdeckte ein internationales Team, dass unter den Oberflächenrezeptoren der roten Blutkörperchen, die das Eindringen des Parasiten ermöglichen, einer für diese Penetration unerlässlich ist (bestätigt mit allen auf P. falciparum getesteten Stämmen ); dieser Rezeptor wird daher zu einem Ziel für die zukünftige Impfstoffforschung.
Durch Diffusion verursachen Merozoiten das Platzen der roten Blutkörperchen (dies ist Hämolyse ).
Das Platzen von reifen Schizonten oder "Rosetten" beendet den ersten schizogonischen Erythrozytenzyklus, indem eine neue Generation von Plasmodien ins Blut freigesetzt wird, die "Erythrozyten" -Merozoiten , die andere rote Blutkörperchen wieder infizieren können.
Es folgt eine regelmäßige Abfolge ähnlicher Zyklen, die nach und nach (die Immunabwehr wird organisiert) durch gamogonische Erythrozytenzyklen ersetzt werden, die die Geschlechtsformen vorbereiten. Die Trophozoiten hören auf, sich zu teilen und ändern ihr nukleoplasmatisches Verhältnis. Diese Formen von Trophozoiten mit einem großen Kern und einem verdichteten Zytoplasma sind männliche und weibliche Gametozyten , die im Blutkreislauf verbleiben.
Parasiten haben in dieser Phase beim Menschen keine Überlebenschance: Sie bleiben etwa zwanzig Tage am Leben und verschwinden dann. Sie werden ihre Evolution nur in der Mücke fortsetzen können. Wenn eine weibliche Anophelesin zu diesem Zeitpunkt eine kranke Person beißt, nimmt sie Gametozyten aus dem Blut auf, und ein neuer, diesmal sexueller Zyklus beginnt in der Mücke. Die bei dieser Vermehrung produzierten Sporozoiten gelangen in den Speichel der Mücke, der einen neuen Wirt infizieren kann, und so weiter ...
Pathophysiologie
Klinische Manifestationen
Die von der Mücke geimpften Hämatozoen lokalisieren und vermehren sich zuerst in der Leber. Diese Phase definiert eine minimale Inkubationszeit ohne Symptome.
Die klinischen Manifestationen der Malaria treten zu Beginn der Blutphase auf , wenn die Parasitämie einen individuell unterschiedlichen Schwellenwert überschreitet. Diese asexuelle Vermehrung von Plasmodien in roten Blutkörperchen macht Malaria buchstäblich zu einer parasitären Erkrankung der roten Blutkörperchen.
Die Lyse parasitierter roter Blutkörperchen (Aufplatzen von reifen Schizonten oder Rosetten) setzt neue Parasiten ( Merozoiten ) frei, die wiederum andere rote Blutkörperchen kontaminieren. Diese Zerstörung führt auch zur Freisetzung von Abfallstoffen aus dem plasmodialen Stoffwechsel (Pigmente und Zelltrümmer der roten Blutkörperchen oder Hämozoin ), diese pyrogenen Substanzen stören die Funktion des Hypothalamus (Produktion von Zytokinen wie TNFα ) und verursachen hohes Fieber .
Die ersten Zyklen sind zuerst asynchron (primäre Malaria, mit kontinuierlichem oder anarchischem Fieber), dann werden sie in Abhängigkeit von der Plasmodium- Art in einem periodischen Rhythmus synchronisiert . Die Zeit, die zwischen dem Eindringen eines Parasiten in ein rotes Blutkörperchen und dessen Platzen vergeht, ist ziemlich konstant und erreicht beim Menschen 48 Stunden für P. vivax , P. ovale und P. falciparum (drittes Fieber), 72 Stunden für P. Malaria (Viertelfieber); und für P. knowlesi , die letzte beim Menschen bestätigte Spezies, nur 24 Stunden.
Bei starkem Parasitismus ist die Zerstörung der roten Blutkörperchen so, dass hämolytische Anämie und Gelbsucht auftreten . Der Körper reagiert mit Hyperplasie (erhöhte Produktion) von Makrophagen , was die Vergrößerung der Leber ( Hepatomegalie ) und Milz ( Splenomegalie ) erklärt.
P. falciparum unterscheidet sich von anderen Plasmodium- Arten dadurch, dass es die Fähigkeit besitzt, seine Blutphase auf der Ebene der viszeralen Kapillaren , insbesondere des Hirngewebes , durchzuführen . Es kann dann "Rosetten" (Ansammlungen gesunder und parasitierter roter Blutkörperchen) bilden, Formationen, die an den Wänden der Kapillaren haften. Diese Situation kann von sekundärer Hypoxie , Stoffwechsel- und Elektrolytstörungen , Gefäß- (Wände kleiner Gefäße) und Gewebeschäden begleitet sein.
Unbehandelte, P. falciparum Malaria stellt ein unmittelbares lebensbedrohenden Risiko (Risiko von Mehrfachorganversagen Syndrom , zum Beispiel), die verschiedene Malaria wahrscheinlich chronischen Formen (historische Formen) , um die Fortschritte, mit fortschreitender Verschlechterung des Zustands allgemeines , das dazu führen können zur Kachexie .
Immunität
Nach mehreren Jahren wiederholter Infektionen kann der Plasmodium- Wirt eine Immunität erlangen, die als Prämunition bezeichnet wird (abgeschwächte Symptome einer Krankheit, die vor einer nachfolgenden Infektion des schweren Typs schützt). Es gibt große Unterschiede in den Reaktionen auf Malariainfektionen zwischen Individuen, die in denselben endemischen Gebieten leben . In Gebieten mit hoher Übertragung trägt ein großer Teil der Kinder häufig P. falciparum- Parasiten, ohne Symptome zu melden; es ist klinische Immunität. Mit zunehmendem Alter und den aufeinanderfolgenden Kontakten zwischen Mensch und Parasiten setzt diese Prämunition allmählich ein, die Mechanismen der Infektionsresistenz aufruft, unter denen die Proteine „ Interferon “ , die unter anderem von der Leber metabolisiert und ausgeschieden werden , eine wichtige Rolle bei der Bekämpfung von Parasiten spielen Immunität. Wir werden dann von Toleranz gegenüber Infektionen oder Immunität gegen Parasiten sprechen. Eine Hypothese ist, dass Plasmodium Eisen zum Wachsen braucht; der Eisenmangel durch eine Erstinfektion würde einen relativen Schutz bieten und eine "Superinfektion" verhindern.
Es wird oft behauptet, dass diese Immunität nicht sterilisierend ist, da nie formal nachgewiesen wurde, dass die Parasiten von P. falciparum ohne Behandlung vollständig verschwunden sind . Es wird auch gesagt, dass diese Immunität labil ist, da die Prämunition bei fehlendem häufigem Kontakt zwischen Mensch und Parasit (sie verschwindet nach 12 bis 24 Monaten, wenn die Person das Endemiegebiet verlässt) sowie bei Frauen verschwindet.
Darüber hinaus ist die gegen P. falciparum gerichtete Immunität hochspezifisch für den (die) vorhandenen parasitären Stamm (s).
Diese Besonderheiten der Immunantwort gegen Malaria sind der Ursprung der Schwierigkeiten bei der Entwicklung eines Impfstoffs .
Genetische Faktoren
Genetische Faktoren können vor Malaria schützen (siehe: heterozygoter Nutzen ). Die meisten von denen, die beschrieben wurden, sind mit roten Blutkörperchen verbunden. Hier ein paar Beispiele:
- Die Sichelzellenanämie (griechisch Drepanos , "Sichel" unter der länglichen Form, die eine Reihe von roten Blutkörperchen hat -oder rote Blutkörperchen) auch Hämoglobin S genannt Sichel- oder Sichelzellenanämie: eine Veränderung der ß-Kette des Hämoglobins verursacht rotes Blutzellen zu verformen , wodurch Heterozygoten gebildet werden, die besser vor Malaria schützen. Die roten Blutkörperchen werden deformiert und das Hämoglobin kristallisiert, wodurch der Parasit daran gehindert wird, in die roten Blutkörperchen einzudringen. Diese Veränderung führt jedoch zu einer schlechten Sauerstoffversorgung der Organe (die verlängerten roten Blutkörperchen können nicht in die feinen Kapillaren oder die Barriere des Milzfilters gelangen, wo sie zerstört werden) und damit zu schweren Komplikationen bis hin zum Tod - homozygote Personen (HbS/HbS). Die Prävalenz der Sichelzellanämie (HbA / HbS) ist in afrikanischen Bevölkerungen, die unter hohem Malariadruck leiden, aufgrund der Resistenz gegen schwere Krankheitsschübe hoch.
- Die Thalassämie oder erbliche Anämie: das Subjekt trägt das SS - Gen in einer Änderung der Rate der Synthese resultierenden Ketten mit daraus folgenden schlechter Blutzirkulation und einer konstanten Ermüdungs Globin.
- Der genetische Mangel an G6PD (Glucose-6-Phosphat-Dehydrogenase), auch Favismus genannt , ein antioxidatives Enzym, das normalerweise vor den Auswirkungen von oxidativem Stress auf rote Blutkörperchen schützt , bietet einen erhöhten Schutz vor schwerer Malaria.
- Der HLA-B53 ist mit einem geringen Risiko für schwere Malaria in Verbindung gebracht. Dieses in der Leber vorhandene MHC-Molekül (Major Histocompatibility Complex) der Klasse I ist ein Antigen von T-Lymphozyten (weil sie sich im Thymus befinden ) gegen das Sporozoitenstadium. Dieses Antigen, das von IL4 (Interleukin-4) kodiert wird und von T-Zellen (Thymus) produziert wird, fördert die Proliferation und Differenzierung der B-Zell-Antikörperproduktion.Eine Studie der Fulani von Burkina Faso , die weniger als zwei Malaria-Anfälle mit höheren Konzentrationen von Anti-Malaria-Antikörper als benachbarte ethnische Gruppen, fanden heraus, dass das IL4-524-T- Allel mit hohen Spiegeln von Anti-Malaria-Antikörpern verbunden war , was die Möglichkeit erhöht, dass es ein Faktor für die Erhöhung der Malariaresistenz sein könnte.
- Im natürlichen Kampf gegen P. vivax in Afrika hat der Selektionsprozess einen Membranrezeptor der Erythrozyten , das Glykoprotein DARC (Duffy Antigen Receptor for Chemokine), aus dem genetischen Erbe entfernt , es ist das Eintrittsziel von P. vivax. Somit können Personen, die für die Duffy-Blutgruppe , abgekürzt FY (-), negativ sind, nicht mit P. vivax kontaminiert werden . Dies erklärt das Fehlen von P. vivax in der westafrikanischen Bevölkerung ausschließlich oder überwiegend der „Duffy-negativen“ Blutgruppe. Diese natürliche Immunität könnte jedoch in Frage gestellt werden, da es P. vivax gelungen war , sich bei Duffy-negativen Probanden nach einer genetischen Vermischung zwischen afrikanischen und asiatischen Populationen an Madagaskar anzupassen . Dies würde die Existenz von sekundären Zielen des Parasiten zeigen, die noch bestimmt werden müssen.
Es gibt noch andere genetische Faktoren, von denen einige an der Kontrolle der Immunantwort beteiligt sind.
Klinisch
Malaria äußert sich in Fieberanfällen oder „Malariaanfällen“. Klassisch ist es üblich, den erstmaligen Anfall einer primären Invasion bei einem "naiven" Patienten zu beschreiben (der keine Immunität mehr gegen Malaria hat oder dem Parasiten noch nie begegnet ist) und wiederkehrende Malaria-Anfälle, die bei bereits infizierten Personen auftreten Plasmodium .
In der modernen Praxis wird zwischen einfachen Anfällen und schweren Formen unterschieden. Einfache Anfälle werden wahrscheinlich zu schweren Formen (insbesondere solche mit P. falciparum ), nicht diagnostiziert oder unbehandelt, sie können sich auch zu chronischen Formen entwickeln. Auch der Verdacht auf einen Malaria-Anfall gilt als diagnostischer und therapeutischer Notfall.
Einfacher Malaria-Zugang
Die Inkubationszeit beträgt je nach Plasmodium-Typ mindestens 7 Tage bis 3 Monate.
Primäre Invasion MalariaDie primäre Invasion durch Plasmodium außer Falciparum kann wenig oder wenig symptomatisch sein und unbemerkt bleiben. Ansonsten ist der erste Malaria-Anfall allen Plasmodien- Formen gemeinsam . Sie tritt bei nicht-immunen Patienten auf: Erwachsene, die ihre Immunität verloren haben, während sie sich in einem Endemiegebiet aufgehalten haben, oder Reisende, die in einem Endemiegebiet ankommen, oder ein Kind, das zum ersten Mal in einem Endemiegebiet geboren und betroffen ist.
Fieber ist in 90% der Fälle das Hauptsymptom, es steigt allmählich auf über 40 °C an. Es wird von einem begleitet grippeähnliche Syndrom ( Kopfschmerzen , Muskel- oder Gelenkschmerzen) und Verdauungsstörungen ( Übelkeit , Erbrechen , Durchfall , usw. ). Bei Kindern können Verdauungsbeschwerden dominant sein (Tabelle der fieberhaften Gastroenteritis usw. ).
Dieses Fieber ist kontinuierlich oder anarchisch (keine Periodizität), da die Erythrozytenzyklen noch nicht synchronisiert sind (asynchrone Zyklen).
Wiederkehrender ZugriffDie „Malaria-Krise“ ist durch intermittierende Fieberschübe gekennzeichnet. Klassisch hat jeder Zugriff 3 Phasen:
- Kaltphase: Intensiver Schüttelfrost und Zittern durch extremes Kältegefühl, wenn die Temperatur ansteigt, dauert etwa eine Stunde.
- Hitzephase: Fieber im Plateau bei 40-41 ° C, Dauer 3 bis 4 Stunden.
- Starke Schwitzphase: mit plötzlichem Fieberabfall in 2 bis 4 Stunden.
Diese Attacken wiederholen sich regelmäßig, abhängig von den Erythrozytenzyklen. Klassisch wird zwischen Tertiärfieber (d. h. alle zwei Tage) durch Plasmodium vivax und Plasmodium ovale (gutartiges Tertiärfieber) und Plasmodium falciparum (bösartiges Tertiärfieber) durch Viertelfieber (d. h. alle 3 Tage auftretend) aufgrund zu Plasmodium malariae (der Begriff "Malaria" bezieht sich speziell auf Viertelfieber).
Bei fehlender oder unzureichender Behandlung können diese Malariaanfälle bei P. ovale , P. vivax und insbesondere bei P. malariae über Monate oder sogar Jahre wiederholt werden , es sei denn, sie werden richtig behandelt und es kommt zu keiner erneuten Infektion (Fälle von importierte Malaria im Allgemeinen).
Bei P. falciparum ist der Verlauf kürzer, aber mit hohem Risiko für tödliche Formen.
| |||||||||||||||||||||||||||||||||||
| * Inkubationszeiten können bei unzureichender Malariaprophylaxe von mehreren Wochen auf mehrere Monate verlängert werden |
P. ovale und P. vivax stehen sich sehr nahe und wurden lange Zeit verwechselt.
In etwa 3 bis 4% der Fälle kommt es zu Mischinfektionen mit zwei Plasmodien- Arten . Beispielsweise führt eine Koinfektion mit P. ovale und P. vivax zu einer Überlagerung von Zyklen von zwei Parasitenpopulationen, die sich durch tägliche Malaria- oder Malaria tertiana- Anfälle manifestieren . Es wurde auch zweistufiges Fieber genannt .
Daher gibt es viele Varianten mit historischen Namen wie: Halbdrittelfieber (abwechselnd schwache und intensive tägliche Anfälle), Doppelviertelfieber (Zugang an zwei aufeinanderfolgenden Tagen getrennt durch einen Tag ohne). Fieber Pseudo-Malaria sind intermittierende Fieber , die andere Ursachen als Malaria haben.
Zugang zu schwerer Malaria
Schwere Malaria wird überwiegend durch P. falciparum verursacht und tritt normalerweise 6 bis 14 Tage nach der Infektion auf. Es kann sofort oder nach unangemessener oder verspäteter Behandlung auftreten.
Im XXI ten Jahrhundert wird durch klinische Kriterien und biologische Internationale definiert (WHO) oder nationale, regelmäßig überprüft. In Frankreich 2017 sind die Hauptkriterien für schwere Malaria-Importe bei Erwachsenen:
- Neurologisches Versagen (von Trübung bis Koma).
- Klinischer Ikterus oder erhöhte Bilirubinämie .
- Hyperparasitämie größer als 4%.
- Nierenversagen ( Kreatinin oder erhöhte Urämie ).
Andere Kriterien, die weniger häufig sind, aber auf Schwere hindeuten, sind Atem- und Herzkreislaufversagen sowie biologische Zustände wie Azidose und Hyperlaktatämie .
Unbehandelt kann schwere Malaria schnell fortschreiten und innerhalb von Tagen oder sogar Stunden zu Koma und Tod führen , insbesondere bei Kleinkindern und besonders gefährdeten Schwangeren. Daher das Interesse einer Notfalldiagnose unverzüglich in Behandlung. In den schwersten Fällen kann die Sterblichkeitsrate sogar bei korrekter Behandlung ohne allzu große Verzögerung 20 % überschreiten.
Schwerwiegende Formen von P. vivax sind vor allem in Südostasien zu beobachten , die Hauptkomplikationen sind dann die Atemwege. P.-knowlesi- Malaria präsentiert sich am häufigsten als einfacher Befall, kann sich jedoch zu einer ernsthaften Form entwickeln (jedoch ohne Hirnschäden).
Ein Milzinfarkt oder eine Milzruptur kann bei jeder Plasmodium- Art beobachtet werden , häufiger bei P. falciparum und P. vivax .
NeuropalariaEs handelt sich um einen schweren Malaria-Anfall, der von neurologischen Manifestationen dominiert wird, wobei zerebrale Malaria mit der Schädigung der Kapillaren des Gehirns in Verbindung gebracht wird. Es ist die zerebrale Malaria der Angelsachsen und historisch bei den Frankophonen der verderbliche Zugang .
Gegen Ende des XX - ten Jahrhunderts, die WHO - Experten haben das Konzept der schweren Malaria Zugang zu anderen Veranstaltungen andere als neurologische, pragmatischen Gründen verbreitert (auch schlechte Prognose, auch von derselben Notfallbehandlung). Auch im XXI ten Jahrhundert, die Bedingungen für den Zugang oder schwerer (Französisch) oder schwerer Malaria (Englisch) sind häufiger als zerebrale Malaria oder verwendet zerebrale Malaria, restriktiver.
Der schädliche Zugang erfolgt allmählich oder plötzlich. Es verbindet Fieber und Bewusstseinsstörungen. Anfälle sind vor allem bei Kindern lokalisiert oder auf den ganzen Körper verallgemeinert, bei anderen Erwachsenen nur in 50 % der Fälle. Dies ist auf eine schlechte Leberfunktion und übermäßigen Zuckerkonsum durch den Parasiten zurückzuführen. Schwangere sind besonders anfällig für Hypoglykämie und eine Überproduktion von Milchsäure, die zu einem erhöhten Säuregehalt des Blutes führt.
Die anderen neurologischen Zeichen sind zeitlich und örtlich variabel. Sie können von Anämie, Leberversagen und funktionellem und vorübergehendem Nierenversagen oder schwererem akutem Nierenversagen begleitet sein .
Ein Lungenödem ist eine seltene, aber schwerwiegende Komplikation mit sehr schlechter Prognose. Es ist schlecht erklärt, mit einer Sterblichkeitsrate von über 80%.
Gallenartiges hämoglobinurisches FieberDies ist eine historische Komplikation, vor allem zwischen 1910 beobachtet und 1940 und wurde in der späten selten XX - ten Jahrhundert. Es war ein Syndrom, das bei europäischen Auswanderern in einer tropischen Endemiezone auftritt, mit einer Vorgeschichte von Zugang zu Plasmodium falciparum und unregelmäßiger Einnahme von Chinin .
Es ist immunallergischen Ursprungs, verbunden mit dem Medikament, mit massiver intravaskulärer Hämolyse (Platzen der roten Blutkörperchen in den Gefäßen).
Der Beginn ist plötzlich und tritt innerhalb von Stunden nach Einnahme des Arzneimittels mit Fieber und Kreuzschmerzen , Gelbsucht und Blutdruckabfall auf . Hämolytische Anämie verursacht Hämoglobinurie (Hämoglobin im Urin, was ihm eine dunkle Farbe verleiht, Schwarzwasserfieber für die Engländer oder portroter Urin für die Franzosen). Die Progression kann zu akutem Nierenversagen durch Zerstörung der Nierentubuli (akute Tubulusnekrose) führen.
Es gibt wenig oder keine Parasitämie, was dieses Syndrom von einem verderblichen Angriff unterscheidet.
Dieses hämoglobinurische Gallenfieber ist praktisch verschwunden, nachdem Chinin durch synthetische Antimalariamittel wie 4- Aminochinoline (wie Chloroquin ) ersetzt wurde. Es wurden jedoch Fälle mit Chinin-ähnlichen Arzneimitteln wie Halofantrin oder Mefloquin berichtet . Diese drei Medikamente sind bei empfindlichen Personen formal kontraindiziert.
Diagnose
Klinische Diagnose
IndustrieländerJedes Fieber rechtfertigt eine Suche nach der Reisegeschichte; und bei der Rückkehr aus einem Malaria-Endemiegebiet gilt jedes Fieber oder Fieber in der Vorgeschichte bis zum Beweis der Schuld, da das Risiko einer schnellen Progression zu einer schweren Form besteht. In Frankreich betrifft dies vor allem Migranten, die aus Subsahara-Afrika zurückkehren, auch im Falle einer Chemoprophylaxe (oft schlecht eingenommen) oder einer Behandlung vor Ort.
Die klassischen Fallen, die die Diagnose von Malaria verzögern, sind fieberhafte Gastroenteritis , insbesondere bei Kindern; eine grippeähnliche Erkrankung im Winter; das Fehlen von Fieber (unangemessene symptomatische Behandlung); ein Bild einer Harnwegsinfektion ; eine Reihe von Dengue-Fieber .
Der Verdacht auf Malaria setzt im Notfall eine Labordiagnostik zur Bestätigung voraus.
EntwicklungsländerVielerorts ist selbst eine einfache Labordiagnostik nicht möglich und die Befragung eines fiebrigen Patienten wird als Indikation für eine Fortsetzung der Malariabehandlung herangezogen. Diese Methode ist jedoch nicht die effektivste: In Malawi zeigte die Verwendung von mit Giemsa gefärbten Blutausstrichen , dass unnötige Antimalariabehandlungen abnahmen, wenn klinische Indikatoren (Rektumtemperatur, Blässe des Nagelbetts, Splenomegalie) anstelle von Fieber in der Vorgeschichte verwendet wurden (Sensitivität stieg von 21 % auf 41 %).
Malaria bei Kindern wird zu oft falsch diagnostiziert (schlechte Anamnese , Missbrauch von Schnelldiagnosetests) von Pflegekräften an vorderster Front (Mitglieder der Gemeinschaft, die eine Grundausbildung erhalten haben, die es ihnen ermöglicht, auch ohne qualifiziertes medizinisches Personal eine Grundversorgung zu gewährleisten); ebenso wird es schlecht bewertet, was zu einer unangemessenen oder unzureichenden Behandlung führt und somit eine wirksame Behandlung verhindert.
Biologische Diagnose
Die Diagnose der Malaria basiert auf dem Nachweis des Parasiten im Blut. Dies ist eine Notfalldiagnose, die innerhalb von zwei Stunden nach der Blutentnahme gestellt werden muss.
Bluttest unter dem Mikroskop (dicker Abstrich)Die günstigste (zwischen 0,40 und 0,70 US-Dollar pro Objektträger), die zuverlässigste und am weitesten verbreitete Diagnosemethode ist die lichtmikroskopische Untersuchung eines Blutausstrichs und eines dicken Blutstropfens.
Der Abstrich ermöglicht es, die einzigartigen Merkmale jeder der vier Arten des Homo sapiens- Parasiten zu identifizieren, da das Erscheinungsbild des Parasiten mit dieser Probe besser erhalten bleibt. Der dicke Blutstropfen ermöglicht es, ein größeres Blutvolumen zu bereisen, um die Diagnose zu stellen und Plasmodium nicht zu übersehen . Diese Untersuchungen sind von einem qualifizierten und informierten Biologen durchzuführen.
Die erwarteten Informationen sind:
- positive Diagnose von Malaria (Anwesenheit von Plasmodium ).
- Artdiagnose (Vorkommen von P. falciparum oder einer anderen Art) für möglichen Schweregrad.
- die Parasitämie (Prozentsatz der infizierten roten Blutkörperchen oder Anzahl der Parasiten pro ul Blut), die für die Überwachung der Behandlung nützlich sind.
Der negative Vorhersagewert der beiden kombinierten Verfahren (Schmier- und Dickfilm) beträgt nicht 100 %. Eine negative Untersuchung sollte innerhalb von 12 bis 24 Stunden wiederholt werden, wenn der klinische Verdacht bestehen bleibt.
Schnelle DiagnosetestsWenn kein Mikroskop zur Verfügung steht, können Tests zum schnellen Nachweis von Antigenen verwendet werden, die nur einen Blutstropfen erfordern und keine besonderen Kenntnisse erfordern.
Diese immunchromatographischen Tests (auch Malaria-Schnelltests oder RDTs genannt) können in Form eines Teststreifens oder eines „Dipsticks“ vorliegen. Frühe Schnelltests verwendeten P. falciparum- Glutamat-Dehydrogenase (GluDH) als Zielantigen (pGluDH), wurden jedoch durch solche ersetzt, die P. falciparum- Lactat-Dehydrogenase (LDH) (pLDH) und HRP2 (für Histidin-Rich) Protein 2 verwendeten ).
Die Sensitivität der verwendeten Tests (200 auf dem Markt erhältliche Produkte) beträgt mehr als 95 %, wenn die Parasitämie mehr als 100 pro µl Blut beträgt, und 70 % bei den schwächeren Parasitämien und noch weniger bei P. ovale. Ihre Spezifität beträgt 90 bis 95 %.
In entwickelten Ländern werden diese Schnelltests mit dem dicken Abstrich in Verbindung gebracht.
MolekularbiologieDiese Methode basiert auf dem Nachweis von Parasiten- Nukleinsäuren durch Polymerase-Kettenreaktion (PCR), eine empfindlichere und spezifischere Technik als die Mikroskopie. Es ermöglicht den Nachweis sehr schwacher Parasitämien und die genaue Identifizierung der Plasmodien-Spezies (einschließlich der Unterscheidung von P. Knowlesi und P. malariae ).
In den am weitesten fortgeschrittenen Ländern wird die PCR tendenziell zur Referenzmethode für die Regressdiagnose (Situation diagnostischer Schwierigkeiten). Schnellere Analysemethoden wie die Real-Time-PCR mit Ergebnissen in weniger als einer Stunde sind in Referenzlabors verfügbar und können mit der Notfall- oder Routinediagnostik kompatibel sein.
SchwerkraftbewertungDie biologische Standardbeurteilung ermöglicht die Beurteilung eines Schweregrades und hilft bei der Differenzialdiagnose: insbesondere das Blutbild , das C-reaktive Protein , Ionogramm , biologische Anzeichen einer Hämolyse, Leber- oder Nierenleiden. Der Bluttest kann je nach Kontext und Empfehlung zum Screening auf andere Infektionen, insbesondere Virusinfektionen, verwendet werden.
Eine Koinfektion mit Malaria ist immer möglich, aber Tests auf Malaria haben aufgrund der höheren Häufigkeit und des möglichen unmittelbaren Schweregrades Priorität.
Chronische Formen
Akute und schwerwiegende Komplikationen betreffen im Allgemeinen nur Plasmodium falciparum , entwickeln sich jedoch nicht zu chronischen Formen.
Die subakuten und chronischen Formen der Malaria werden bei Infektionen mit anderen Plasmodien beobachtet: P. vivax , P. ovale und insbesondere P. malariae . Die Krankheit kann mehrere Monate oder Jahre nach der Exposition aufgrund des latenten Vorhandenseins von Parasiten in der Leber erneut auftreten. Daher kann man nicht sagen, dass ein Subjekt von Malaria geheilt wird, indem man einfach das Verschwinden der Parasiten aus dem Blutkreislauf beobachtet. Die längste Inkubationszeit von P. vivax beträgt 30 Jahre. Ungefähr jeder fünfte Fall von P. vivax- Malaria in gemäßigten Gebieten beinhaltet einen Winterschlaf durch Hypnozoiten (Rückfälle beginnen im Jahr nach dem Mückenstich).
Sich entwickelnde viszerale Malaria
Früher Malariakachexie genannt, wird diese Malaria bei Kindern im Alter von 2 bis 5 Jahren in Endemiegebieten, bei Auswanderern in Endemiegebieten mit unzureichender Behandlung und bei Migranten, die nicht mehr in Endemiegebieten leben, beobachtet.
Es geht mit einer fortschreitenden Verschlechterung des Allgemeinzustandes einher, mit einem mäßigen intermittierenden Fieber (manchmal nicht vorhanden), einer chronischen Anämie mit Zytopenie , einer mäßigen Splenomegalie (manchmal wichtig). Die Parasitämie ist sehr schwach, sogar nicht nachweisbar.
Hyperimmune Malaria-Splenomegalie
Diese chronische Malaria, die früher in einer Gruppe namens "tropische Splenomegalie" verwechselt wurde, entspricht einer abnormalen immunologischen Reaktion. Es ist eher selten und wird bei einigen wenigen Individuen gefunden, die in einem Gebiet leben, in dem Malaria endemisch ist.
Es unterscheidet sich von der progressiven viszeralen Malaria durch eine signifikante Splenomegalie und Hepatomegalie , eine Erhöhung einer bestimmten Art von Immunglobulinen im Blut (IgM, Anti-Malaria-Antikörper) und der Anzahl der Lymphozyten in den hepatischen Sinusoiden . Parasitämie ist meistens nicht nachweisbar.
Die Biopsie der Leber und die Untersuchung des Lichtmikroskops ermöglichen die Diagnose. Der sehr langsame Verlauf kann durch Milzruptur , Superinfektion oder das Auftreten eines malignen lymphoproliferativen Syndroms ungünstig sein .
Quartannephritis
Es ist eine schwere Nierenkomplikation durch eine chronische Infektion mit Plasmodium malariae (verantwortlich für Viertelfieber, daher der Name). Es tritt am häufigsten bei Kindern in Endemiegebieten nach mehreren Jahren der Entwicklung auf.
Das Bild ist das eines nephrotischen Syndroms durch Ablagerung von Immunkomplexen (Antikörper-Antigen-Assoziationen) in den Nierenglomeruli .
Die Nierenbiopsie kann die Läsion identifizieren. Diese Untersuchung zeigt Ablagerungen von Komplement (Elemente, die am Immunsystem beteiligt sind) und Immunglobulinen (eine Vielzahl von Proteinen, die die Rolle von Antikörpern spielen). Das Labor weist Antigene von Plasmodium malariae bei Kindern nach .
Die Entwicklung kann trotz der Behandlung (Antimalariamittel und Kortikosteroide ) mehr oder weniger schnell in Richtung eines chronischen Nierenversagens erfolgen .
Formen je nach Gelände
Schwangere Frau
Bei einer Schwangerschaft mit Plazentainfektion durch Plasmodium besteht ein höheres Komplikationsrisiko. In Endemiegebieten führt eine Schwangerschaft zu einer Abnahme der Antimalariaimmunität, während Plazentaläsionen zu einer Abnahme des fetalen-mütterlichen Kreislaufs führen.
Bei der Mutter sind Malariaanfälle häufiger und schwerwiegender (Risiko eines Aborts oder einer Frühgeburt ), bei Kindern: Perinatalsterblichkeit , Anämie, niedriges Geburtsgewicht.
Im Jahr 2018 waren in Afrika südlich der Sahara fast 11 Millionen schwangere Frauen (in mäßig bis stark endemischen Gebieten) mit 872.000 Säuglingen mit niedrigem Geburtsgewicht gefährdet. Westafrika ist die Region mit der höchsten Prävalenz von niedrigem Geburtsgewicht, die mit Malaria während der Schwangerschaft in Verbindung gebracht wird.
Häufigkeit und Schwere von Infektionen in Endemiegebieten hängen vom Grad der Malariaübertragung ab. In instabilen Niedrigendemiegebieten wie Indien oder der Südostasien-Pazifik-Region ist das Risiko schwerer Formen bei Schwangeren dreimal so hoch wie bei Nichtschwangeren. In diesen Regionen sind mehr als 23% der Müttersterblichkeit auf Malaria zurückzuführen.
In Regionen mit einer hohen stabilen Endemie wie Subsahara-Afrika treten die schwersten Formen während der ersten Schwangerschaft oder der ersten Geburt auf ( Erstgebärende ), während Frauen, die bereits mindestens eine Schwangerschaft hatten, selbst bei einem hohen Parasitenanteil weniger Probleme haben Belastung. Dieses Phänomen könnte durch den Erwerb einer spezifischen Plazentaimmunität durch selektive Anreicherung von P. falciparum in der Plazenta erklärt werden.
Die transplazentare Passage von Plasmodium von der Mutter zum Fötus ist relativ häufig, manifestiert sich jedoch selten als "Krankheit", nämlich angeborene Malaria , die zwischen den ersten Tagen und dem ersten Monat nach der Geburt auftritt. Ihre genaue Inzidenz ist umstritten: Sie wäre in hyperendemischen Gebieten sehr selten (weniger als 3 pro Tausend Geburten bei infizierten Müttern), aber anderswo häufiger.
Kinder
Im EndemiegebietKinder unter 5 Jahren sind die am stärksten von Malaria betroffene Gruppe. Im Jahr 2018 schätzte die WHO die Zahl der mit P. falciparum infizierten Kinder in Afrika südlich der Sahara auf 24 Millionen , darunter 1,8 Millionen mit schwerer Anämie, und die Zahl der Todesfälle auf 272.000 oder 67% der Sterblichkeitsrate weltweit.
Klinisch treten bei Kindern einfache Malariaanfälle in Form von Verdauungs- und Atemwegserkrankungen auf, deren Schwere von der Art des Plasmodiums und dem genetischen, Ernährungs- und Immunstatus des Kindes abhängt .
Die schweren Formen, verbunden mit P. falciparum mit mehr als 4% Parasitämie, können zerebrale Malaria, Atemnot , schwere Anämie, Hypoglykämie und sekundäre bakterielle Infektionen kombinieren ; und seltener Nierenversagen im Vergleich zu Erwachsenen.
Die zerebrale Malaria im Kindesalter äußert sich am häufigsten durch Krämpfe, eine abnorme Haltung in Streckung ( Opisthotonos ), die durch eine intrakranielle Hypertonie kompliziert werden kann, die zu einem Koma mit malariaspezifischer Retinopathie fortschreitet , was es ermöglicht, Malariakoma von anderen Koma zu unterscheiden.
Die meisten Kinder kommen innerhalb von 48 Stunden ohne Folgen aus dem Koma, aber 20 % sterben daran und 10 % haben neurologische Folgen oder kognitive Verzögerungen .
IndustrieländerEs ist eine importierte Malaria. In Frankreich, dem am stärksten betroffenen europäischen Land, machen Kinder 15 % der insgesamt gemeldeten Fälle aus, das sind fast tausend Kinder pro Jahr, von denen 10 % Säuglinge sind. Über 80% dieser Fälle im Kindesalter sind auf P. falciparum zurückzuführen .
Bei den betroffenen Säuglingen handelt es sich meist um Migranten der zweiten Generation, die im Urlaub in das Herkunftsland ihrer Eltern, hauptsächlich in Subsahara-Afrika, zurückgekehrt sind. Malaria bei Säuglingen ist schwerer als bei Kindern. In den Jahren 2000-2009 deutet das Fehlen der Kindersterblichkeit in Frankreich wahrscheinlich in den allermeisten Fällen auf eine angemessene Versorgung hin.
Im Jahr 2014 wurden in den Vereinigten Staaten 1.513 Fälle von importierter Malaria gemeldet, darunter 55 Fälle importierter Malaria bei Kindern unter 5 Jahren (1 Fall von angeborener Malaria) und 241 Fälle bei unter 18 Jahren. 85% der Fälle im Kindesalter kehrten von einer Reise nach Afrika zurück.
Transfusionsmalaria
Die Plasmodien , die mehrere Tage gegen eine Temperatur von 4 °C resistent sind, können durch Bluttransfusion von gelagertem Blut und erst recht von frischem Blut übertragen werden.
Klinisch ähnelt die Transfusionsmalaria der primären Invasionsmalaria, aber eine längere Inkubationszeit für alle Arten von Plasmodium, P. falciparum und P. malariae ist am häufigsten damit verbunden (jeweils 45 bzw. 30 % bei nicht endemischen).
WeltIn Endemiegebieten ist Transfusionsmalaria häufig, aber aufgrund der Semiimmunität der Empfänger, denen manchmal zusätzlich eine Malariabehandlung angeboten wird, gutartig.
Die höchste Prävalenz von Malaria unter Blutspendern wird in Afrika beobachtet. Mit molekularen Techniken: In Afrika wären es rund 36 %, in Asien 4 %, in Amerika 2 % und in Europa 1 %.
Die Malaria-Hämovigilanz-Kriterien werden von der WHO vorgeschlagen und von jedem Land gemäß den nationalen Empfehlungen angepasst. Einige Länder, wie die Vereinigten Staaten, verwenden einen Fragebogen, um potenziell infizierte Blutspender zu ermitteln. Andere, wie Frankreich, Großbritannien oder Australien, verwenden auf der Grundlage dieses Fragebogens zusätzliche serologische Tests.
In den 1970er Jahren traten in nicht-endemischen Ländern zwei bemerkenswerte "Transfusions-Epidemien" von Malaria in nicht-endemischen Ländern auf, in den Vereinigten Staaten durch erfahrene Spender aus Vietnam und 1971 in Spanien: 54 Fälle von Transfusions-Malaria durch P. vivax , verbunden mit einer einzigen Blutbank in Barcelona .
FrankreichAuf dem französischen Festland (Transfusionszentren Marseille und Nizza ) kam es in den Jahren 1960-1970 zu einer Zunahme solcher Übertragungen, die mit einer unzureichenden Untersuchung der Blutspender verbunden waren. Zu Beginn des XXI ten Jahrhundert wird dieses Risiko als gering betrachtet, durch Rückstellung des Spenders nach einem kürzlichen Aufenthalt in Endemiegebieten gewarnt (innerhalb von weniger als 6 Monaten, nach europäischen Standards) und biologischen Tests (Serologie Malaria).
Insbesondere in Frankreich 2019 gelten als gefährdete Spendenkandidaten: 1) Menschen mit Malaria in der Vorgeschichte, 2) Menschen mit nicht diagnostiziertem Fieber, das innerhalb von 4 Monaten nach einer Rückkehr aus einem Malariagebiet auf einen Malaria-Anfall hindeutet. 3) Personen, die sich in einer Risikoregion aufgehalten haben und 4) Personen, die in einer Risikoregion heimisch sind oder länger als 6 aufeinanderfolgende Monate in einer Risikoregion gelebt haben. Gefährdete Spender werden vorübergehend zur Blutspende verschoben; die Abschottungsfrist beträgt je nach den Umständen 4 Monate oder 3 Jahre.
Die am stärksten gefährdeten Blutprodukte sind Erythrozytenkonzentrate, während Plasma, das keine roten Blutkörperchen enthält, als risikoarm gilt. Ein Restrisiko stellen asymptomatische Spender dar, die als Immunsilencing (Fehlen von Antikörpern bei bestimmten chronischen Parasitenträgern) bezeichnet werden. In Frankreich beträgt die Wahrscheinlichkeit einer Posttransfusionsmalaria 2019 0,2 bis 0,5 Fälle pro Million Transfusionen, verglichen mit 1 Ende der 1990er Jahre. Zwischen 2000 und 2019 wurden 4 Fälle von Posttransfusionsmalaria gemeldet auf Blutspenden einer Person aus einem Endemiegebiet. In drei dieser Fälle handelte es sich um P. falciparum und die infizierten Empfänger starben.
Impfung Malaria
Es kann sich um eine Malaria durch versehentlichen Blutkontakt , bei einer Injektion beim Pflegepersonal oder um den Austausch kontaminierter Spritzen zwischen Drogenabhängigen handeln.
Die Impfung kann freiwillig oder "kontrolliert" sein. Historisch gesehen , die Inokulation von P. vivax oder P. malariae wurde als therapeutisches Mittel gegen die verwendeten Neurolues im ersten Drittel des XX - ten Jahrhundert.
Am Ende des XX - ten Jahrhunderts, die Impfung von P. falciparum ist in den USA in Freiwilligen während Impfung Studien oder Untersuchungen der Stämme , die gegen Antimalariamittel verwendet.
Im Jahr 2018 ist die Impfung von Plasmodium, bekannt als kontrollierte menschliche Malariainfektion, bei Freiwilligen ein Mittel zur experimentellen Erforschung neuer Medikamente oder Impfstoffe gegen Malaria.
Behandlungen
In Endemiegebieten ist die Behandlung oft unbefriedigend und die Gesamtsterblichkeitsrate aller Malariafälle kann einen von zehn erreichen. Der massive Einsatz veralteter Therapien, gefälschte Medikamente und die schlechte Anamnese sind für das schlechte klinische Ergebnis verantwortlich.
Alte Behandlungen
Der Endoparasit kann mit verschiedenen Molekülen entweder in kurativen Behandlungen oder in der Prophylaxe bekämpft werden . Diese unterschiedlichen Therapien sind je nach Region und erworbener Resistenzrate mehr oder weniger wirksam, denn wie DDT (das in den 1960er Jahren am weitesten verbreitete Insektizid) sind Medikamente, die vor dreißig Jahren noch wirksam waren, wie Chloroquin , heute nicht mehr wirksam .
Diese veralteten Formulierungen sind jedoch in den betroffenen Ländern immer noch weit verbreitet. Als Teil der Dritten Welt haben sie nicht die Möglichkeit, ihr Behandlungsprotokoll auf ein teureres Instrument wie die ACT ( Artemisinin-basierte Kombinationstherapie ) zu übertragen. Behandlungen wurden lange Zeit mit Chloroquin, Chinin und SP (Sulfadoxin- Pyrimethamin ) und in geringerem Maße mit Mefloquin , Amodiaquin und Doxycyclin verwendet .
Diese Moleküle waren sehr wirksame Waffen im Kampf gegen Malaria-Parasiten, aber ihre unkontrollierte Verschreibung hat die Entstehung resistenter Stämme begünstigt . Nach Angaben der Weltgesundheitsorganisation (WHO) ist die Behandlung wirksam , wenn die Ausfallrate von weniger als 5% beträgt; wenn er 25 % überschreitet, muss das Protokoll geändert werden.
Dem Chloroquin wird seit langem Priorität eingeräumt. Durch die Nahrungsaufnahme von Hämoglobin spaltet der Parasit es in Aminosäuren auf , wodurch die im Hämoglobin enthaltenen Hämmoleküle freigesetzt werden, die für den Parasiten selbst giftig sind, die er umwandelt und in seiner Verdauungsvakuole als inerte Kristalle speichert. Chloroquin dringt in die infizierte Zelle ein und stoppt die schützende Umwandlung von Häm in inerte Kristalle, wodurch sich dieses giftige Eisen ansammelt. Der Parasit wird somit durch seinen eigenen Abfall abgetötet.
Es war ein Medikament mit vielen Vorteilen, darunter seine geringen Kosten und das Fehlen von Nebenwirkungen. In den von Malaria betroffenen Ländern Afrikas südlich der Sahara versagen heute mehr als 25 % der auf Chloroquin basierenden Behandlung . Sie sind jedoch weiterhin erwerbstätig.
Dieser Widerstand ist aufgrund der Allel - Mutante PfCRT ( Plasmodium falciparum Chloroquin - Resistenz Transporter ) K76T. Diese Mutation entzieht der infizierten Zelle das Chloroquin, würde jedoch zu einer schlechteren Anpassung des Parasiten an seine Umgebung führen. Der Malawi ist das erste afrikanische Land Chloroquin verlassen zu haben, beginnend im Jahr 1993 , zu einem erneuten Auftreten von empfindlichen Stämmen führen dann wieder hoch Mehrheit werden.
Wenn Chloroquin nicht mehr wirkt, wird ein Arzneimittel, das als Arzneimittel der zweiten Wahl bezeichnet wird, angewendet: MS (wie Fansidar ( Sulfadoxin/Pyrimethamin (en) ), hergestellt von Roche ). Dieses Molekül umgeht die Chloroquinresistenz. Nur fünf Jahre reichten für das Auftreten resistenter Stämme. Dann maßgeschneiderte Therapie mit einem "Drug of 3 e Intention": das Chinin , oral verabreicht in leichten Fällen oder Infusion in akuten Fällen. Allerdings sind diese Behandlungen auch mit neuen Resistenzen des Parasiten konfrontiert.
GESETZ
Die Artemisinin-basierte Kombinationstherapie in der französischen Artemisinin-basierten Kombinationstherapie und Abkürzung ACT ist eine Therapie und Tertiärprävention bei unkomplizierter Malaria . Es besteht aus der Verbindung von zwei Molekülen : einem halbsynthetischen Molekül, das von Artemisinin abgeleitet ist, und einem synthetischen Molekül, dessen Aufgabe es ist, die Wirkung des ersten Moleküls zu verstärken, aber auch das Auftreten von Resistenzen zu verzögern und somit Malaria besser zu behandeln.
Seit dem erfolgreichen Abschluss der klinischen Phase-III-Studien der ersten jemals entwickelten ACT im Jahr 2001 ist es die einzige von der Weltgesundheitsorganisation empfohlene medizinische Behandlung zur Bekämpfung dieser Krankheit.
In relativ kleinen Mengen hergestellt, sind ACT-Medikamente teurer als Chloroquin . Eine Behandlung mit Chloroquin oder mit MS kostet derzeit zwischen 0,2 und 0,5 USD pro , Während eine ACT - Behandlung ist zwischen 1,2 und 2,4 USD / , Oder fünf- bis sechsmal mehr. Für viele Patienten ist dieser Unterschied der Preis für ihr Überleben. Ein Preis, den nur sehr wenige Menschen in Afrika zahlen können. Nur eine Produktion in größerem Maßstab oder eine größere finanzielle Unterstützung durch reiche Länder könnten die Produktionskosten signifikant senken.
Forschungspfade
Neue Wege werden beschritten, darunter:
- Ein Weg mit Peptiden und neuen chemischen Verbindungen.
Die Spiroindolone bilden eine neue Klasse von Antimalariamitteln, die getestet werden.
Das Cipargamin gehört zu dieser Klasse mit heilender Wirkung, indem es oral versprochen wird. - eine Behandlung, die einen oder mehrere neue Wirkmechanismen kombiniert, die durch das Testen einer Sammlung synthetischer Verbindungen mit dreidimensionalen Eigenschaften entdeckt werden könnten, die denen natürlicher Malariamittel ähnlich sind und noch nicht ausreichend getestet wurden.
Solche Verbindungen umfassen beispielsweise bizyklische Azetidine, die (oral) in niedrigen Dosen gegen alle Lebensstadien des Parasiten wirksam zu sein scheinen, in mehreren in vivo getesteten Modellen, und die ein Potenzial zur Heilung und/oder Vorbeugung von Krankheiten zeigen, und Bevölkerungen gefährdet schützen.
Gefälschte Drogen
Von gefälschten Medikamenten, die angeblich Malariamittel in Thailand, Vietnam, Kambodscha und China zirkulieren; sie bilden eine wichtige Todesursache, die dennoch vermeidbar wäre. Im August 2007 musste das chinesische Pharmaunternehmen Holley-Cotec zwanzigtausend Dosen seines Artemisinin-Medikaments Duo - Cotecxin in Kenia wegen Fälschungen mit Ursprung in Asien, die nur sehr wenige Wirkstoffe enthielten und zu keiner Therapie in der Lage waren, zurückziehen zu einem fünfmal niedrigeren Preis vermarkten. Ohne die Hilfe eines Labors gibt es für Ärzte und Patienten keine einfache Möglichkeit, ein echtes Medikament von einer Fälschung zu unterscheiden. Pharmaunternehmen versuchen, gefälschte Medikamente zu bekämpfen, indem sie neue Technologien einsetzen, um das Produkt von der Quelle bis zum Vertrieb zu sichern.
Verhütung
Zu den Methoden, die verwendet werden, um die Ausbreitung der Krankheit zu verhindern oder um Menschen in Endemiegebieten zu schützen, gehören die Prophylaxe durch Medikamente, die Ausrottung von Mücken und die Vorbeugung von Mückenstichen. Damit Malaria dauerhaft an einem Ort existieren kann, ist eine Kombination von Faktoren erforderlich: eine hohe Bevölkerungsdichte, eine hohe Übertragungsrate vom Menschen auf die Mücken und umgekehrt. Wenn einer dieser Faktoren abnimmt, verschwindet der Parasit schließlich, wie in Nordamerika und Europa. Umgekehrt kann der Parasit wieder in ein Gebiet eingeschleppt werden und dort überleben, wenn diese Faktoren dort vorhanden sind.
Gegen Malaria gibt es derzeit keinen Impfstoff , aber die Suche nach einem Impfstoff ist ein sehr aktiver Bereich.
Einige Forscher behaupten, dass die Vorbeugung von Malaria kostengünstiger wäre als die langfristige Behandlung. aber die dafür aufzubringenden Kosten sind für die Ärmsten zu hoch. Der Ökonom Jeffrey Sachs schätzt, dass Malaria mit drei Milliarden US-Dollar pro Jahr bekämpft werden könnte. Um die Millenniums-Entwicklungsziele zu erreichen , sollten die derzeit für die AIDS- Bekämpfung bereitgestellten Gelder in die Malariaprävention umgeschichtet werden, was der afrikanischen Wirtschaft weiter zugute kommen würde.
Einigen Ländern wie Brasilien, Eritrea, Indien oder Vietnam ist es gelungen, die Geißel Malaria einzudämmen. Die Analyse dieser Programme zeigt, dass viele Faktoren zusammenkommen mussten, um die Krankheit erfolgreich zu bekämpfen, sei es die Finanzierung, Maßnahmen der Regierung und von NGOs oder konkrete Maßnahmen.
Möglichkeiten zur Bekämpfung oder zum Schutz vor Mücken
Der Malariaüberträger (weibliche Anopheles) kann mit mehreren Präventionsmaßnahmen bekämpft werden, die bei richtiger Umsetzung wirksam sein können.
Das eigentliche Problem bei dieser Prävention sind die sehr hohen Behandlungskosten für die betroffenen Bevölkerungsgruppen. In der Tat kann es bei Reisenden wirksam sein, aber die Entwicklungsländer, die die Hauptopfer dieser Krankheit sind, haben Mühe, sehr wirksame Maßnahmen zu organisieren. Als Beweis können wir das Beispiel der Insel La Réunion anführen, auf der Malaria weit verbreitet war, wie insbesondere auf den anderen Inseln der Region ( Madagaskar und Mauritius ). Da Réunion ein französisches Überseegebiet ist, bestand das Problem der zu hohen Kosten nicht und die Malaria konnte von dieser Insel problemlos ausgerottet werden.
In den betreffenden Ländern werden zwei Präventionsmethoden angewendet. Sie zielen zum einen darauf ab, die Bevölkerung vor Mückenstichen zu schützen und zum anderen durch den Einsatz verschiedener Mittel zu eliminieren. Das Hauptziel dieser Prophylaxe ist die Bevölkerung zu begrenzen Mückenvektoren der Krankheit und damit zu versuchen , diese Geißel zu beseitigen.
In den 1960er Jahren war die Hauptmethode zur Ausrottung weiblicher Anopheles der starke Einsatz von Insektiziden . Am häufigsten wurde DDT (Dichlor-Diphenyl-Trichlorethan) verwendet. Diese Methode trug in vielen Gebieten Früchte, in denen die Malaria vollständig ausgerottet wurde. Der intensive Einsatz von DDT hat jedoch die Selektion resistenter Mücken begünstigt. Dieser Widerstand wurde KDR ( Knock Down Resistance ) genannt. Darüber hinaus kann es in der Bevölkerung zu Vergiftungen und Krankheiten führen, wie es in Indien der Fall war, wo es in der Landwirtschaft missbraucht wurde. Obwohl dieses Produkt in Europa seit 1972 vollständig verboten ist und seit 1992 von der WHO als POP (persistent organic pollutant) eingestuft wird, scheint diese Organisation dennoch ihre Position umzukehren, indem sie neue Empfehlungen zur Verwendung von dieses Pestizid (ausschließliche Verwendung zur Bekämpfung von Malaria in Gebäuden). Die vier WHO-Kriterien sind:
- Toxizität : DDT wird vorgeworfen, potenziell krebserregend zu sein und die Nerven- und Hormonfunktion des Menschen zu verändern (Wirkung auf den Östrogenstoffwechsel bei Frauen, antiandrogene Wirkung).
- persistent : seine Halbwertszeit beträgt 15 Jahre, d.h. wenn wir 10 kg auf ein Feld sprühen , bleiben 15 Jahre später 5 kg übrig , nach 30 Jahren 2,5 kg und so weiter;
- dispersiv : Es wurde im Schnee der Arktis gefunden ;
- kumulative Bio : Tiere, die es aufnehmen, sterben nicht daran, sondern eliminieren es nicht. Sie speichern es in ihrem Fett und finden es in hohen Konzentrationen bei Tieren an der Spitze der Nahrungskette. Andererseits ist seine Toxizität umstritten, obwohl eine Einnahme von 35 g für eine Person von 70 kg tödlich sein kann (wie zum Beispiel bei Ibuprofen und im Vergleich zu 225 g für Salz oder 120 g für Kaffee).
Die Toxizität von DDT ist jedoch nicht nachgewiesen.
Um DDT zu ersetzen, sind alternative Mittel zur Bekämpfung des Malariavektors möglich:
- Entwässerung der Sümpfe (ohne das ökologische System zu stören), Entwässerung von stehendem Wasser, wo sich die Larven von Anopheles entwickeln (ein alter Reifen, der vom Regen verlassen und mit Wasser gefüllt wurde, reicht aus, damit die Mücke dort ihre Eier ablegt);
- Larvenbekämpfung durch Ausbringen von Petroleum oder Pflanzenöl und die Verwendung von löslichen Insektiziden, die auf der Oberfläche von stehendem Wasser verteilt werden, um zu versuchen, die Geburten von Anopheles zu begrenzen oder zu verhindern, dass die Larven an der Oberfläche atmen. Sehr unerwünschte Maßnahmen, da sie völlig unökologisch sind;
- Ansäen von Gewässern mit Fressfeinden von Anopheles oder deren Larven wie bestimmte Weichtiere oder Fische ( Tilapien , Guppys , Gambusies , Aphanius );
- Wiederansiedlung und Schutz von insektenfressenden Fledermausarten , wo sie verschwunden sind (eine Fledermaus kann über Nacht fast die Hälfte ihres Gewichts an Insekten verschlucken);
- gezielt aus der Genomsequenzierung von Moskitos . Dieses Genom bietet unter anderem einen Katalog der Zunahme von Entgiftungsgenen und mutierten Genen, die die von Insektiziden angegriffenen Proteine kodieren, sowie die Variationen einzelner Nukleotide , sogenannte Nukleotidpolymorphismen, die im Genom vorkommen:
- Verwendung von Insektenschutzmitteln und Insektiziden, die nur gegen Anopheles gerichtet sind,
- Verbreitung steriler Anopheles-Männchen in freier Wildbahn,
- genetische Eingriffe an Vektorarten oder in unbestimmter Zukunft mit Impfstoffen, die die Übertragung blockieren, indem sie Antikörper induzieren, die die Reifung der sexuellen Stadien des Parasiten bei Anopheles verhindern.
- Orales Antiparasitenmittel. Ivermectin erhöht die Sterblichkeit von Mücken beim Stich für mindestens 28 Tage.
Diese Maßnahmen sind nur in einem begrenzten Bereich wirksam. Es ist sehr schwierig, sie im Maßstab eines Kontinents wie Afrika anzuwenden.
Jeder kann individuell Anophelin-Bisse durch mechanische, physikalische und chemische Maßnahmen verhindern; Erinnern wir uns vor allem daran, dass die Anopheles eine nächtliche Aktivität haben, bei Einbruch der Dunkelheit zu stechen beginnen und sich tagsüber in Häusern ausruhen:
- Installation von Moskitonetzen (Maschenweite weniger als 1,5 mm ), die mit Permethrin- oder Pyrethroid- Derivaten imprägniert sind . Diese Moskitonetze werden der Bevölkerung in Endemiegebieten zunehmend zu sehr günstigen Preisen (maximal 1,70 USD ) oder sogar kostenlos zur Verfügung gestellt. Diese Netze sind je nach Modell und Einsatzbedingungen 3 bis 5 Jahre wirksam;
- Installation von Siebgewebe an Fenstern;
- Kleininsektizideinsatz: Versprühen von Insektiziden für Innenräume (Pyrethroide, DDT usw. ) in Wohnungen (Schlafzimmern);
- Installation von Klimaanlagen in Wohnungen, um die Temperatur zu senken und die Luft zu rühren (die Mücke verabscheut Luftbewegungen, die sie in ihren Bewegungen und ihrer sensorischen Fähigkeit stören, ihr Ziel zu finden);
- nach Sonnenuntergang: Tragen von lockerer, langer, heller Kleidung und Verzicht auf Alkohol (Anopheles werden von dunklen Farben, insbesondere Schwarz, genauso angezogen wie von Alkoholdämpfen);
- Auftragen einer Abwehrcreme auf die Haut oder Kleidung, sobald die Sonne untergeht. Von allen synthetischen Abwehrmitteln sind diejenigen am wirksamsten , die DEET (N,N-Diethyl-m-toluamid) enthalten. DEET tötet keine Insekten, aber seine Dämpfe halten sie davon ab, auf der Person zu landen oder zu klettern.
Im Allgemeinen sind Produkte mit einer Konzentration von 25 bis 30 % DEET am längsten wirksam (± 8 Stunden gegen kriechende Insekten und 3 bis 5 Stunden gegen Anopheles). Auch für Erwachsene oder Kinder über zwei Jahren gelten sie als unbedenklich, wenn die Konzentration bei letzteren 10 % nicht überschreitet. Bei Schwangeren und Säuglingen unter drei Monaten zu vermeiden. Produkte mit einer Konzentration von mehr als 30 % sind nicht mehr zugelassen.
Die verkauften Produkte sind direkt auf die Haut oder auf Kleidung oder Moskitonetze aufzutragen. Achten Sie jedoch darauf, dass sie Kunststoffe, bestimmte synthetische Stoffe wie Nylon, Gummi, Leder und lackierte oder lackierte Oberflächen verändern. Achten Sie auch auf die Augen und direktes Einatmen mit versprühten Produkten sowie Verschlucken. Daher werden Applikatoren mit einer Kugel bevorzugt.
Die transkutane Resorption beträgt 50 % in sechs Stunden und die Elimination erfolgt über den Urin. Der nicht entfernte Teil (30 %) wird in Haut und Fett gespeichert.
Abwehrmittel
Studien haben gezeigt, dass Eukalyptus- Repellentien , die natürliches Eukalyptolöl enthalten, eine wirksame, ungiftige Alternative zu DEET sind . Außerdem haben sich Pflanzen wie Zitronengras als wirksam gegen Mücken erwiesen. Eine ethnobotanical Studie in der Region durchgeführt Kilimanjaro ( Tansania ) zeigt , dass die am häufigsten verwendeten Repellents, von der lokalen Bevölkerung, sind lamiacées Geschlecht ocimée der Ocimum kilimandscharicum und Ocimum suave . Die Studie über die Verwendung von ätherischen Ölen, die aus diesen Ocimeas gewonnen werden, zeigt, dass der Schutz gegen Bisse bestimmter Anopheles-Vektoren der Malaria in 83 bis 91 % der Fälle zunimmt und beim Insekt in 71,2 bis 92,5 % der Fälle seine Sauglust hemmt .
Andere natürliche Lösungen werden ebenfalls empfohlen. So ist nach einer Studie des Ministeriums Kamerun Public Health durchgeführt, der Akt der Haut reiben Arten von Pflanzen krautigen alle zwei Jahre von der Familie von Amaryllidaceae , wie Zwiebeln und Knoblauch würde die Loch- Rate von 71 auf 79% verringern. Diese Art der vorbeugenden Behandlung wird dringend empfohlen für Menschen, die eine vegetarische Ernährung einhalten und möglicherweise Eisen- und Proteinmangel haben, eine Quelle für das Insekt.
Icaridin, auch bekannt als KBR 3023, ist ein neues Abwehrmittel aus der chemischen Familie der Piperidine und in der Stärke vergleichbar mit DEET, jedoch weniger reizend und löst keine Kunststoffe. Es wurde vom deutschen Chemieunternehmen Bayer AG entwickelt und unter dem Namen SALTIDIN vertrieben. Die Gelform mit 20% Wirkstoff ist derzeit die beste. Seien Sie vorsichtig, trotz allem sind noch nicht alle möglichen Nebenwirkungen gegenüber Kindern bekannt.
Eine von einer unabhängigen Verbraucherorganisation auf den Markt gebrachte Studie mit verschiedenen Repellents ergab, dass synthetische Repellents, darunter DEET, wirksamer waren als Repellents mit natürlichen Wirkstoffen.
- Verwendung von Permethrin ((3-Phenoxyphenyl)methyl) oder Pyrethroid- Derivaten . Sie sind Abwehrmittel, können aber auch zu den Insektiziden zählen. Wenn sie die Mücke abstoßen und reizen, erzeugen sie eine Knockdown-Aktion, die sie direkt tötet oder neutralisiert.
Nicht direkt auf der Haut anwenden, sondern Kleidung oder Moskitonetze imprägnieren, dabei die Nasenschleimhäute nicht reizen oder bei der Handhabung verschlucken. Die Wirkungsdauer beträgt ca. 6 Monate (weniger bei Kleidung, die Reibung, Regen etc. ausgesetzt ist). Die Nachimprägnierung erfolgt nach dem Waschen mit Seife.
Vorsichtsmaßnahme: Keine mit Permethrin imprägnierte Kleidung auf der bereits mit DEET behandelten Haut tragen.
Schwangere Frau
Die zuletzt implementierte Methode ist viel zielgerichteter. In der Tat gilt es nur für schwangere Frauen, und sein Zweck besteht darin, eine Schwangerschaft mit Problemen aufgrund vorzeitiger Wehen zu vermeiden und Babys bei guter Gesundheit und nicht mit einem zu geringen Gewicht (insbesondere wenn es sich um eine Primipara ) oder sogar handelt, auf die Welt zu bringen leidet an vielen Krankheiten wie Plazenta-Malaria (angeborene Infektion oder nicht, hängt direkt mit der Anzahl der Parasiten in der Plazenta zusammen ), schwerer Anämie und Fehlbildungen des Babys.
Um schwerwiegende Komplikationen zu vermeiden und zu verhindern, wurde eine umfassende Betreuung, die die Prävention von Malariainfektionen und den Gesundheitsschutz umfasst, eingeführt. Diese Maßnahmen zielen darauf ab, Infektionen und deren Folgen zu begrenzen, die für das Kind und die Mutter sehr schwerwiegend sein können. Dazu gehören die Verwendung von mit Insektiziden behandelten Moskitonetzen und die Verwendung von Antimalariamitteln, entweder als primäre Prophylaxe oder als intermittierende Behandlung.
Andererseits ist nicht nur nachgewiesen, dass die intermittierende Behandlung von Schwangeren mit der Wirkstoffkombination SP (Sulfadoxin-Pyrimethamin) einmal im zweiten und ein zweites Mal im dritten Trimester das Anämierisiko senkt Mutter, Plazentaparasitämie und niedrigem Geburtsgewicht, sondern auch, dass die systematische Behandlung mit SP bei Säuglingen im Alter von 2, 3 und 9 Monaten während der Impfungen die Episoden klinischer Malaria um 60 % und die Episoden perniziöser Anämie um 50 % reduzierte.
In Endemiegebieten hat sich durch eine wirksame Vorbeugung von Malaria während der Schwangerschaft gezeigt, dass die Inzidenz von Anomalien wie niedrigem Geburtsgewicht oder schwerer mütterlicher Anämie (erniedrigte Hämoglobinkonzentration im Blut - unter 0,13 g/ml bei Männern und 0,12 g/ml bei Frauen) reduziert wird ).
Die Anwendung dieser wenigen Regeln würde ausreichen, um die Zahl der von dieser Krankheit betroffenen Menschen und damit die Zahl der Opfer erheblich zu reduzieren, aber der Mangel an Mitteln behindert ihre Anwendung. Viele Bewohner können sich nicht einmal Moskitonetze leisten, was die Ansteckungsgefahr verringern kann.
[Ref. notwendig]Prophylaxe
Um eine Ansteckung bei Touristen zu verhindern, die in Länder reisen, in denen Malaria weit verbreitet ist, haben Forscher eine prophylaktische Technik eingeführt . Diese Technik besteht aus einem therapeutischen Arsenal präventiver Drogen (begrenzt auf Chloroquin, Proguanil, die Pyrimethamin - Dapson - Kombination, die proguanil- Atovaquon Kombination, die Chloroquin-Proguanil Hydrochlorid Kombination , Mefloquin und Doxycyclin) , um Infektionen zu verhindern , wenn der Parasit in dem Körper gelangt .
Bei kurzen Aufenthalten in Gebieten mit starker Malariaübertragung wird eine regelmäßige präventive Behandlung, insbesondere für Kinder und Schwangere, die ein erhöhtes Risiko für schwere Malaria haben, empfohlen. Aufgrund der zunehmenden Resistenz gegen Parasiten (Resistenz von Parasiten gegen Produkte, die das therapeutische Arsenal bilden) und der produktspezifischen Nebenwirkungen wird es jedoch immer schwieriger, Richtlinien für die Chemoprophylaxe zu erstellen.
Antimalariamittel garantieren keinen absoluten Infektionsschutz und es ist auch wichtig, sich vor Mückenstichen zu schützen (Mückennetze, Mückenschutzmittel), denn auch bei richtiger Behandlung kann eine Malaria auftreten, die manchmal erst spät auftritt zur Hypnozoitenform , die Plasmodium annehmen kann .
In Belgien kommt es jedes Jahr zu Todesfällen aufgrund von Malaria bei zurückkehrenden Reisenden.
Malaria-Prophylaxe-RegimeAb dem 9. März 2006 wurde die Malariaprävention in drei Stufen eingeteilt, die nach Chemoresistenzgrad eingeteilt wurden. Jedes gefährdete Land wird somit in eine Gruppe eingeordnet. Lange vor Reiseantritt ist es ratsam, Ihren Arzt zu konsultieren, da diese Behandlungen in der Regel im Voraus begonnen werden.
Gruppenland 0 Malariafreie Gebiete: Keine Chemoprophylaxe.- Afrika : Lesotho , Libyen , Marokko , Réunion , Île Sainte-Hélène , Seychellen und Tunesien ;
- Amerika : alle Städte , Antigua und Barbuda , Niederländische Antillen , Bahamas , Barbados , Bermuda , Kanada , Chile , Kuba , Dominica , Vereinigte Staaten , Grenada , Kaimaninseln , Inseln Falkland , Jungferninseln , Jamaika , Martinique , Puerto Rico , St. Lucia , Trinidad und Tobago und Uruguay ;
- Asien : alle Städte, Brunei , Georgien , Guam , Hongkong , Weihnachtsinsel , Cookinseln , Japan , Kasachstan , Kirgisistan , Macau , Malediven , Mongolei , Turkmenistan , Singapur und Taiwan ;
- Europa : alle Länder einschließlich Armenien , Azoren , Kanarische Inseln , Zypern , Russland , Baltikum , Ukraine , Weißrussland und Türkei in Europa;
- Naher und Mittlerer Osten : alle Städte, Bahrain , Israel , Jordanien , Kuwait , Libanon und Katar ;
- Ozeanien : alle Städte, Australien , Fidschi , Hawaii , Marianen , Marshallinseln , Föderierte Staaten von Mikronesien , Neukaledonien , Neuseeland , Osterinseln , Französisch-Polynesien , Samoa , Tonga und Tuvalu .
- Afrika : Algerien , Kap Verde , Ägypten , Eritrea und Mauritius ;
- Asien : Aserbaidschan , Nordkorea , Südkorea und Usbekistan ;
- Naher und Mittlerer Osten : Vereinigte Arabische Emirate , Oman , Syrien und Türkei .
Doxycyclin (Wirkstoff)
eine 100-mg-Tablette pro Tag, einen Tag vor der Abreise (zweimal am ersten Tag eingenommen) und bis zu 28 Tage nach der Rückkehr oder nach Verlassen des Malaria-Endemiegebiets (in sitzender Position mit viel Flüssigkeit einzunehmen oder während der Mahlzeit) ). Bei Kindern über acht Jahren sollte die Dosis halbiert werden. Doxycyclin kann mehrere Monate lang eingenommen werden, kann jedoch Phototoxizität (chemische Reaktion, die durch zu viel photoreaktive Substanz in der Haut verursacht wird und unter Einwirkung von UV- oder sichtbaren Strahlen reagiert) und orale und genitale Hefeinfektionen verursachen; es sollte nicht bei schwangeren (Lebererkrankungen) oder stillenden Frauen sowie bei Kindern unter 8 Jahren angewendet werden (reversible Verlangsamung des Knochenwachstums und irreversible Gelbfärbung der Zähne mit erhöhtem Kariesrisiko) Es ist ein Derivat von Tetracyclin (ein Antibiotikum mit vier aufeinanderfolgenden Zyklen, das in der Lage ist, eukaryotische Zellen einschließlich Plasmodium zu durchdringen ), die manchmal gegen Malaria in Kombination mit Chinin zur intravenösen Notfallbehandlung verwendet wird.Das Mefloquin oder Lariam ( Roche )
Zusammensetzung: 250 mg Mefloquin Schachtel mit acht Tabletten - 34,26 EUR (Preis in Belgien im Jahr 2012) Eine Tablette pro Woche, einige Wochen vor Abreise und bis zu vier Wochen nach Rückkehr Um bei der Ankunft eine wirksame Blutkonzentration von Lariam zu erhalten, muss die Behandlung zwei bis drei Wochen vor der Abreise eingeleitet werden. Personen, die dieses Produkt noch nie eingenommen haben, sollten die Behandlung zwei bis drei Wochen vor der Abreise beginnen, um mögliche Nebenwirkungen (Schwindel, Schlaflosigkeit, Albträume, Aufregung, unerklärliche Angstzustände, Herzklopfen) zu überprüfen. Es wird nicht verschrieben, wenn der Arzt eine Kontraindikation feststellt (Schwangerschaftswunsch, erstes Schwangerschaftstrimester, Epilepsie, Depression oder Herzrhythmusstörungen, die mit Medikamenten wie Betablockern, Kalziumkanalblockern oder Digitalis behandelt werden) , oder wenn es in der Vergangenheit nicht geduldet wurde. Die Behandlung sollte bis zu vier Wochen nach der Rückkehr fortgesetzt werden. Bei guter Verträglichkeit kann Lariam bei Bedarf über Monate oder sogar Jahre eingenommen werden. Bei längeren Aufenthalten (Dauer von mehr als drei Monaten) sollte die Chemoprophylaxe so lange wie möglich aufrechterhalten werden und Reisenden wird empfohlen, schnell einen Arzt vor Ort zu kontaktieren, um die Relevanz und den Nutzen/Risiko einer Chemoprophylaxe abzuschätzen.Als Alternative zu Mefloquin kann die Kombination Atovaquon-Proguanil wie Malarone ( GlaxoSmithKline ) empfohlen werden.
Zusammensetzung für Erwachsene: 250 mg Atovaquon + 100 mg Proguanilhydrochlorid Schachtel mit zwölf Tabletten - 44,14 EUR (Preis in Belgien im Jahr 2012) Zusammensetzung für Junior: 62,5 mg Atovaquon + 25 mg Proguanilhydrochlorid Schachtel mit zwölf Tabletten - 18,48 EUR (Preis in Belgien im Jahr 2012) Eine Tablette pro Tag, einen Tag vor der Abreise und bis zu sieben Tage nach der Rückkehr. Beginnt die erste Einnahme erst während des Aufenthalts, sollte sie bis zu vier Wochen nach der Rückkehr eingenommen werden. Für einen Kurztrip ist die Einnahme von Malarone, das meist sehr gut verträglich ist, eine ausgezeichnete Wahl. Es kann mehrere Monate verwendet werden (dann müssen jedoch die hohen Kosten berücksichtigt werden). Die Dauer der kontinuierlichen Anwendung von Atovaquon-Proguanil sollte in dieser Indikation jedoch auf drei Monate begrenzt werden, da bisher keine ausreichende Nachsorge bei längerer Behandlung vorliegt.In jedem Fall ist der Rat eines Arztes vor jeder Medikation mehr als wünschenswert.
In Tansania wurde gerade eine Technologie mit SMS erfolgreich getestet .
Diese Operation, SMS for Life genannt, besteht darin, Lagerbestände mit Medikamenten gegen Malaria, Aids und Tuberkulose an einem bestimmten Ort, auch am entlegensten, durch die Interaktion zwischen einem Computerserver und Mobiltelefonen zu vermeiden .
Aufkommen
Die Forschung sowohl in der Pharmakologie für Behandlungen (siehe ausführlicher Abschnitt „ Zukunft – Pharmakologie “) als auch in der Impfung zur Prophylaxe (siehe ausführlicher Abschnitt „ Impfstoffe “) wird dank Sponsoren wie der Malaria Vaccine Initiative oder NGOs wie MSF . immer schneller .
Vorsichtsmaßnahmen
Die Einnahme von Malaria-Medikamenten reicht auch bei richtiger Behandlung nicht aus, um sich hundertprozentig vor dem Malariarisiko zu schützen. Es ist auch notwendig, sich vor Mücken zu schützen, um zu verhindern, dass sie mit ihren Opfern in Kontakt kommen, um den Stich des Insekts zu vermeiden:
- vermeiden Sie ungeschützte Reisen in Risikogebiete, schlafen Sie immer mit einem Moskitonetz mit einer Maschenweite von weniger als 1,5 mm , auch unter dem Sternenhimmel;
- lange, weite, weiße Kleidung tragen, eng an den Handgelenken und Knöcheln, mit geschlossenen Schuhen, mit Abwehrmittel imprägniert (Vorsicht, die Anopheles-Mücke fliegt oft tief zu Boden und kann Socken durchbeißen);
- Hautabwehrmittel auf alle unbedeckten Körperteile auftragen (basierend auf DEET, aber bei Säuglingen unter 3 Monaten und schwangeren oder stillenden Frauen zu vermeiden);
- Insektizide verwenden, drinnen, aber auch draußen;
- Schlafen Sie mit Klimaanlage oder unter einem Moskitonetz (vorzugsweise mit Insektizid imprägniert, wenn der Körper nachts mit diesem Moskitonetz in Kontakt kommen kann): Der Mensch wirkt somit als Köder und zusätzlich zur mechanischen Barriere des Moskitonetzes, die die Stich verursacht den Tod der Mücke, die mit dem Insektizid in Kontakt gekommen ist;
- Schützen Sie alle Öffnungen mit geeigneten Moskitonetzen.
Die Verwendung von Repellents oder Insektenschutzmitteln (wie DEET oder DDT ) und Moskitonetzen verringert das Infektionsrisiko, aber eine Chemoprophylaxe bleibt unerlässlich ( Nivaquine , Savarine, Lariam, Malarone). Es wird nicht empfohlen, während der Einnahme dieser Medikamente Alkohol zu trinken.
Wirtschaftliche Folgen
Laut der Ligue contre le malaria würde eine betroffene Familie wegen der verlorenen Arbeitstage nur 40% ihrer landwirtschaftlichen Produktion ernten. Die WHO hat sogar berechnet, dass das BIP Afrikas sein derzeitiges Niveau um 115 Milliarden Euro oder zusätzliche 32 % übersteigen würde, wenn die Malaria vor 35 Jahren eliminiert worden wäre.
Im Hinblick auf die Bekämpfung schätzt UNICEF die durchschnittlichen jährlichen Kosten für Malaria-Programme in jedem afrikanischen Land auf rund 345.000 Euro oder bei einem Land mit fünf Millionen Einwohnern auf weniger als sieben Cent Euro pro Kopf.
Die Bevölkerung in Malariagebieten lebt in der überwiegenden Mehrheit in Armut, die neuen Medikamente, die viel wirksamer, aber teurer sind als die alten, übersteigen oft ihre Verhältnisse.
Manchmal kommt es sogar vor, dass ein Patient seine Behandlung nicht vollständig befolgt und sich geheilt fühlt, dass er das, was ihm übrigbleibt, auf dem Schwarzmarkt verkauft, wodurch das Auftreten von Resistenzen gegen die Behandlungen beschleunigt wird (siehe Kapitel über die Resistenz des Parasiten ).
Den Zahlen zufolge gab der Privatsektor im Jahr 1990 pro Opfer 789 Dollar für die Bekämpfung von Asthma aus , 3.274 Dollar für AIDS (das Virus betrifft sowohl Entwicklungs- als auch Industrieländer) und nur 65 Dollar für Malaria. Mit anderen Worten, der Betrag, der für die Impfstoffforschung und die Entwicklung von Antimalariamitteln ausgegeben wird, ist minimal, wenn man bedenkt, dass fast fünfzig Prozent der Weltbevölkerung gefährdet sind.
Darüber hinaus verfügt die überwiegende Mehrheit der von Malaria betroffenen Länder weder über die wirtschaftlichen noch über die technologischen Mittel, um in ihrem Land echte Forschung im medizinischen Bereich zu entwickeln. Länder mit sehr begrenzten finanziellen Mitteln (meist zerbröckelnd unter der Last der Auslandsverschuldung), fehlendem soliden politischen Willen, einem weit unter den Erwartungen liegenden Forschungsbudget und lächerlicher internationaler Hilfe im Vergleich zu den Bedürfnissen der Bevölkerung und der Anzahl der betroffenen Menschen, Erinnerung dass die katastrophalen Folgen dieser Krankheit der Unterentwicklung nicht allein der Natur geschuldet sind, dass der Mensch viel damit zu tun hat.
2001 gründete die WHO jedoch einen Globalen Fonds zur Bekämpfung von Malaria, aber auch von AIDS und Tuberkulose .
Seit 2003 hat auch die Bill and Melinda-Gates Foundation mehrere hundert Millionen Dollar unter anderem an die Malaria Vaccine Initiative gespendet , um die Krankheit zu bekämpfen.
Der 2002 gegründete Global Fund to Fight AIDS, Tuberculosis and Malaria oder Global Fund bündelt internationale Mittel zur Behandlung von Malaria.
Verschieden
- In Frankreich steht diese Krankheit auf der Liste der meldepflichtigen Infektionskrankheiten .
- Malaria wurde oft auf Briefmarken abgebildet. Das erste Beispiel ist eine 1939 herausgegebene mexikanische Wohltätigkeitsmarke , die einen Menschen zeigt, der einer riesigen Mücke zum Opfer gefallen ist. Am spektakulärsten war jedoch die Ausgabe von 1962, als gleichzeitig in hundert Ländern die Kampagne der WHO mit dem Titel Malaria-Eradikation gefeiert wurde . Die WHO hat die Ausrottung der Malaria zu einer ihrer obersten Prioritäten erklärt.
- Der Roman Das Chromosom von Kalkutta von Amitav Ghosh (Hrsg. Seuil 1998, Slg. Cadre vert) räumt in einer fantastischen Atmosphäre der Entdeckung von Ronald Ross bei der Malaria einen großen Raum ein.
- Ein 2013 erschienener angelsächsischer Fernsehfilm Mary and Martha: Two Mothers Courage spricht vom Kampf zweier Mütter gegen Malaria (oder Malaria).
Hinweise und Referenzen
- (fr) Dieser Artikel ist teilweise oder vollständig aus dem Wikipedia - Artikel in genommen englischen Titeln „ Malaria “ ( siehe die Liste der Autoren ) .
- (en) Weltgesundheitsorganisation , Weltmalariabericht 2020 , Genf, Weltgesundheitsorganisation,2020, 300 S. ( ISBN 978-92-4-001580-7 , online lesen )
- Lexikographische und etymologische Definitionen von "Malaria" aus dem computergestützten französischen Sprachschatz , auf der Website des Nationalen Zentrums für textliche und lexikalische Ressourcen
- Lexikographische und etymologische Definitionen von „Malaria“ aus dem computergestützten französischen Sprachschatz , auf der Website des Nationalen Zentrums für textliche und lexikalische Ressourcen
- Gérard Duvallet ( dir. ), Medizinische und veterinärmedizinische Entomologie , IRD - Quae,2017( ISBN 978-2-7099-2376-7 ) , p. 210
- (in) AA Escalante von Freeland, WE Collins und AA Lal, " Die Evolution von Primaten-Malaria-Parasiten basierend auf dem Gen, das für mitochondriales Cytochrom b aus dem linearen Genom kodiert " , PNAS , vol. 95, n o 14,1998, s. 8124-8129 ( online lesen )
- (en) Weimin Liu, Yingying Li, Learn GH et al. , „ Ursprung des menschlichen Malariaparasiten Plasmodium falciparum bei Gorillas “ , Nature , vol. 467,2010, s. 420–425 ( online lesen )
- (en) Frederick L. Dunn, Malaria , Cambridge, Cambridge University Press ,1993, 1176 S. ( ISBN 0-521-33286-9 ) , p. 860-862.in The Cambridge Word History of Human Disease, KF Kiple (Hrsg.).
- (de) Joy D, Feng X, Mu J. et al. "Früher Ursprung und neuere Expansion von Plasmodium falciparum " Science , vol. 300, Ausgabe 5617, S. 318-21 , 2003.
- (in) Andreas Nerlich, Paläopathologie und Paläomikrobiologie der Malaria , ASM Press,2016, 212 S. ( ISBN 978-1-55581-916-3 ) , p. 155-159in Paleomicrobiology of Humans, M. Drancourt und D. Raoult (Hrsg.).
- (in) Malaria hat die Hälfte der Menschen getötet, die jemals gelebt haben Ever
- (in) Hat Malaria wirklich die Hälfte aller Menschen getötet, die jemals gelebt haben?
- (in) F. Cox "Geschichte der menschlichen Parasitologie" Clin Microbiol Rev. . 2001, Bd. 15, n o 4, p. 595-612.
- " Tutankhamun wäre an Malaria und einer Knochenkrankheit gestorben ", Le Monde.fr ,16. Februar 2010( online lesen )
- (in) Z. Hawass, YZ Gad, S. Ismail et al., „ Vorfahren und Pathologie in der Familie von König Tutanchamun “ , JAMA , vol. 303 n o 7,Februar 2010, s. 638-647 ( DOI 10.1001 / jama.2010.121 )
- (in) Paul U. Unschuld , Medicine in China: A History of Ideas (Comparative Studies of Health Systems and Medical Care) , University of California Press ,16. April 2010, 2 nd ed. , 464 S. , Überarbeitete Ausgabe ( ISBN 978-0-520-26613-1 und 0-520-26613-7 , online lesen )
- Die Geschichte der Malaria, einer uralten Krankheit . Auf der Website des Zentrums für die Kontrolle und Prävention von Krankheiten .
- (in) R. Sallares, A. Bouwman, C. Änderung, " Die Verbreitung der Malaria nach Südeuropa in der Antike: Neue Ansätze für alte Probleme " , Medizingeschichte , vol. 48, n O 3,1 st Juli 2004, s. 311–28 ( online lesen )
- (in) " Die Suche nach Chinin: Diejenigen, die die Schlachten gewonnen haben und diejenigen, die den Krieg gewonnen haben ." Von T. Kaufman und E. Rúveda, in Angew. Chem. Int. Ed. Engl. , vol. 44, n o 6, p. 854-885 , 2005.
- (in) E. Yalcindag et al. , „ Mehrere unabhängige Einführungen von Plasmodium falciparum in Südamerika “ , PNAS , vol. 109, n o 210. Januar 2012, s. 511-516 ( DOI 10.1073 / pnas.1119058109 )
- (in) R. Kyle und Mr. Shampe "Entdecker des Chinins" JAMA 1974 Flug. 229, n o 4, p. 462 .
- Jean-Paul Bado, Kolonialmedizin und große Endemiten in Afrika 1900-1960 , Karthala Editions ,1996
- (in) " Geschichte der Beiträge des US-Militärs zum Studium der Malaria " . Von Christian F. Ockenhouse (Hrsg.).
- (de) Biographie von Alphonse Laveran . In der Nobelstiftung .
- Seite auf Ettore Marchiafava .
- Lénaick Ollivier vom Institut für Tropenmedizin des Heeresgesundheitsdienstes (IMTSSA Marseille), zitiert von Le Figaro vom 10. Juni 2008, Seite 16.
- (de) Biographie von Ronald Ross , in The Nobel Foundation .
- (in) Ross und die Entdeckung, dass Moskitos Malaria-Parasiten übertragen . Auf der Website des Zentrums für die Kontrolle und Prävention von Krankheiten .
- „ Fieber von gestern, Malaria von heute. Leben und Tod durch Krankheit “. Von Chantal Beauchamp, in Annales. Volkswirtschaften, Gesellschaften, Zivilisationen . 43 rd Jahr, n o 1, 1988, p. 252-253 .
- (in) " Plasmodium vivax (Grassi und Feletti, 1890) " .
- (in) L. Pauling, Itano H., SJ Singer und I. Wells, „ Sichelzellanämie, eine molekulare Krankheit “ , Science , vol. 110,November 1949( online lesen [PDF] )
- Chemotherapie der Malaria , unter der Leitung von HR Schwarz, Craig J. Canfield, DF Clyde W. Peters und WH Wernsdorfer, 2 th ed., Weltgesundheitsorganisation, Genf, 1984, p. 13
- Ernest Fourneau , Jacques und Thérèse Tréfouël und Germaine Benoit , „ Vorbereitungen für therapeutische Versuche. NS. Chinol-Derivate und Arsin-Chinolin “, Ann. Inst. Pasteur , n o 44,1930, s. 719.
- Ernest Fourneau , Jacques und Thérèse Tréfouël , Georges Stefanopoulo , Yvonne de Lestrange und Germaine Benoit , „ Beitrag zur Chemotherapie der Malaria: Essays über die kanarische Malaria “, Ann. Inst. Pastor , Bd. 44,1930, s. 503-533 ( Zusammenfassung ).
- Ernest Fourneau , Jacques und Thérèse Tréfouël , Daniel Bovet und Germaine Benoit , „ Beitrag zur Chemotherapie der Malaria: Essays über Dichtungsmasse (zweite These) “, Ann. Inst. Pastor , Bd. 50,1933, s. 731-744.
- Marcel Delépine , Mitteilung über Leben und Werk von Ernest Fourneau (1872-1949) (Auszug aus Bull. Soc. Chim. Fr. ), Paris, Masson et C. ie , sd (1950?), 90 S. , s. 61-63.
- (in) " Chemotherapie der Vogelmalaria " . Tschüss. K. Marshall.
- Chloroquindiphosphat .
- (in) Wall Street und der Aufstieg Hitlers . Von Anthony Sutton , in The Modern History Project , Kap. 2 „ Das Reich der IG Farben “. 1976.
- (in) " Hämozoin Biokristallisation in Plasmodium falciparum und die Antimalariaaktivität von Kristallisationsinhibitoren ." Von E. Hempelmann, in Parasitol Research , vol. 100, n o 4, p. 671-676 , 2007.
- " Geschichte von Chinin im Kampf gegen Malaria " , auf der CNRS- Website .
- (in) " Menschliche Malaria-Parasiten in kontinuierlicher Kultivierung ." Von Trager und Jensen, in Science , vol. 193, n o 4254, p. 673-675 , August 1976.
- „ Desinformation, Malaria und DDT “ , auf afis.org .
- Daniel Vangroenweghe "AIDS und Sexualität in Afrika" , EPA 2000, n o 479, p. 124-125 .
- X. Pourrut & V. Robert: "Abwesenheit von plasmodialen Infektionen bei wilden Affen des nördlichen Senegals? » In Stier. Soz. Pathol. Exot. 2009 n o 102, 1, p. 17-18 .
- "Ein enzootischer Herd der Affenmalaria" . Von SP Ramakrishnan und BN Mohan, Malaria Institute of India.
- (in) G. Robert Coatney "Simian Malaria - Its Importance to World-Wide Eradication of Malaria" JAMA 1963; 184 (11): 876-7.
- (de) Ward RA, Rutledge LC, Hickman RL. (1969) "Zyklische Übertragung von Chesson vivax Malaria subhumanen Primaten" Nature n o 224, p. 1126-1127 , zitiert in The American Journal of Tropical Medicine and Hygiene .
- (in) " Nachweis von Hypnozoiten bei einer Sporozoiten-übertragenen Plasmodium vivax-Infektion ." Von Krotoski W, Collins W, Bray R, et al. , in Am J Trop Med Hyg , vol. 31, n o 6, p. 1291-1293 , 1982. Siehe auch " Malaria-Parasiten - Entdeckung der frühen Leberform ", in Nature . Von Meis J, Verhave J, Jap P, Sinden R, Meuwissen J, vol. 302, n o 5907, p. 424-6, 1983.
- Zentrum für Studium und Forschung afrikanischer Ärzte, verbunden mit dem Universitätsklinikum und dem Laboratoire de Chimie de la Coordination ( CNRS ) von Toulouse
- (en) Held J Supan C., Salazar CL, et al., " Ferroquine and artesunat in African adult and children with Plasmodium falciparum malaria: a Phase 2, multicenter, randomized, double blind, dose-range, non-inferiority lernen. “ , Lancet Infect Dis. ,2015, s. 15 (12): 1409-19
- Paul-Sabatier - Universität von Toulouse , CNRS , IRD , und das National Museum of Natural History
- Quassia Kräutertee: ein wirksames Malariamittel . Pressemitteilung des CNRS vom 11. September 2006.
- (in) Antibakterielle Neurymenolide aus der Fidschi-Rotalge Neurymenia fraxinifolia - Zusammenfassung . Von EP Stout, AP Hasemeyer, AL Lane, TM Davenport, S. Engel, ME Hay, CR Fairchild, J. Prudhomme, K. Le Roch, W. Aalbersberg, J. Kubanek. In Org Lett. (2009); 01.01.2011 (1), pp. 225-228.
- (in) " Struktur und antibakterielle Aktivität von bromierten Diterpenen aus der Rotalge Sphaerococcus coronopifolius - Zusammenfassung" . Von V. Smyrniotopoulos, C. Vagias, MM Rahman, S. Gibbons, V. Roussis, in Chem Biodivers , 7. Januar 2010 (1), pp. 186-195.
- (in) Artikel des Microbe Magazine September 2009 über das Antimalariapotenzial von Rotalgen .
- (in) " Bioactive bromophycolides UK from the Fidschi Red Alga Callophycus serratus - Summary" For AS Lin EP Stout, J. Prudhomme K. Le Roch, Fairchild CR, SG Franzblau W. Aalbersberg, ME Hay und J. Kubanek . In J Nat Prod. , 26. Februar 2010; 73 (2), pp. 275-278.
- (in) " Pressemitteilung GlaxoSmithKline " ( Archiv • Wikiwix • Archive.is • Google • Was tun? ) (Zugriff am 29. März 2013 ) vom 20. Januar 2010.
- (in) " Moskito-Darmbakterien töten nachweislich Malaria-Parasiten " . Artikel vom 12. Mai 2011 auf Examiner.com.
- (in) " Natürliche Mikroben-vermittelte Refraktärität gegenüber Plasmodium-Infektion bei Anopheles gambiae " - Zusammenfassung . In Sciencemag.org, Artikel vom 13. Mai 2011.
- „ Malaria: das neue Medikament, das den Parasiten in der Leber und im Blut trifft “. auf der Website santelog.com.
- Marc Mennessier, " Malaria: Sanofi synthetisiert Artemisinin ", Le Figaro .fr ,14. September 2012( online lesen )
- (in) Cochrane Reviews veröffentlicht 19. April 2006 [ (in) online lesen ]
- Datenblatt: RTS, Klinische Studien zu Malaria-Impfstoffen gegen S . 17. Oktober 2007 Pressemappe, gemeinsam herausgegeben von The PATH Malaria Vaccine Initiative (PATH / MVI) und GlaxoSmithKline Biologicals (GSK Bio) |.
- (in) Informationen von Professor Alonso zum RTS, S in The Lancet vom 10. Dezember 2005.
- (in) Malaria Vaccine Initiative – Standorte ausgewählt für klinische Studien der Phase III des RTS, S / AS02A .
- (in) Selidji T Agnandji José F Fernandes Emmanuel B & Michael Bache Ramharter, „ Klinische Entwicklung des RTS, S/AS Malariaimpfstoffs: eine systematische Überprüfung der klinischen Phase-I-III-Studien “ , Future Microbiology ,6. Oktober 2015( online lesen )
- (in) R. Audran Lurati F. Ruiz, B. Genton ET Blythman, O. Ofori-Anyinam, C. Reymond, G. und F. Corradin Spertini, „ The Synthetic Plasmodium falciparum Circumsporozoite Peptide PfCS102 have a Malaria Vaccine Candidate: Eine randomisierte kontrollierte Phase-I-Studie “ , PLOS ONE ,2. Oktober 2009( DOI 10.1371 / journal.pone.0007304 )
- Pressemitteilung des Institut Pasteur .
- (in) Kampf gegen Malaria: Stärkung des Malaria-Impfstoffprogramms des US-Militärs . Von Institute of Medicine - Bericht vom 25. Mai 2006.
- (in) Phase - I - Studien von FMP2.1 / AS02A in Mali - 1 st Edition . Vom US-amerikanischen National Institute of Health. 27. Juli 2006.
- "Ein neuer experimenteller Impfstoff" . Artikel vom 4. Februar 2010 (Quelle AFP ). Auf der Seite guinee24.com.
- (in) US National Institute of Health: Phase-I-Studien zu FMP2.1 / AS02A in Mali . 1 st Ausgabe: 12. April 2007.
- Impfstoff könnte tödliche Waffe gegen Malaria und Cholera sein . Von University of Central Florida, Pressemitteilung vom 26. Januar 2010.
- (in) " Von Chloroplasten abgeleitete Impfstoffantigene verleihen durch orale Verabreichung oder Injektion Immunität gegen Cholera und Malaria. "- Zusammenfassung . Von A. Davoodi-Semiromi, M. Schreiber, S. Nalapalli, D. Verma, ND Singh, RK Banks, D. Chakrabarti und H. Daniell, in Plant Biotechnol J. , Februar 2010; 8 (2), pp. 223-242. Epub 28. Dezember 2009. .
- A transplastomischen Pflanze ist eine Pflanze , deren Chloroplasten wurden genetisch in transformierten zu multiplizieren , um Transgenen pro Zelle.
- (en) „Der Malaria-Impfstoff des Oxford-Covid-19-Teams ist der wirksamste, der je hergestellt wurde “ , New Scientist .23. April 2021( online lesen , eingesehen am 29. April 2021 ).
- Lebenslauf Professor Crisanti [ (in) online lesen ]
- (in) Artikel in Science Daily vom 21. Februar 2003.
- Website Genoscope - Artikel zur vollständigen Sequenzierung des Genoms von Anopheles gambiae [ (de) online lesen ]
- Akademie der Wissenschaften des Institut de France - Artikel vom 12. Juni 2007 „ http://www.academie-sciences.fr/conferences/seances_publiques/pdf/gas_12_06_07_C_Frolet.pdf “ ( Archiv • Wikiwix • Archive.is • Google • Was tun? )
- Artikel über Anopheles gambiae auf der Genoscope- Website .
- (in) " Die erste Malaria-sichere Mücke " . Von Daniel Stolte, University of Arizona - Mitteilung vom 15. Juli 2010.
- (in) Zusammenfassung des World Malaria Report 2015 ( online lesen ) , S. 5
- (in) Datentabelle F: Geschätzte Risikopopulation und Malariafälle und Todesfälle, 2010-2018 ( online lesen )
- (in) J. Breman, „ Die Ohren des Nilpferds: Manifestationen, Determinanten und Schätzungen der Malariabelastung “, in Am J Trop Med Hyg , vol. 64, Nr . 1-2, p. 1-11 , 2001 [ online lesen ]
- Schätzungen sind aufgrund der Unzuverlässigkeit der Statistiken in den betreffenden Ländern schwierig; in 2005 , Forscher in der Zeitschrift geschätzt Natur bei 515 Millionen der Zahl der Kranken in 2002 (in einem Bereich von 300 bis 660.000.000 gehen), während die Schätzung der WHO im Jahr 1999 in seinem Bericht über die Gesundheit in der Welt 273 Millionen. Die WHO sagte, sie habe diese Zahl im folgenden Jahr revidiert und seitdem mit einer Spanne von 300 bis 500 Millionen gearbeitet. Vgl. die Botschaft von John Bonner vom 10. März 2005 (15:18 Uhr), „Row erupts over WHO’s malaria 'miscalculation'“, auf der New Scientist-Website [ (en) online lesen ]
- „ Factsheet on the World Malaria Report 2013 “ , zur WHO ,Dezember 2013
- (en) Greenwood BM, Bojang K, Whitty CJ, Targett GA, „ Malaria “, in The Lancet , vol. 365, s. 1487-1498, 2005.
- (in) Hay S, C Guerra, Tatem A, Noor A, R Snow, „ Die globale Verbreitung und Bevölkerung mit Risiko von Malaria: Vergangenheit, Gegenwart und Zukunft “ in Lancet Infect Dis , vol. 4, n o 6, pp. 327-36, 2004.
- Murray CJL, Rosenfeld LC, Lim SS et al. Globale Malariamortalität zwischen 1980 und 2010: eine systematische Analyse , Lancet, 2012; 379: 413-431
- (in) Korenromp E, B Williams, S Vlas, Gouws E, C Gilks, Ghys P Nahlen B, " Malaria zuzurechnenden die HIV-1 - Epidemie, Afrika südlich der Sahara " in Emerg Infect Dis , Bd. 11, n o 9, pp. 1410-1419, 2005 [ online lesen ]
- (in) Abu-Raddad L, P Patnaik, Kublin J „ Doppelinfektion mit HIV und Malaria befeuert die Ausbreitung beider Krankheiten in Afrika südlich der Sahara “, in Science , vol. 314 n o 5805, pp. 1603-1606, 2006.
- (in) Layne SP, Principles of Infectious Disease Epidemiology , EPI 220, UCLA Department of Epidemiology [ online lesen ]
- Greenwood B Mutabingwa T, "Malaria im Jahr 2002", in Nature , vol. 415, Nr . 670-2, 2002.
- (in) Grover-Kopec E, M Kawano, Klaver R Blumenthal B Ceccato P, S Connor, "Eine Online-Ressource zur operativen Niederschlagsüberwachung für epidemische Malaria-Frühwarnsysteme in Afrika" Malar J. 2005, vol. 4, s. 6. [ online lesen ]
- (in) Van Benthem B Vanwambeke S Khantikul N, Burghoorn-Maas C Panart K Oskam L Lambin E, Somboon P „Räumliche Muster und Risikofaktoren für Seropositivität für Dengue-Infektion“, Am J Trop Med Hyg . 2005, Bd. 72, n o 2, p. 201-8. [ online lesen ]
- (in) Trung H, Van Bortel W Sochantha T Keokenchanh K, N Quang Cong L, M Coosemans, "Malaria-Übertragung und Haupt-Malaria-Vektoren in verschiedenen geografischen Gebieten Südostasiens" Trop Med Int Health 2004 Flug. 9, n o 2, p. 230-7, 2004.
- Rémi Barroux , „ Sri Lanka hat nach jahrzehntelangem Kampf die Malaria besiegt “, Le Monde.fr ,13. September 2016( online lesen , eingesehen am 25. April 2017 )
- https://www.france24.com/fr/asie-pacifique/20210630-apr%C3%A8s-70-ans-de-lutte-la-chine-ar%C3%A9ussi-a-%C3%A9radiquer- Malaria
- (in) Keizer J, Utzinger J, Caldas de Castro M, Smith T, Tanner M, Singer B, „ Urbanisierung in Afrika südlich der Sahara und Auswirkungen auf die Malariakontrolle “, in Am J Trop Med Hyg , vol. 71, n o 2, p. 118-27, 2004 [ online lesen ]
- (in) Hay SI, Snow RW, „ The Malaria Atlas Project: Developing Global Maps of Malaria Risk “ in PLoS Medicine , vol. 3, n o 12, p. e473, 2006 [ online lesen ]
- Callot J.: "Ein komplexes Problem: die Rückbildung der Malaria in Frankreich" . In: Annalen. Volkswirtschaften, Gesellschaften und Kulturen , 2 - ten Jahr, n o 3, 1947, S.. 330-332.
- Adéa Guillot, „ In Griechenland, die Not und Isolation der Migranten aus dem Lager Frakaport “, Le Monde .fr ,2. September 2016( online lesen )
- Pierre-Olivier Fanica, „ Das Verschwinden der Malaria im ländlichen Frankreich und die Rückbildung der Feuchtgebiete: Beispiel der Sologne “, tude et Gestion des Sols , vol. 13, n o 1,2006, s. 53-61 ( online lesen [PDF] )
- Gilles Bouvenot, Bernard Devulder und Loïc Guillevin, Medizinische Pathologie , Band 2: Immunpathologie, Allergologie, Infektionskrankheiten, Parasitologie, Geriatrie, Masson-Ausgaben, Abrégé Médecine, 1994, p. 336.
- Figaro- Podcast .
- Moskitosinfos.sante.gouv.fr „Malaria auf der Insel La Réunion und in der Welt“ auf der Website des französischen Gesundheitsministeriums.
- (de) Bruno Pradines, „ Epidemiologie der importierten Malaria in Frankreich “ , The Practitioner's Review , vol. 69,Februar 2019, s. 150-152
- Olivier Bouchaud und Bruno Pradines, „ Situation der Malaria in der Welt “, La Revue du Praticien , Bd. 69,Februar 2019, s. 145-149
- G. Brücker, " Pathologie von Urlaub und Rückkehr ", La Revue du Praticien , vol. 34 "Pathology of Zug", n o 57,11. Dezember 1984, s. 3223-3228
- Simon I. Hay et al. „Die globale Verbreitung und Bevölkerung mit Malariarisiko: Vergangenheit, Gegenwart und Zukunft“ The Lancet Infectious Diseases , vol. 4, n o 6, Juni 2004, S.. 327-336 [ (in) online lesen ]
- Weltmalariabericht 2011 auf der WHO-Website
- Sekretariat des Übereinkommens über die biologische Vielfalt, „ The LifeWeb Initiative “ ( Archiv • Wikiwix • Archive.is • Google • Was tun? ) (Zugriff am 29. März 2013 ) (doppelseitige Farbbroschüre)
- Le Figaro vom 10. Juni 2008, Seite 16.
- (in) Braginets OP Minakawa N, Mbogo CM Yan G. "Population genetische Struktur der afrikanischen Malariamücke Anopheles funestus in Kenia" The American Journal of Tropical Medicine & Hygiene 2003; 69 (3) 303-8 [ online lesen read ]
- (in) Darwin H. Stapleton "Geschichte? » Chronik der öffentlichen Gesundheit , März-April 2004, vol. 119.
- (in) Marcus Hall: "The Rockefeller Foundation in Sardinia: Pesticide Politics in the Struggle Against Malaria - Environmental Values (1991-2002)" , 28. März 2005.
- Auriane Guilbaud, Malaria – Der globale Kampf gegen einen resistenten Parasiten , L'Harmattan, Chaos internationale Sammlung, 2008, S. 32 .
- Pierre Mouchet et allii, Biodiversität der Malaria in der Welt , John Libbey Eurotext, 2004.
- WHO (2019) Bericht über die Ausrottung der Malaria: Nutzen, Zukunftsszenarien und Durchführbarkeit. Zusammenfassung des Berichts der Strategischen Beratungsgruppe der WHO zur Ausrottung der Malaria , 23. August 2019; CC BY-NC-SA 3.0 IGO; PDF, 172 kB; 13pp
- Martin Enserink (2019) [ https://www.sciencemag.org/news/2019/08/setting-deadline-erdicating-malaria-good-idea-scientists-are-divided (Eine Frist zur Beendigung der Malaria ist es eine gute Idee? Wissenschaftler sind gespalten) ] 27. August 2019
- „ Große Fortschritte im Kampf gegen Malaria “ , zur WHO ,11. Dezember 2013
- (in) Victoria A. Ingham , Amalia Anthousi Vassilis Douris und Nicholas J. Harding , „ Ein sensorisches Anhängselprotein schützt Malariavektoren vor Pyrethroiden “ , Nature , vol. 577, n o 7790,Januar 2020, s. 376–380 ( ISSN 1476-4687 , PMID 31875852 , PMCID PMC6974402 , DOI 10.1038 / s41586-019-1864-1 , online gelesen , abgerufen am 31. Mai 2020 )
- (in) J. Sachs und P. Malaney, „Die wirtschaftliche und soziale Belastung der Malaria“, Nature , 2002, vol. 415, s. 680-5.
- Roll Back Malaria Malaria in Afrika , Newsletter n o 3, [ online lesen ]
- Sandi Doughton, Artikel Seattle Times 13. Juni 2008 - " Reviving Low-Tech-Lösungen " [ (in) online lesen ]
- Roll Back Malaria, Wirtschaftliche Kosten von Malaria , OMS [ online lesen ]
- (in) K. Mendis, B. Sina, Marchesini P. und R. Carter, „ Die Last der vernachlässigten Plasmodium vivax Malaria “ , Am J. Trop Med , Vol. 2 , No. 64, n Knochen 1-2S,2001, s. 97-106 ( online lesen [PDF] )
- (in) AA Escalante und FJ Ayala, " Phylogenie der Malaria- Gattung Plasmodium , abgeleitet von rRNA Gensequenzen " , PNAS , Bd. 91, n o 24,1994, s. 11373-7 ( online lesen [PDF] )
- (in) PCC Garnham, Malaria parasites and other Haemosporidia , Blackwell Scientific Publications, Oxford, 1996.
- Permin A. und Madsen M., Investing in Animal Health Research to Linderung Poverty , International Livestock Research Institute, 2001, Anhang 2: Überprüfung des Auftretens und der Auswirkungen von Krankheiten (Kleinbauerngeflügel) [ online lesen ]
- (in) Atkinson CT, Woods KL, Dusek RJ, Sileo LS Iko WM "Wildlife Disease and Conservation in Hawaii pathogenicity of avian malaria ( Plasmodium relictum ) in experimentell infizierter Iiwi ( Vestiaria coccinea )" Parasitology 1995; 111 Suppl. : S59- 69.
- Science & Vie vom 6. Dezember 2009: „ Anopheles in einer schmutzigen Socke gefangen “ „ http://mondedurable.science-et-vie.com/2009/12/lanophele-piege-par-une-chaussette-sale/ » ( Archiv • Wikiwix • Archive.is • Google • Was tun? )
- (in) Oshikazu Shirai , Takao Tsuda Shinya Kitagawa und Ken Naitoh , „ Alkoholaufnahme stimuliert Mückenanziehung “ , Journal of the American Mosquito Control Association , Vol. 18, n o 2Juni 2002, s. 91–96 ( ISSN 8756-971X , PMID 12083361 , online gelesen , abgerufen am 26. Juni 2017 )
- (in) RJ Pitts, CD Rinker, PL Jones, A. Rokas LJ und LJ Zwiebel, „ Transcriptome profiling of chemosensory appendages in the malaria vector Anopheles gambiae Reveals Tissue and sex-specific signatures of odor Coding “ , BMC Genomics , Flight. 12,2011, s. 271 ( DOI 10.1186 / 1471-2164-12-271 )
- (in) T. Lefevre, C. Lebarbenchon, Gauthier-Clerc, Misse D., R. Poulin und F. Thomas, „ Die ökologische Bedeutung manipulativer Parasiten “ , Trends Ecol Evol , vol. 24, n o 1,2009, s. 41–48 ( online lesen [PDF] )
- (in) KD Lafferty und Kuris AM, "Ökologische Folgen von manipulativen Parasiten" in Host Manipulation by Parasites , Hrsg. DP Hughes, J Brodeur, Thomas F (Oxford University Press, New York)2012( online lesen ) , s. 158–179
- (in) T. Lefèvre und F. Thomas, " Hinter der Bühne, etwas anderes die Fäden in der Hand: parasitäre Manipulation in Vektor- übertragene Krankheiten betonend " , Infect Genet Evol , vol. 8, n o 4,2008, s. 504–519 ( online lesen [PDF] )
- Poulin R (2010) Parasitenmanipulation des Wirtsverhaltens: Ein Update und häufig gestellte Fragen . Fortschritte in der Verhaltensforschung, Hrsg. Mitani J, et al. (Elsevier, New York) Bd. 41, S. 151–186.
- H. Hurd (2003) Manipulation von medizinisch wichtigen Insektenvektoren durch ihre Parasiten . Annu Rev. Entomol 48 (1): 141–161.
- (en) De Moraes CM, Stanczyk NM, Betz HS, Pulido H, Sim DG, Read AF, Mescher MC, „ Malaria-induzierte Veränderungen der Wirtsgerüche verstärken die Anziehungskraft von Mücken “ , PNAS , vol. 111,2014, s. 11079–11084 ( DOI 10.1073 / pnas.1405617111 , online lesen [PDF] )
- Ferguson HM, Read AF (2004) Der Appetit der Mücken auf Blut wird durch Plasmodium chabaudi-Infektionen bei sich selbst und ihren Wirbeltierwirten stimuliert . Malar J 3:12.
- (en) R. Lacroix, WR Mukabana, LC Gouagna und JC Koella, „ Malaria-Infektion erhöht die Attraktivität des Menschen für Mücken “ , PLoS Biol 3: e298 ,2005( DOI 10.1371 / journal.pbio.0030298 )
- Cornet S, Nicot A, Rivero A, Gandon S (2013) Malaria-Infektion erhöht die Attraktivität von Vögeln für nicht infizierte Mücken . Ecoll Lett 16: 323–329. doi: 10.1111 / ele.12041.
- Van Dooren GG, Striepen B (2013) „Die Algenvergangenheit und Parasitenpräsenz des Apicoplasten“. Annu Rev. Microbiol 67: 271–289. doi: 10.1146 / annurev-micro-092412-155741 ( Zusammenfassung ).
- Molekularer Mikrobiologieforscher und Spezialist für Malaria bei Kindern an der Washington University School of Medicine in St. Louis
- Website der School of Medicine der Washington University in St. Louis
- Imlay L & Odom AR (2014) Isoprenoid-Metabolismus in apikomplexen Parasiten . Aktuelle Klinische Mikrobiologie-Berichte. 1.3-4 (2014): 37-50
- Guggisberg, AM, Amthor, RE und Odom, AR (2014) Isoprenoid-Biosynthese in Plasmodium falciparum . Eukaryotische Zelle. 13.11 (2014): 1348-1359 ( Zusammenfassung )
- Wong RP, Flematti GR & Davis TM (2012) „ Untersuchung von flüchtigen organischen Biomarkern aus Plasmodium falciparum in vitro “. Malar J 11: 314. doi: 10.1186 / 1475-2875-11-314
- Kelly, M., Su, CY., Schaber, C., Crowley, JR, Hsu, FF., Carlson, JR, Odom, AR (2015) „ Malariaparasiten produzieren flüchtige Mückenlockstoffe “ . mBio doi: 10.1128 / mBio.00235-15, vol. 6 Nr. 2 e00235-15
- (in) VO Nyasembe, PEA Teal, WR Mukabana, JH Tumlinson und B. Torto, „ Verhaltensantwort des Malariavektors Anopheles gambiae auf flüchtige Stoffe und synthetische Mischungen der Wirtspflanze “ , Parasites & Vectors , vol. 5,2012, s. 234 ( online lesen [PDF] )
- Dekker T, Geier M & Cardé RT (2005) „ Kohlendioxid sensibilisiert weibliche Gelbfiebermücken sofort für menschliche Hautgerüche “. J. Exp. Biol. 208: 2963–2972. doi: 10.1242 / jeb.01736 ( Zusammenfassung ).
- (in) CJ McMeniman, RA Corfas, BJ Matthews, SA Ritchie SA und LB Vosshall, „ Multimodale Integration von Kohlendioxid und anderen sensorischen Hinweisen treibt die Anziehungskraft von Mücken auf den Menschen “ , Cell , vol. 156,2014, s. 1060–1071 ( DOI 10.1016 / j.cell.2013.12.044 , online lesen [PDF] )
- Website des St. Louis Hospital Laboratory
- (in) Talman A. Domarle O., F. McKenzie, Ariey F. Robert V. „ Gametocytogenese: die Pubertät von Plasmodium falciparum “ in Malar J , Vol. 2 , No. 3, s. 24.
- Malaria-Entomologie und Vektorkontrolle (S. 7-8), WHO 2003 [ online lesen ]
- MEDIZIN / WISSENSCHAFTEN 2005 (Proteinverkehr in den durch Plasmodium infizierten roten Blutkörperchen) [ online lesen ]
- (in) Cécile Crosnier Leyla Y. Bustamante S. Josefin Bartholdson Amy K. Bei Michel Theron, Makoto Uchikawa Souleymane Mboup Omar Ndir Dominic P. Kwiatkowski, Manoj T. Duraisingh, Julian C. Rayner und Gavin J. Wright, Basigin ist a Rezeptor essentiell für die Erythrozyteninvasion durch Plasmodium falciparum . online lesen .
- E. Pilly, Infektions- und Tropenkrankheiten: alle Infektionskrankheiten , Paris, Alinéa Plus,2018, 720 S. ( ISBN 978-2-916641-66-9 ) , p. 512-514
- Universität Paris Val de Marne - 2000 - Diplomarbeit zum Doktor der Medizin (Titel 1.2.2.) [ Online lesen ]
- (in) Cox-Singh J, Davis TM, Lee KS, Shamsul SS Matusop A Ratnam S, Rahman HA Conway DJ, Singh B, „ Plasmodium knowlesi malaria beim Menschen ist weit verbreitet und potenziell lebensbedrohlich “ , Clin Infect Say , vol . 46, n o 22008, s. 165-71. ( PMID 18171245 , PMCID PMC2533694 , DOI 10.1086 / 524888 , online lesen [html] )
- Marc Gentilini, Tropenmedizin , Paris, Flammarion Medicine-Sciences,1993, 928 S. ( ISBN 2-257-14394-9 ) , p. 101.
- (in) Ergebnisse einer Studie an Mäusen DOI : 10.1038 / nm.2368
- NCBI - Taxonomie-Browser (Navigator zu den genetischen Codes von Artenunterschieden Plasmodium falciparum ) [ (in) online lesen ]
- P. Bartolucci, „ Hämoglobinopathien: ein Vorteil gegen Malaria, aber das Risiko schwerer Krankheiten “, La Revue du Praticien , vol. 64,Oktober 2014, s. 1110-1011
- (in) Denis Pierron , Margit Heiske , Harilanto Razafindrazaka und Veronica Pereda-loth , „ Starke Selektion während des letzten Jahrtausends für afrikanische Abstammung in der gemischten Bevölkerung Madagaskars “ , Nature Communications , Bd. 9, n o 1,2. März 2018, s. 932 ( ISSN 2041-1723 , PMID 29500350 , PMCID PMC5834599 , DOI 10.1038 / s41467-018-03342-5 , online gelesen , abgerufen am 8. November 2020 )
- CNRS - Malaria - Der P. vivax- Parasit infiziert bisher als resistent geltende Populationen - 16. März 2010 [ (fr) online lesen ]
- (in) Carolina Lopez, Carolina Saravia et al. „Mechanismen der genetisch bedingten Resistenz gegen Malaria“ Gene 2010; 467 (1-2): 1-12.
- Nicolas Vignier, „ Management einfacher Malaria-Attacken, ein therapeutischer Notfall “, La Revue du Praticien , vol. 69,Februar 2019, s. 152-158
- Johann Cailhol, „ Malaria “, The Practitioner's Review , vol. 64,Dezember 2014, s. 1457-1468
- Von Fritz H. Kayser ( über. Von Deutsch), Taschenhandbuch für Medizinische Mikrobiologie , Paris, Flammarion Médecine-Sciences,2008, 764 S. ( ISBN 978-2-257-11335-1 ) , p. 597-599.
- Marc Gentilini 1994, op. cit., p. 95.
- Marc Gentilini 1993, op. cit., p. 103-106.
- A. Manuila, Französisches Wörterbuch für Medizin und Biologie , t. II, Paris, Masson,1971, s. 207-210
- Von der WHO verabschiedete Kriterien für schwere Malaria [ online lesen ] , S. 131. fünfzehn.
- Trampuz A, Jereb M, Muzlovic I, Prabhu R, „Klinische Überprüfung: Schwere Malaria“, in Crit Care , vol. 7, n o 4, p. 315-23, 2003 [ online lesen ]
- Kain K, Harrington M, Tennyson S, Keystone J, „Importierte Malaria: prospektive Analyse von Problemen bei Diagnose und Management“ Clin Infect Dis . 1998, Bd. 27, n o 1, p. 142-9.
- Stéphane Jauréguiberry, " Access Malaria ", La Revue du Praticien - Allgemeinmedizin , vol. 21, Nr . 754/755,16. Januar 2007, s. 23-28.
- Redd S et al., „Klinischer Algorithmus zur Behandlung von Plasmodium falciparum Malaria bei Kindern“, in Lancet , vol. 347, n o 8996, S.. 223-7, 1996.
- American Journal of Public Health "Community Health Worker Performance in the Management of Childhood Illnesses Multiple: Siaya District, Kenya, 1997-2001" im Oktober 2001 [ (in) online lesen ]
- (in) Pattanasin S. et al. „Evaluierung eines neuen Plasmodium-Laktat-Dehydrogenase-Assays (OptiMAL-IT) zum Nachweis von Malaria“ Transact Royal Soc Trop Med . 2003, Bd. 97, s. 672-4.
- RollBackMalaria - Verbrauchs- und nichtmedizinische Produkte gegen Malaria - Seminar vom 5. bis 9. März 2006 in Dakar [ online lesen ]
- (de) Ling IT. et al. "Antikörper gegen die Glutamatdehydrogenase von Plasmodium falciparum " Parasitology 1986, vol. 92, s. 313-24.
- „ Schnelltests für Malaria “ , auf medecinetropicale.free.fr ,2018
- (in) Adak T, Sharma V, V Orlov, "Studien über das Plasmodium vivax-Rezidivmuster in Delhi, Indien", in Am J. Trop Med Hyg , vol. 59, n o 1, p. 175-9, 1998
- Marc Gentilini 1994, op. cit., p. 109.
- Marc Gentilini 1994, op. cit., p. 107-109.
- Bénédicte Girard, " Fieber und Schwangerschaft ", La Revue du Praticien , vol. 57,31. März 2007, s. 665-669
- „ WER | The World Malaria Report 2019 at a Glance “ , zur WHO (Zugriff am 15. Dezember 2019 )
- (in) Athena P. Kourtis, „ Schwangerschaft und Infektion “ , The New England Journal of Medicine , vol. 370, n o 23,5. Juni 2014, s. 2211-2218.
- (in) Zhi-yong Tao Qiang Fang , Xue Liu und Richard Culleton , „ Angeborene Malaria in China “ , PLoS Vernachlässigte Tropenkrankheiten , vol. 8, n O 3,13. März 2014( ISSN 1935-2727 , PMID 24626148 , PMCID 3953009 , DOI 10.1371 / journal.pntd.0002622 , online gelesen , abgerufen am 13. Dezember 2019 )
- (en) Jane Crawley, „ Malaria bei Kindern “ , Lancet , vol. 375,24. April 2010, s. 1468-1481.
- (in) Lauren M. Cohee und Miriam K. Laufer , " Malaria bei Kindern " , Pädiatrische Kliniken von Nordamerika , vol. 64, n o 4,August 2017, s. 851–866 ( ISSN 0031-3955 , PMID 28734514 , PMCID 5733786 , DOI 10.1016 / j.pcl.2017.03.004 , online gelesen , abgerufen am 15. Dezember 2019 )
- Tania Ikowsky, "Importierte Malaria bei Säuglingen ", La Revue du Praticien - Médecine générale , vol. 23, n o 824,16. Juni 2009, s. 431-432
- (in) Kimberly E. Mace und Mr. Paul Arguin , " Malaria Surveillance - United States, 2014 " , MMWR Surveillance Summaries , vol. 66, n o 12,26. Mai 2017, s. 1–24 ( ISSN 1546-0738 , PMID 28542123 , PMCID 5829864 , DOI 10.15585 / mmwr.ss6612a1 , online gelesen , abgerufen am 15. Dezember 2019 )
- Marc Gentilini 1994, op. cit., p. 110.
- (en) Federica Verra , Andrea Angheben , Elisa Martello und Giovanni Giorli , „ Eine systematische Übersicht über transfusionsübertragene Malaria in nicht-endemischen Gebieten “ , Malaria Journal , vol. 17,16. Januar 2018( ISSN 1475-2875 , PMID 29338786 , PMCID 5771189 , DOI 10.1186 / s12936-018-2181-0 , online gelesen , abgerufen am 16. Dezember 2019 )
- F. Denis, Bacteria, fungi and parasites transmissible from mother to child , John Libbey Eurotext, 2002, p. 376.
- (en) Ehsan Ahmadpour , Masoud Foroutan-Rad , Hamidreza Majidiani und Sirous Mehrani Moghaddam , „ Transfusion-Transmitted Malaria: A Systematic Review and Meta-analysis “ , Open Forum Infectious Diseases , vol. 6, n O 7,11. Juni 2019( ISSN 2328-8957 , PMID 31334300 , PMCID 6634438 , DOI 10.1093 / ofid / ofz283 , online gelesen , abgerufen am 16. Dezember 2019 )
- J. Ranque: "Malaria nach Transfusionen: aktueller Stand der Dinge" .
- François Lefrère, „ Aktuelle Transfusionsrisiken “, La Revue du Praticien – Médecine générale , Bd. 27, n o 894,Januar 2013, s. 74-75
- „ Malaria: Stellungnahme zu Transfusionssicherheit und Transplantationen “ , auf hcsp.fr ,September 2019, s. 7-8
- Nicolas Vignier, „ Besondere Formen der Malaria “, La Revue du Praticien , vol. 69,Februar 2019, s. 159-161
- (in) Danielle I. Stanisic , James S. McCarthy und Michael F. Good , „ Controlled Human Malaria Infection: Applications, Advances, and Challenges “ , Infection and Immunity , Vol. 2 , No. 86, n o 1,19. Dez. 2017( ISSN 0019-9567 , PMID 28923897 , PMCID 5736798 , DOI 10.1128 / IAI.00479-17 , online gelesen , abgerufen am 16. Dezember 2019 )
- (de) Mockenhaupt F. et al. „Manifestation und Ausgang schwerer Malaria bei Kindern in Nordghana“ Am J Trop Med Hyg. 2004; 71 (2): 167-72.
- Veraltete Medikamente verzögern den Sieg gegen Malaria - Artikel der Daily Nation 30.06.2009 [ (in) online lesen ]
- immer Privatkliniken verwenden ältere Behandlungen - Artikel der Daily Nation vom 23.04.2009 [ (in) online lesen ]
- BEH - Chemosensitivität der 2001 und 2002 nach Frankreich importierten Malaria (Artikel vom 3. Februar 2004) [ (en) online lesen ]
- (in) Nicholas J. White, „ Malaria – Zeit zum Handeln “ , New Eng. J. Med. , Bd. 355,9. November 2006, s. 1956-1957 ( online lesen )
- (in) K. Laufer, PC Thesing, ND Eddington, R. Masonga, FK Dzinjalamala, SL Takala, TE Taylor und CV Plowe, „ Return of Chloroquine Antimalariaal Efficacy in Malawi “ , New Engl. J. Med. , Bd. 355,9. November 2006, s. 1959-1966 ( online lesen )
- (in) Shweta Sinha , Bikash Medhi und Rakesh Sehgal , „ Herausforderungen der arzneimittelresistenten Malaria “ , Parasite , vol. 21,2014, s. 61 ( ISSN 1776-1042 , DOI 10.1051 / Parasit / 2014059 )
- (in) Brian KS Yeung , Bin Zou , Matthias Rottmann et al. , „ Spirotetrahydro-Beta-Carboline (Spiroindolone): Eine neue Klasse potenter und oral wirksamer Verbindungen zur Behandlung von Malaria “ , J. Med. Chem.-Nr. , Bd. 53, n o 14,22. Juni 2010, s. 5155-5164 ( Zusammenfassung ).
- (en) Nicholas J. White , Sasithon Pukrittayakamee Aung Pyae Phyo et al. , " Spiroindolone KAE609 für Falciparum und Vivax Malaria " , N. Engl. J. Med. , N o 376,31. Juli 2014, s. 404-410 ( Zusammenfassung ).
- Nobutaka Kato (2016) Diversity-orientierte Synthese liefert neue mehrstufige Antimalaria-Inhibitoren ; Natur ; doi: 10.1038 / nature19804, hochgeladen: 07.09.2016, abgerufen am 10.09.2016
- Lon CT, Tsuyuoka R, Phanouvong S et al. „Gefälschte und minderwertige Malariamedikamente in Kambodscha“, in Trans R Soc Trop Med Hyg , vol. 100, n o 11, p. 1019-24, 2006.
- (in) US Pharmacopeia, gefälschte Malariamittel gefunden in der Provinz Yunan, China 2004 " http://www.uspdqi.org/pubs/other/FakeAntimalarialsinChina.pdf " ( Archiv • Wikiwix • Archive.is • Google • Was tun? )
- (in) Newton PN, Green MD, Fernández FM Day JSP, NJ White, "Gefälschte Antiinfektiva" in Lancet Infect Dis , vol. 6, n o 9, p. 602-13, 2006
- BBC News, 17. August 2007 [ online lesen ]
- Kevin Hull, Malaria: Fever Wars , PBS Documentary, 2006 “ http://www.wgbh.org:81/cgi-bin/nph-algs.cgi/000000A/http/www.wgbh.org/schedules/program- info? program_id = 2682027 & episode_id = 2682029 » ( Archiv • Wikiwix • Archive.is • Google • Was tun? )
- Barat, „Vier Malaria-Erfolgsgeschichten: Wie die Malariabelastung in Brasilien, Eritrea, Indien und Vietnam erfolgreich reduziert wurde“, in Am J Trop Med Hyg , vol. 74, n o 1, p.12-16 2006.
- WHO-Position zum Einsatz von DDT 2005 [ online lesen ]
- Präfektur La Réunion - Ministerium für Gesundheit und Soziales - Der Kampf gegen Mücken - 2006 [ online lesen ]
- Weltgesundheitsorganisation , Planung von Malaria-Kontrollprogrammen: Ein Leitfaden für Auszubildende , hrsg. vorläufig, WHO , Genf , 2003 , p. 128 [ online lesen ]
- " Was ist eine Fledermaus?" » , Auf www.nuitdelachauvesouris.com
- "Mosquito Genome Sequencing, veröffentlicht in der Zeitschrift Science, öffnet den Weg zu neuen Mitteln zur Bekämpfung von Malaria" Eurekalert.org , 2. Oktober 2002 [ online lesen ]
- (in) Smit MR, Ochomo EO Aljayyoussi G, et al., „ Sicherheit und Wirksamkeit von Moskitozid-Hochdosis-Ivermectin bei gleichzeitiger Anwendung mit Dihydroartemisinin-Piperaquin bei kenianischen Erwachsenen mit unkomplizierter Malaria (IVERMAL): eine randomisierte, doppelblinde , Placebo-kontrollierte Studie ” , The Lancet Infectious Diseases , vol. 18, n o 6,27. März 2018, s. 615-626 ( DOI 10.1016 / s1473-3099 (18) 30163-4 , online lesen )
- (in) EJ Kweka F. Mosha Lowassa A. et al., „ Ethnobotanical study of Reviews some of Mückenabwehrpflanzen im Nordosten Tansanias “ , Malaria Journal , Vol. 2 , No. 7,2008, s. 152 ( DOI 10.1186 / 1475-2875-7-152 )
- Saltidin - Technische Informationen (de) „ http://www.bayrepel.com/?501A1 “ ( Archiv • Wikiwix • Archive.is • Google • Was tun? )
- Institut für Tropenmedizin Antwerpen-Gesundheitsratgeber für Reisende, Ausgabe für Ärzteschaft 2007-2008 [[ http://www.itg.be/ITG/Uploads/MedServ/fmedasso.pdf online lesen]]
- ITG (Instituut voor Tropische Geneeskunde-Ihre Gesundheit auf Reisen-Malaria (Stand August 2008) [ online lesen ]
- Belgisches Zentrum für pharmakotherapeutische Informationen-Kommentare, Dosierung von Tetracyclinen [ online lesen ]
- Belgisches Zentrum für pharmakotherapeutische Informationen-Kommentare, Dosierung von Antimalariamitteln-Verzeichnis "Name der Fachrichtung" beginnend mit "L" [ online lesen ]
- Belgisches Zentrum für pharmakotherapeutische Informationen-Kommentare, Dosierung von Antimalariamitteln-Verzeichnis "Name der Spezialität" beginnend mit "M" [ online lesen ]
- Artikel im Standard vom 8. Mai 2010 - Malaria-Bekämpfung per SMS [ (in) online lesen ]
Siehe auch
Literaturverzeichnis
- Jacques Verdrager, WHO und Malaria: Erinnerungen eines auf Malaria spezialisierten Arztes . - L'Harmattan, Coll. „Schauspieler der Wissenschaft“, Paris, 2005 ( ISBN 2-7475-8246-9 )
- „Reisende , die Gesundheit und Sanitär Empfehlungen 2005” Weekly Epidemiologische Bulletin , n o 24-25 / 2005 (14. Juni 2005) [ online lesen ]
- (fr) Robert W. Snow et al. „Die globale Verteilung der klinischen Episoden von Plasmodium falciparum Malaria“, Nature , vol. 434, n o 7030 (10. März 2005), p. 214-217 [ (de) Online-Präsentation ]
- Marie Josserand Debacker, Malaria: Geschichte, Mythen, Überzeugungen und empfangene Ideen , Übungsarbeit, Medizin, Paris XII , 2000 [ online lesen ]
- Serge Paul Eholié, Emmanuel Bissagnéné und Pierre-Marie Girard (dir.), Therapeutic Memento of Malaria in Africa , Doin, IMEA, Paris, 2008, 139 Seiten ( ISBN 978-2-7040-1253-4 )
- Christian Lengeler, Jacqueline Cattani und Don de Savigny (Hrsg.), Eine Mauer gegen Malaria: Etwas Neues bei der Verhinderung von Malaria-Todesfällen , International Development Research Center, Ottawa; Weltgesundheitsorganisation, Genf, 1997, 220 Seiten ( ISBN 0-88936-831-7 )
- Jean Mouchet, Pierre Carnevale, Marc Coosemans et al. Biodiversität der Malaria in der Welt , J. Libbey Eurotext, Montrouge, 2004, 428 Seiten ( ISBN 2-7420-0528-5 )
Filmografie
- Malaria, die stille Hekatombe , Dokumentarfilm unter der Regie von Bernard Germain und Jean Vercoutère, produziert von Mosaïque Films (Paris) und vertrieben von ADAV, 2000, 54 Minuten (VHS)
- Les Faucheurs de Palu , 52-minütiger Dokumentarfilm unter der Regie von Patrice Desenne, produziert von Effervescence, France 5, Public Senate, IRD.
- Malaria: Untersuchung im gabunischen Wald ein Film zum tierischen Ursprung der Malaria (16 min), IRD.
Verwandte Artikel
- Martin Shkreli und der Daraprim-Skandal
- Weltmalariatag
- Vogelmalaria
- Malariakontrolle
- Globaler Fonds zur Bekämpfung von AIDS, Tuberkulose und Malaria
- DNDi (Drugs for Neglected Diseases Initiative)
- Pontinische Sümpfe
- Atabrine
- Internationale Entwicklungsvereinigung
- Dichlordiphenyltrichlorethan
Externe Links
- Normdatensätze :
- Hinweise in allgemeinen Wörterbüchern oder Enzyklopädien :
- Gesundheitsbezogene Ressourcen :
- NCI Thesaurus
- Waisenkind
- (de) Internationale Klassifikation der Primärversorgung
- (de) Ontologie von Krankheiten
- (de) KrankheitenDB
- (en + es) Informationszentrum für genetische und seltene Krankheiten
- ( fr ) Mendelsches Erbe beim Menschen
- ( fr ) Mendelsches Erbe beim Menschen
- (de) Medizinische Schlagworte
- (de + es) MedlinePlus
- (cs + sk) WikiSkripta
- WER-Seite
- Malaria-Atlas-Projekt
- (de) Europäische BIOMALPAR-Site für Malaria