Kohlendioxid
| Kohlendioxid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Struktur von Kohlendioxid. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikation | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-Name | Kohlendioxid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyme |
Kohlendioxid, Kohlendioxid |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.004.271 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EG | 204-696-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-Code | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 280 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E290 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LÄCHELN |
C (= O) = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / CO2 / c2-1-3 InChIKey: CURLTUGMZLYLDI-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Das Auftreten | Verflüssigtes, farb- und geruchloses Druckgas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formel |
C O 2 [Isomere] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molmasse | 44.0095 ± 0.0014 g / mol C 27,29 %, O 72,71 %, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° Fusion | −78,48 ° C (Sublimation bei 760 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° Kochen | −56,6 ° C ( 5,12 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Löslichkeit | in Wasser bei 20 ° C : 88 ml / 100 ml unter 1 bar CO 2, d.h. 1,69 g / kg Wasser (3,35 g bei 0 ° C , 0,973 g bei 40 ° C und 0,576 g bei 60 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
1,87 kg m −3 ( Gas bei 15 ° C 1,013 bar ) dichter als Luft Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sättigungsdampfdruck |
5.720 kPa ( 20 ° C ) 569,1 mmHg ( –82 °C ); Gleichung:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamische Viskosität | 0,07 mPa·s bei −78 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritischer Punkt | 31,3 °C ; 72,9 atm und 0,464 g cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dreifacher Punkt | −56,6 ° C bis 5,11 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 3.840 × 10 −5 cal cm −1 s −1 K −1 bei 20 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 259 m s -1 ( 0 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 -Gas | -393,52 kJ mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
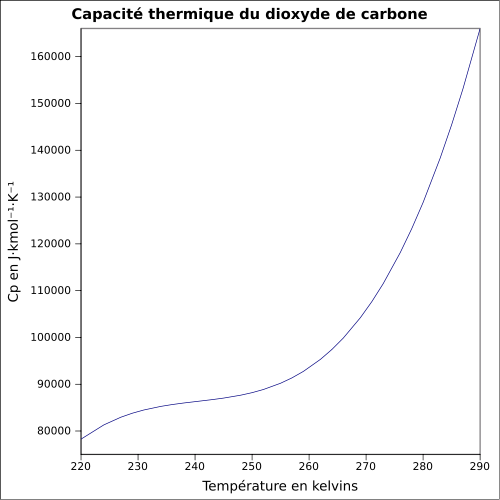
| C p |
Gleichung:
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 erneute Ionisationsenergie | 13,773 ± 0,002 eV (Gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallographie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallklasse oder Weltraumgruppe | P42 / mm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Netzparameter |
a = 3,535 Å b = 3,535 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumen | 51,73 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brechungsindex | 1.00045 (1 ATM ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vorsichtsmaßnahmen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Warnung H280 , P403 und P410 H280 : Enthält Gas unter Druck; kann bei Erwärmung explodieren P403 : An einem gut belüfteten Ort aufbewahren. P410 : Vor Sonnenbestrahlung schützen. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 ZU, A : Kritische Temperatur des komprimierten Gases = 31,1 °C Offenlegung bei 1,0% gemäß der Offenlegungsliste der Inhaltsstoffe ingredient |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : erstickendes Gas oder Gas, das kein Nebenrisiko darstellt UN-Nummer : 1013 : KOHLENDIOXID Klasse: 2.2 Klassifizierungscode: 2A : Verflüssigtes Gas, erstickend; Etikett: 2.2 : Nicht brennbare, nicht giftige Gase (entspricht den mit einem A oder einem großen O gekennzeichneten Gruppen); 
22 : tiefgekühlt verflüssigtes Gas, erstickend UN-Nummer : 2187 : gekühltes flüssiges Kohlendioxyd Klasse: 2.2 Klassifizierungscode: 3A : tiefgekühlt verflüssigtes Gas, erstickend; Etikett: 2.2 : Nicht entzündbare, nicht giftige Gase (entspricht den mit einem A oder einem großen O gekennzeichneten Gruppen); 
- UN-Nummer : 1845 : KOHLENDIOXID, FEST; oder CARBON SNOW Klasse: 9 Klassifizierungscode: M11 : Andere Stoffe, die beim Transport eine Gefahr darstellen, aber nicht der Definition einer anderen Klasse entsprechen. Tag: 9 : Verschiedene gefährliche Stoffe und Gegenstände  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Einheiten von SI und STP, sofern nicht anders angegeben. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Das Kohlendioxid , auch bekannt als Kohlendioxid oder Kohlendioxid ist eine anorganische Verbindung , deren chemische Formel ist CO 2, Das Molekül mit einer linearen Struktur der Form O = C = O . Es wird unter den Standardbedingungen für Temperatur und Druck präsentiert , wie ein Gas farblos, geruchlos, der Tang.
CO 2wird vom Anabolismus von Pflanzen verwendet , um Biomasse durch Photosynthese zu erzeugen , ein Prozess , der darin besteht , Kohlendioxid durch Wasser zu reduzieren , dank der von der Sonne empfangenen und vom Chlorophyll eingefangenen Lichtenergie , indem der Sauerstoff freigesetzt wird , um Monosaccharide und zunächst Glukose zu produzieren durch den Calvin-Zyklus . CO 2wird durch den Krebs-Zyklus durch den Katabolismus von Pflanzen , Tieren , Pilzen (Pilzen oder Pilzen ) und Mikroorganismen freigesetzt . Dieser Katabolismus besteht insbesondere darin, die Lipide und Kohlenhydrate Wasser und Kohlendioxid mit dem Sauerstoff der Luft zu oxidieren , um Kraft bzw. Reduktionskraft in Form von ATP und NADH + H + zu erzeugen . CO 2ist daher ein grundlegender Bestandteil des Kohlenstoffkreislaufs auf unserem Planeten. Es wird auch durch die erzeugte Verbrennung von fossilen Brennstoffen wie Kohle , Erdgas und Erdöl sowie durch die von allen organischen Stoffen im Allgemeinen. Es ist ein unerwünschtes Nebenprodukt in großtechnischen Prozessen.
Erhebliche Mengen CO 2werden auch von Vulkanen und anderen geothermischen Phänomenen wie Geysiren zurückgewiesen .
Im Januar 2021 enthielt die Erdatmosphäre 415,13 ppmv (parts per million by volume) CO 2, oder 0,04153%. Laut Eisbohrkernen aus der Antarktis betrug dieser Wert im Jahr 1839 283,4 ppmv , was einem Gesamtanstieg von etwa 46% in 182 Jahren entspricht.
CO 2ist ein wichtiges Treibhausgas , das im sichtbaren Licht transparent ist , aber im Infrarotbereich absorbiert , so dass es dazu neigt , die Rückemission der vom Boden aufgenommenen Wärmeenergie in den Weltraum unter der Einwirkung von Sonnenstrahlung zu blockieren . Es ist für rund 26% des Treibhauseffekts in der Erdatmosphäre verantwortlich ( Wasserdampf liefert 60%); seine Konzentration zu erhöhen , ist zum Teil verantwortlich für die Erwärmung über den Planeten in den letzten beobachteten Jahrzehnten des XX - ten Jahrhundert. Darüber hinaus ist die Versauerung könnte sich aus der Auflösung des atmosphärischen Kohlendioxids vor dem Ende der das Überleben vieler Meeresorganismen gefährden XXI ten Jahrhunderts.
Physikochemische Eigenschaften
Bei Atmosphärendruck sublimiert es bei -78,5 ° C (Wechsel vom festen in den gasförmigen Zustand), schmilzt jedoch nicht (Wechsel vom festen in den flüssigen Zustand).
Die flüssige Phase kann nur bei einem minimalen Druck von 519 kPa (also 5,12 atm ) und in einem Temperaturbereich von −56,6 °C ( Tripelpunkt ) bis maximal 31,1 °C bei 7,38 MPa (also 72,8 atm ) existieren ( kritisch Punkt ).
Sättigungsdampfdruck
|
| Übergang | Temperatur | Latente Hitze |
|---|---|---|
| Verdampfung | 0 ° C | 234,5 kJkg -1 |
| Verdampfung | -16,7 °C | 276,8 kJ kg -1 |
| Verdampfung | −28,9 °C | 301,7 kJkg -1 |
| Zusammenschluss | −56,6 °C | 199 kJkg -1 |
Es gäbe mindestens fünf feste molekulare Phasen (bestehend bei "niedrigem" Druck, weniger als 30 bis 60 GPa) und drei feste Polymerphasen (bei höheren Drücken) von CO 2. :
- molekulare Phasen:
- I: „Trockeneis“, bis 800 K und 11-12 GPa
- II: zwischen 400 und 5-600 K und einem Druck von 12 bis etwa 50 GPa
- III: über 12 GPA und weniger als 500 K
- IV: über 11 GPa und über 500 K
- VII: von 600 bis 900 K (bis 1000 K einschließlich des überkritischen Teils) und 11 bis 20 GPa
- Polymerphasen:
- V: über 30 GPa und über ca. 1.300 K
- VI: Temperatur zwischen ca. 500 K und 1300 K und Druck größer 30 (bei 1300 K) bei 50 GPa (bei 500 K)
- amorph, unter 500 K und über 50 GPa
Wässrige Löslichkeit
CO 2löst sich in Wasser und bildet Kohlensäure H 2 CO 3 : CO 2 (wässrig)+ H 2 O (l) H 2 CO 3 (wässrig), mit K h = [H 2 CO 3] / [CO 2] ≈ 1,70 × 10 -3 bis 25 ° C .
Es ist auch fettlöslich (löslich in Fettstoffen).
Kohlensäure ist nur mäßig stabil und zerfällt leicht in H 2 Ound CO 2. Wenn sich andererseits Kohlendioxid in einer basischen wässrigen Lösung (Soda, Pottasche usw.) löst, deprotoniert die Base Kohlensäure, um ein Hydrogencarbonat- Ion HCO . zu bilden-
3, auch Bicarbonat- Ion genannt , dann ein Carbonat- Ion CO2–
3. Auf diese Weise wird die Löslichkeit von CO 2wird erheblich gesteigert. Das Kaliumcarbonat K 2 CO 3hat zB eine Löslichkeit von 1,12 kg/l Wasser bei 20 °C .
So löst sich Kalkstein in Wasser im pH- Bereich, in dem das saure Hydrogencarbonat stabil ist, und erzeugt eine Lösung von Hydrogencarbonat (en) (von Calcium und Magnesium…). Es ist daher wahrscheinlich, dass es ausfällt, wenn das CO 2gelöst wird entgast, wie bei der Bildung von Stalagmiten und Stalaktiten . Kalkstein hat somit in Gegenwart von CO 2, eine Löslichkeit, die mit steigender Temperatur abnimmt, wie Gase und im Gegensatz zu den meisten Feststoffen (deren Löslichkeit im Allgemeinen mit der Temperatur zunimmt).
Unter bestimmten Bedingungen (hoher Druck + niedrige Temperatur) CO 2können in sogenannten Clathrat- Wasserkäfigen gefangen werden . Es ist eines der möglichen Mittel zur industriellen Abtrennung von CO 2in einem Vor- oder Nachverbrennungsgas enthalten . Es ist auch eines der geplanten Mittel zur CO 2 -Sequestrierungindustrielle oder geologische Speicherung untersucht, die möglicherweise mit korrelierten Meerwasserentsalzung (theoretisch kann es sogar für substituiert sein Methan - Hydrat Methan ).
Wissensgeschichte
Kohlendioxid ist eines der ersten Gase (zusammen mit Wasserdampf ), das als eine von der Luft verschiedene Substanz beschrieben wurde. Im XVII - ten Jahrhundert , der Chemiker und Arzt Flemish Jan Baptist van Helmont beobachtet , dass brennende Holzkohle in einem geschlossenen Gefäß, die Masse der resultierenden Asche ist geringer als die von Kohle. Seine Interpretation war, dass sich die fehlende Masse in eine unsichtbare Substanz verwandelt hatte, die er „ Gas “ oder spiritus sylvestre („wilder Geist“) nannte.
Die Eigenschaften von Kohlendioxid wurden in den 1750er Jahren von dem schottischen Chemiker und Physiker Joseph Black genauer untersucht . Er entdeckte, dass durch Erhitzen oder durch Gießen einer Säure auf Kalkstein (Gestein aus Kalziumkarbonat ) ein Gas freigesetzt wurde, das er "fixierte Luft" nannte und die damals noch gelehrte Theorie des Phlogistons untergrub . Er stellte fest, dass es dichter als Luft ist und weder eine Flamme noch das Leben eines Tieres ertragen kann. Black entdeckte auch, dass beim Einbringen von Kohlendioxid in eine Kalksteinlösung ( Calciumhydroxid ) ein Niederschlag von Calciumcarbonat entsteht. Er nutzte dieses Phänomen, um zu veranschaulichen, dass Kohlendioxid durch Tieratmung und mikrobielle Fermentation entsteht.
In 1772 , der englischen Chemiker Joseph Priestley veröffentlichte ein Werk mit dem Titel Imprägnier Wasser mit Fest Air , in dem er ein Verfahren beschrieben , Gießen Schwefelsäure (oder „Vitriolöl“ , wie es damals genannt wurde) auf Kreide. Zu produzieren , um Kohlenstoff Dioxid, dann zwangen Sie das Gas, sich in einer Schüssel mit Wasser aufzulösen. Er hatte gerade Sprudelwasser "erfunden" . Der Prozess wurde dann von Johann Jacob Schweppe übernommen, der 1790 in London eine Soda- Produktionsstätte namens Schweppes gründete .
In 1781 , das Französisch Chemiker Antoine Lavoisier die Tatsache hervorgehoben , dass dieses Gas das Produkt der ist Verbrennung von Kohlenstoff mit Sauerstoff .
Kohlendioxid wurde erstmals 1823 von Humphry Davy und Michael Faraday verflüssigt . Die erste Beschreibung des Kohlendioxids in der festen Phase wurde von Charles Thilorier (fr) geschrieben , der 1834 einen Druckbehälter mit verflüssigtem Kohlendioxidgas öffnete und feststellte, dass die Kühlung durch die schnelle Verdampfung der im "Schnee" erzeugten Flüssigkeit entsteht "CO 2.
Verwendet
Kohlendioxid wird in unterschiedlichen Formen für eine Vielzahl von Anwendungen in einem von großen Unternehmen wie Messer , Air Liquide und Air Products dominierten Markt vermarktet . Für die Lebensmittelindustrie wird der Benchmark-Standard in Europa von der European Industrial Gases Association (de ) herausgegeben. In Frankreich macht es 70 % des Verbrauchs aus.
Die Internationale Energieagentur hat im September 2019 einen Bericht über die Verwendung von CO 2 veröffentlicht, die er auf 230 Mt / Jahr schätzt , davon 130 Mt / Jahr für die Herstellung von Düngemitteln und 80 Mt / Jahr für die verstärkte Gewinnung von Öl und Erdgas. Ziel dieses Berichts ist es, ihr Potenzial zur Kompensation von CO 2 -Emissionen zu bewerten.. Er kommt zu dem Schluss, dass dieses Potenzial kurzfristig gering ist und langfristig viel niedriger bleiben wird als das der Abscheidung und Sequestrierung von Kohlendioxid ; Die vielversprechendsten Wege sind die Verwendung in Baumaterialien, bei der Herstellung von Polymeren und in Gewächshäusern.
In gasförmiger Form
CO 2 hat viele Verwendungsmöglichkeiten, darunter:
- Brände löschen : Viele Rechenzentren (Rechen-Serverräume) oder Archivräume sind mit einer Anlage ausgestattet, die im Brandfall den Raum mit CO 2 füllt die die Wirkung hat, das Feuer zu löschen;
- Schaumkomponente in kohlensäurehaltigen Getränken ;
- in Aquarien und Gewächshäusern für besseres Pflanzenwachstum;
- in Verpackungen mit kontrollierter Atmosphäre als neutralisierendes Element;
- in der Trinkwasserverteilung, verbunden mit Karbonat, um die Wasserhärte (TH) von übermäßig aggressivem Wasser zu erhöhen ;
- Löslichkeit von Kalkstein in hartem Wasser (TH größer als 25 ° F );
- Bierpumpen: Durch den Kontakt mit der Oberfläche des Bieres verhindert es seine Oxidation und verlängert seine Konservierung, im Gegensatz zu einem Kompressor, der (Umgebungs-)Luft verwendet;
- CO 2 wird manchmal auch verwendetin großen Schweineschlachthöfen, um sie vor dem Ausbluten zu betäuben; es wurde zur Konservierung von Fleisch verwendet ;
- für das Phänomen der Photosynthese notwendige Komponente, die das Wachstum der Pflanzen ermöglicht, indem sie anorganisches Material in organisches Material umwandelt und so ihr Holz bildet;
- Wärmeübertragungsflüssigkeit in bestimmten Typen von Kernreaktoren wie denen des UNGG- Sektors in Frankreich;
- es wird aufgrund seiner Diffusionsfähigkeit (Diffusionsfähigkeit) zur Bildung des Pneumoperitoneums bei Laparoskopien verwendet .
In flüssiger Form
In flüssiger Form wird es verwendet als:
- Kältemittel zum Einfrieren bestimmter Lebensmittel;
- Kältemittel in der Elektronikindustrie;
- Löschmittel in sogenannten "Kohlendioxid" -Feuerlöschern spricht man manchmal von Kohlendioxid-Schnee, weil ein Teil des CO 2 die Flüssigkeit verfestigt sich sofort beim Verlassen des Feuerlöschers und erzeugt ein weißes Pulver, das mit Kohlendioxidgas vermischt ist;
- Treibmittel (und manchmal auch Kohlensäure) für Getränke vom Fass.
Bei Verwendung als Kältemittel CO 2trägt die industrielle Nomenklaturbezeichnung "R744". Sein Einsatz als Kältemittel hat sich in den letzten Jahren tendenziell demokratischer entwickelt: Es gilt als „natürliches Kältemittel“ und sein Treibhauspotenzial ist im Vergleich zu „traditionellen“ Kältemitteln sehr gering.
Kohlendioxid liegt bei Atmosphärendruck nie in flüssiger Form vor. Es geht direkt von der festen in die gasförmige Form über ( Sublimation ).
In fester Form
Kohlendioxid in fester Form hat viele Namen: "Trockeneis", "Trockeneis", "Trockeneis", "Trockeneis". Es kommt aus der Verfestigung von CO 2flüssig. Es wird Trockeneis erhalten, das dann komprimiert wird, um Trockeneis zu erhalten.
In seiner festen Phase sublimiert dieses Trockeneis rückstandsfrei mit einer Sublimationsenthalpie von 573 kJ kg −1 (oder 25.2 kJ mol −1 ), bei −78.5 °C und 1 atm . Es fand daher schnell vielfältige Verwendungen als Kältemittel.
Es wird je nach Verwendung in verschiedenen Aufmachungen vermarktet:
- in Granulatform (Reiskorngröße 3 mm Durchmesser): hauptsächlich zum Reinigen und Tieftemperatur-Strippen ;
- in Stäbchen (ca. 16 mm lang ):
- für die Konservierung und den Transport von Produkten unter kontrollierter Temperatur (pharmazeutische Produkte, Transport von Tiefkühlkost, Transport von Proben usw.),
- bei Events: Das Trockeneis im Wasser bildet einen sehr dichten Nebel, der an den Wänden des Containers entlang gleitet;
- für Grundlagen- oder angewandte Forschung, zum Beispiel:
- in der Chemie als Kältemittel gemischt mit einem organischen Lösungsmittel (meist Aceton ) zur besseren Wärmeleitung, seltener als Reagenz. In diesem Bereich verwenden wir in Frankreich den Begriff „Carboglace“ oder in der gesprochenen Sprache nur „Carbo“ und niemals den Begriff „Trockeneis“, der in Quebec hingegen bevorzugt wird;
- zur Weinbereitung : verlangsamt die Gärung und verhindert die Oxidation ;
- in Blister oder Blöcken:
- für Luftversorgung ( Catering ), Caterer, Bestattungsunternehmen etc. ;
- im Brot:
- um dichten Nebel zu machen (Spezialeffekte, Kino, Video).
Festes Kohlendioxid ist auch in Form von Kohlendioxidschnee an den Polen des Planeten Mars vorhanden , wo es während des lokalen Winters die Eiskappen (meist bestehend aus Wasser) und deren Ränder bedeckt , sowie in Form von Kohlendioxid Eis in niedrigeren Breiten, späte Nacht in frühen lokalen Quellen (Fotos von Viking- Landern , dem Sojourner- Rover , dem Phoenix- Lander und zahlreichen HRSC- Bildern ). Am Südpol sind wichtige Lagerstätten geologisch sequestriert.
In überkritischer Phase
Über seinen kritischen Punkt hinaus tritt Kohlendioxid in eine Phase ein, die als überkritisch bezeichnet wird . Die Flüssig-Gas-Gleichgewichtskurve wird am kritischen Punkt unterbrochen, wodurch der überkritischen Phase ein Kontinuum physikalisch-chemischer Eigenschaften ohne Phasenänderung gewährleistet wird. Es ist eine Phase, die so dicht wie eine Flüssigkeit ist, aber Transporteigenschaften (Viskosität, Diffusion) gewährleistet, die denen eines Gases nahe kommen. Als grünes Lösungsmittel wird überkritisches Kohlendioxid verwendet, wobei die Extrakte frei von Lösungsmittelspuren sind.
In dieser Form dient es als:
- Mittel Extraktion :
- Entkoffeinierung von Kaffee ,
- Eliminierung von 2,4,6-Trichloranisol (TCA) aus mit Chlor (oder Hypochlorit) behandelten Korken, um dem Wein nach der Abfüllung keinen Korkgeschmack zu verleihen,
- Extraktion chemischer oder biologischer Verbindungen,
- Reinigung chemischer Verbindungen (Laufmittel in der Chromatographie , insbesondere in SFC );
- Transport- und Speichermittel bei der geologischen Sequestration von Kohlendioxid (in seltenen industriellen Anwendungen);
- Kühlmittel zur Mikronisierung von Wirkstoffen .
Nebenprodukt industrieller Prozesse
Es ist ein Nebenprodukt großtechnischer Prozesse. Ein Beispiel ist die Herstellung von Acrylsäure, die in einer Menge von über fünf Millionen Tonnen pro Jahr produziert wird. Die Herausforderung bei der Entwicklung dieser Prozesse besteht darin, einen geeigneten Katalysator und Prozessbedingungen zu finden, die die Produktbildung maximieren und die CO 2 -Produktion minimieren..
Reaktivität
Kohlendioxid ist ein sehr stabiles Molekül mit einer Standardbildungsenthalpie von −393.52 kJ mol −1 . Kohlenstoff hat eine positive Teilladung, die das Molekül schwach elektrophil macht . Ein Carbanion kann beispielsweise eine nukleophile Addition an CO 2 . durchführenund Bilden einer Carbonsäure nach der Hydrolyse. Außerdem CO 2kann durch Zugabe zu Epoxiden zur Bildung organischer Carbonate verwendet werden .
Schließlich CO 2beispielsweise reduziert werden kann Kohlenmonoxid durch Elektrochemie mit einem Redoxpotential von -0,53 V gegenüber der Standard - Wasserstoffelektrode oder durch Hydrierung .
Toxizität
Die Außenluft enthält 2019 etwa 0,04% CO 2 (412 ppm im Januar 2019).
Ab einer bestimmten Konzentration in der Luft ist dieses Gas wegen Erstickungsgefahr oder Übersäuerung gefährlich oder sogar tödlich , obwohl CO 2ist chemisch nicht giftig. Der Expositionsgrenzwert beträgt 3% über einen Zeitraum von 15 Minuten. Dieser Wert sollte niemals überschritten werden. Darüber hinaus sind die gesundheitlichen Auswirkungen umso gravierender als der CO 2 -Gehaltist gestiegen. Also bei 2% CO 2in der Luft nimmt die Atemamplitude zu. Bei 4% (oder dem 100-fachen der aktuellen Konzentration in der Atmosphäre) beschleunigt sich die Atemfrequenz. Bei 10 % können Sehstörungen, Zittern und Schwitzen auftreten. Bei 15% ist es plötzlicher Bewusstseinsverlust . Bei 25 % führt ein Atemstillstand zum Tod.
Das Einatmen von konzentriertem Kohlendioxid führt zu einer Blockierung der Ventilation, die manchmal als heftiges Strangulationsgefühl, Kurzatmigkeit, Atemnot oder Engegefühl in der Brust beschrieben wird und bei längerer Exposition schnell zum Tod führen kann.
Laut ANSES berichten Studien über „Konzentrationen, die mit intrinsischen gesundheitlichen Auswirkungen von CO 2 verbunden sind“(Schwelle bei ca. 10.000 ppm entsprechend dem Auftreten einer respiratorischen Azidose (Sinken des pH-Wertes im Blut), dem ersten kritischen Effekt von CO 2) “ . Eine respiratorische Azidose kann bereits bei 1% (10.000 ppm ) CO 2 . auftretenin der Luft, wenn ein gesunder Erwachsener mit mäßiger körperlicher Belastung dreißig Minuten oder länger atmet, und möglicherweise früher bei gefährdeten oder empfindlichen Personen. Diese Raten „sind höher als die behördlichen und/oder normativen Grenzwerte für die Lufterneuerungsqualität in Frankreich und international, die in der Regel zwischen 1.000 und 1.500 ppm CO2 schwanken . ". Eine kleine experimentelle Studie (mit 22 Erwachsenen) kam zu dem Schluss, dass CO 2 eine Wirkung hatzur Psychomotorik und intellektuellen Funktion (Entscheidungsfindung, Problemlösung) ab 1000 ppm (Studie von Satish et al. , 2012), diese Studie muss jedoch durch Studien mit höherer statistischer Power bestätigt werden. ANSES stellt fest, dass es letztlich nur wenige epidemiologische Studien zu diesem verbreiteten Gas gibt, einschließlich möglicher CMR-Wirkungen (krebserregend, erbgutverändernd und fortpflanzungsgefährdend).
Kohlendioxid ist ein farbloses und schweres Gas, das sich in Platten ansammelt und von einer unerfahrenen Person schwer zu erkennen ist.
In der Raumluft
Der Mensch verbringt immer mehr Zeit in einer geschlossenen Atmosphäre (ca. 80-90% der Zeit in einem Gebäude oder Fahrzeug). Laut ANSES und verschiedenen Akteuren in Frankreich ist die CO 2 -Ratein der Raumluft von Gebäuden (in Verbindung mit menschlicher oder tierischer Belegung und dem Vorhandensein von Feuerungsanlagen ), gewichtet nach der Lufterneuerung, liegt „normalerweise zwischen etwa 350 und 2.500 ppm “ .
In Wohnungen, Schulen, Kindergärten und Büros besteht kein systematischer Zusammenhang zwischen den CO 2 -Wertenund andere Schadstoffe und CO 2Innenräume sind statistisch kein guter Prädiktor für Schadstoffe, die mit dem Straßen- (oder Luftverkehr) im Freien verbunden sind. CO 2ist der Parameter, der sich am schnellsten ändert (mit der Hygrometrie und dem Sauerstoffgehalt, wenn Menschen oder Tiere in einem geschlossenen oder schlecht belüfteten Raum versammelt sind. In armen Ländern sind viele offene Feuerstellen CO 2 .- Quellenund CO direkt am Ort des Lebens emittiert. Oder bleiben Sie den ganzen Tag in der Luft mit einer CO 2 -RateDas Erreichen oder Überschreiten von 600 ppm beeinträchtigt unsere kognitiven Fähigkeiten (Denken, Denken, Erinnern, Entscheiden). Kleine Veränderungen des CO 2 -Gehalts, laut einer in Environmental Health Perspectives veröffentlichten Studiein der Luft wirken sich stark auf unser komplexes Denken und unsere Entscheidungsfähigkeit aus. Dieser Wert von 600 ppm wird oft in der Raumluft erreicht, wo er oft 1000 ppm überschreitet , mehrmals täglich mit beispielsweise einem durchschnittlichen Gehalt von 3110 mg/m 3 CO 2in den studierten Klassenzimmern; zu Lasten der Lernfähigkeit der Kinder).
Ein Sonderfall sind Sporthallen, in denen körperliche Anstrengung einen zusätzlichen Sauerstoffbedarf und eine CO 2 -Erhöhung mit sich bringt .von Spielern (und Zuschauern) abgelaufen. Zum Beispiel bei Eishockeyspielen , CO 2steigt während eines Spiels von 92 auf 262 ppm (meist von erwachsenen Männern gespielt). In der Mitte der Eisbahn wird der CO 2 -Wertbei jedem Spiel 1000 ppm überschreitet (vom Norwegischen Institut für öffentliche Gesundheit empfohlener Höchstwert). In-situ-Messungen zeigen, dass ein Spieler mit CO 2 angereicherte Luft atmetdass die Zuschauer und das CO 2sinkt während der Ruhezeiten und steigt während der Spielzeit. In der Nacht nach einem Spiel in einer geschlossenen Hockeyhalle dauert es fast ein Dutzend Stunden, bis der CO 2 .- Wert wieder erreicht istniedrig (600-700 ppm ), was immer noch über dem Normalwert liegt. Darüber hinaus sind in kalten, gemäßigten oder heißen Ländern viele Sporthallen klimatisiert; aus Gründen der Energieeinsparung haben sie keine ständige oder ausreichende Erneuerung der Außenluft. Bei einem Eishockeyspiel emittieren Frauen und Kinder weniger CO 2als Männer, aber im gleichen Raum, der Grad der Erhöhung des CO 2- Gehaltsin der Luft der Sporthalle ist vergleichbar, und in allen untersuchten Fällen verringert die Pause zwischen zwei Spielen nicht die CO 2- Konzentrationgenug, damit der Beginn der zweiten Periode genauso schwach ist wie der Beginn der ersten. Mit steigender Zuschauerzahl steigt der CO 2- Gehaltim Raum nimmt noch mehr zu. Auch die Anzahl der Öffnungen/Schließungen von nach außen führenden Türen beeinflusst die Lufterneuerung und damit den CO 2 -Gehalt.im Fitnessstudio. Studien haben eine Abnahme der kognitiven Leistung und der Entscheidungsfindung oder des Lernens gezeigt, wenn CO 2ist gestiegen. Nur wenige Studien haben sich auf die Wirkung dieses gleichen CO 2 . konzentriert auf die sportliche Leistung eines Einzelnen oder seines Teams.
In den UnterkünftenEs ist in der häuslichen Luft nicht reguliert; er muss jedoch an bestimmten geschlossenen Orten als „Indikator für den Einschluss und die Qualität der Lufterneuerung“ auf der Grundlage von Standards gemessen werden, die nach Ansicht der ANSES keine hygienische Grundlage haben.
In NichtwohngebäudenIn Frankreich, empfehlen die Abteilungs-Gesundheitsvorschriften (RSD) nicht die Schwelle von 1000 bis passieren ppm (parts per million) „unter normalen Belegungsbedingungen“, mit einer Toleranz von 1300 ppm an Orten , wo es verboten ist. Rauchen ( „ohne explizite Gesundheitsgrundlage für diese beiden Werte", so ANSES.
Ein Dekret von 5. Januar 2012schreibt die Überwachung der Luftqualität in Innenräumen in bestimmten Einrichtungen vor, die sensible Personen wie Kinder empfangen; sie schlägt die Berechnung eines "Einschlussindex" namens "Icone-Index" vor (vorgeschlagen vom Wissenschaftlich-Technischen Zentrum für Bauwesen (CSTB) auf der Grundlage der Häufigkeit der Überschreitung der CO 2 -Werte.verglichen mit zwei Schwellenwerten von 1000 und 1700 ppm in Klassenzimmern .
Am Arbeitsplatz ist das Thema Sicherheit und Prävention im Zusammenhang mit dem Risiko einer Kohlendioxidvergiftung ein wichtiges Anliegen, um das Risiko von Arbeitsunfällen zu begrenzen . Aufgrund fehlender epidemiologischer Daten wurde es jedoch in Frankreich als Indikator für die hygienische Qualität der Innenraumluft von der ANSES nicht als relevant erachtet , die hierfür keinen Richtwert für die Innenraumluftqualität (IGAI) liefert.
Bei hohen Konzentrationen von nahezu 50 bis 100 %, wie sie in künstlichen Kohlendioxid-Slicks am Arbeitsplatz vorkommen, kann es zu nervösem Erstaunen und sofortigem Bewusstseinsverlust kommen , gefolgt von einem schnellen Tod ohne fremde Hilfe. Diese Unfälle stellen ein hohes Risiko eines zweiten Unfalls dar , da Zeugen dem Opfer ohne Rücksicht auf ihre eigene Sicherheit zu Hilfe eilen und auch Opfer eines Rausches werden können.
CO 2 in der Erdatmosphäre
Kohlendioxid ist normalerweise nur in Spuren in der Erdatmosphäre vorhanden. Gemessen wird er über einen Index , der seit 1979 als „ Annual Greenhouse Gas Index “ (AGGI) von einem Netzwerk von rund hundert Stationen an Land und auf See von der Arktis bis zum Südpol bezeichnet wird.
Seit der industriellen Revolution , aufgrund der ständigen Verbrennung sehr großer Mengen fossilen Kohlenstoffs , während der Rückgang von Bränden , Wäldern und Vegetationsflächen weitergeht , sinkt der CO 2 . -Gehaltin der Luft steigt regelmäßig an (im Januar 2021: 415,13 Volumen- ppm , bzw. 632,96 Massen-ppm. Dies entspricht einer Gesamtmasse an CO 2atmosphärisch von etwa 3.258 × 10 15 kg (etwa dreitausend Gigatonnen ) . Dieser Gehalt betrug 1839 283,4 ppmv aus den Eisbohrkernen, die aus der Region Poinsett cap in der Antarktis entnommen wurden , was einer Gesamtzunahme von etwa 42% in 177 Jahren entspricht. Die CO 2 -Rateatmosphärisches erwartete am Ende des XXI ten Jahrhundert bei einer Temperatur zwischen 540 und 970 geschätzt wird ppmv von ausgewählten Simulationen (ISAM - Modell und Bern-CC - Modell). Das Jahr 1990 (entspricht einem Überschuss von ca. 2,1 W / m 2 gegenüber 1980 ) ist das Referenzjahr des Kyoto-Protokolls (es hat daher einen „AGGI-Index“ von 1). Eine eigene Forschungsgruppe zum Kohlenstoffkreislauf und zu Treibhausgasen wurde eingerichtet.
Zum Zeitpunkt t ist der CO 2 -Gehaltunterscheidet sich in jeder Hemisphäre, mit regelmäßigen jahreszeitlichen Schwankungen in jeder Hemisphäre (vgl. „Sägezahn“-Muster in der Grafik rechts, das einen Rückgang des CO 2 zeigtin Saison der Vegetation und eine Zunahme im Winter). Auch gibt es regionale Variationen, insbesondere auf der Ebene der atmosphärischen Grenzschicht , also in den bodennahen Schichten.
CO 2 -Werte sind im Allgemeinen in städtischen Gebieten und in Wohnungen höher (bis zum Zehnfachen des Hintergrundniveaus).
Kurz nach der Erdentstehung (lange vor dem Erscheinen des Lebens), als die Sonne fast halb so heiß war, stieg der Anfangsdruck von CO 2war etwa 100.000-mal höher als heute (30 bis 60 Atmosphären CO 2( d. h. 3.000.000 bis 6.000.000 Pascal), d. h. das 100.000-fache der aktuellen CO 2- Menge vor etwa 4,5 Milliarden Jahren).
Dann erschien Leben und Photosynthese , wobei das CO 2der Atmosphäre und des Wassers, um es in Karbonatgesteine und Kohle, Öl und Erdgas umzuwandeln , von denen ein Großteil tief in den Tiefen der Erde vergraben ist. Die CO 2 -Ratehat dennoch einige Spitzen von viel geringerer Bedeutung erlebt (zwanzigmal höher als heute vor etwa einer halben Milliarde Jahren, aber die Sonne war damals weniger heiß als heute (die Sonneneinstrahlung nimmt mit der Zeit zu und ist in den letzten vier Jahren um etwa 40% gestiegen) Milliarden Jahre) die CO-Rate. 2fiel während des Jura noch vier-fünfmal und sank dann langsam ab, außer in beschleunigter Weise während einer geologisch kurzen Episode, die als " Azolla-Ereignis " bekannt ist (vor etwa 49 Millionen Jahren).
Vulkanismus emittiert auch CO 2(bis zu 40% des von dem bestimmten emittierten Gas Vulkan während subaerial Eruptionen sind Kohlendioxid) und bestimmte heiße Quellen auch emittieren (beispielsweise auf dem italienischen Ort des Bossoleto nahe Rapolano Terme , wo in einer Vertiefung in der Form eines Becken etwa 100 m Durchmesser, in einer ruhigen Nacht, die CO 2kann in wenigen Stunden 75 % klettern, genug, um Insekten und kleine Tiere zu töten . Bei sonnigem Standort erwärmt sich die Gasmasse jedoch schnell und wird tagsüber durch die Konvektionsströmungen der Luft zerstreut. Lokal hohe Konzentrationen von CO 2, erzeugt durch die Störung des Wassers eines mit CO 2 gesättigten tiefen Seeskann auch töten (Beispiel: 37 Tote bei einer CO 2 -Eruptionvom Lake Monoun in Kamerun im Jahr 1984 und 1.700 Opfern rund um den Lake Nyos (auch Kamerun) im Jahr 1986.
CO 2 -Emissionendurch menschliche Aktivitäten verursacht werden, sind derzeit mehr als 130-mal höher als die von Vulkanen emittierten Mengen und beliefen sich 2007 auf fast 27 Milliarden Tonnen pro Jahr Die Staaten an zweiter Stelle produzieren 14% der weltweiten Gesamtmenge. Im Jahr 2016 meldete die UN-Meteorologie, dass die Konzentration von Kohlendioxid mit 403,3 ppm ein neues Allzeithoch erreichte und für den El Niño 2017 laut OMM ein Temperaturrekord gebrochen wurde, während mit 405 ppm der CO 2 So hoch war die Luft seit etwa 800.000 Jahren noch nie.
Globale CO 2 -Emissionenstieg 2018 um 2,7 %, der größte Anstieg seit sieben Jahren. In einem Bericht aus dem Jahr 2019 wurden die CO 2 -Konzentrationenerreichte 2018 407,8 ppm , ein Befund korrelierte auch mit dem Anstieg der Methankonzentrationen (CH 4) und Lachgas (N 2 O).
Pflanzennährstoff
Ein höherer CO 2- Gehaltstimuliert die Photosynthese und das Pflanzenwachstum mit potenziellen Vorteilen für die Produktivität von Getreidepflanzen, der weltweit wichtigsten Nahrungsquelle für Menschen und Nutztiere. Kohlenstoff, der von autotrophen Pflanzen durch Photosynthese aus Kohlendioxid in der Luft oder aus Bodenkohlenstoff gewonnen wird, ist in der Tat einer der Hauptnährstoffe im Nahrungsnetz . Die Zunahme der Biomasse ist ein Effekt simulierter Experimente, die eine 5-20%ige Steigerung des Ernteertrags bei 550 ppm CO 2 . vorhersagen. Blatt- Photosyntheseraten wurden in 30-50% C3 Pflanzen und 10-25% in C4 unter CO erhöhen gezeigten 2 Stufen verdoppelt.
Ab 2010 ergibt sich ein vollständigeres Bild mit signifikanten Unterschieden in den beobachteten Reaktionen für verschiedene Pflanzenarten, Wasserverfügbarkeit und Ozonkonzentration . Das Projekt Horsham Free-Air Concentration Enrichment ( FACE) 2007-2010 (unter Verwendung von Weizenkulturen) in Victoria, Australien, fand beispielsweise heraus, dass „die Wirkung von CO2 darin bestand, die Pflanzenbiomasse zu erhöhen Anthese 49%". Es hat sich gezeigt, dass ein Anstieg des atmosphärischen Kohlendioxids den Wasserverbrauch der Pflanzen und damit die Stickstoffaufnahme reduziert , was insbesondere den Ernteerträgen in Trockengebieten zugute kommt.
Erwartete Auswirkungen auf den Nährwert von Pflanzen
Wenn jedoch der Anstieg des CO 2 .- GehaltsAtmosphärisch fördert effektiv das Wachstum ( z. B. von Getreide ) aus noch ungeklärten Gründen, dann reduziert es den Nährwert der wichtigsten Grundnahrungsmittel (insbesondere Reis , Weizen und Kartoffeln ), indem es deren Proteingehalt , Spurenelemente und . reduziert B-Vitamine . Unter experimentellen Bedingungen ist der CO 2- Gehalterhöht (auch nicht in Verbindung mit erhöhter Temperatur) führt zu einem erhöhten Zuckergehalt bei Kulturpflanzen (Quelle für immer stärkere Alkohole für Trauben), aber auch durch Protein- und Mineralstoffmangel. Reis weist zudem oft hohe Arsenkonzentrationen auf , wodurch sich die Ansäuerung der Medien verschlimmern kann. Schließlich höhere Konzentrationen von CO 2die Versauerung von Süßwasser und die Versauerung der Ozeane verschärfen , was die Produktivität der Algen (und damit der Algenkultur ) beeinträchtigen könnte .
Aus diesem Grund ist laut einer aktuellen Studie (2018) von 2015-2050 der ungewöhnlich hohe CO 2- Gehaltunserer Atmosphäre könnten vor 2050 weltweit zu Krankheiten führen, die bei Menschen und bestimmten Nutztieren (Schweine, Kühe, Geflügel) durch Mangelernährung induziert werden. In einer in einer Sonderausgabe von PLOS Medicine veröffentlichten Studie zu Klimawandel und Gesundheit konzentrierten sich Christopher Weyant und seine Kollegen an der Stanford University auf zwei essentielle Mikronährstoffe , Zink und Eisen. Unter Berücksichtigung des Klimawandels und der Ernährungsgewohnheiten zeigen sie, dass sich das Krankheitsrisiko in den 137 Ländern verändern wird. Wenn nichts unternommen wird, steigt die CO 2 -Ratewird den Zink- und Eisengehalt in Lebensmitteln senken, was im Zeitraum 2015–2050 aufgrund einer Zunahme von Infektionskrankheiten , Durchfall und Fällen weltweit schätzungsweise 125,8 Millionen an Behinderungen angepasste Lebensjahre (95%-Konfidenzintervall [CrI] 113,6–138,9) kosten wird von Anämie , insbesondere in Südostasien und Afrika, wo die Bevölkerung bereits stark von Zink- und Eisenmangel betroffen ist. Besonders betroffen wären Kinder mit der Gefahr irreversibler Entwicklungsstörungen, die mit diesen Mängeln verbunden sind, die zumindest aus epigenetischen Gründen über mehrere Generationen hinweg vererbt werden können .
Die Studie von Weyant würde auch darauf hindeuten, dass die Ernährungsungleichheit zunehmen könnte, und würde zeigen, dass traditionelle Maßnahmen der öffentlichen Gesundheit (einschließlich der Ergänzung mit Mineralien und Vitaminen und einer verstärkten Kontrolle von Krankheiten bei Mensch und Tier) möglicherweise nicht ausreichen, um das Krankheitsphänomen einzudämmen. Tatsächlich würden solche Maßnahmen nur 26,6% (95% des CI 23,8–29,6) dieser gesundheitlichen, menschlichen und wirtschaftlichen Belastung reduzieren, während eine wirksame Strategie zur Verringerung der Treibhausgasemissionen den Treibhauseffekt, wie im Pariser Klimaabkommen vorgeschlagen , verhindern würde bis zu 48,2 % (95 % des CIF-Index 47,8–48,5) dieser Ladung.
Obwohl CO 2nährt das Wachstum von Pflanzen, sein Überschuss führt zu einer Verschlechterung ihres Nährwerts, die globale Folgen für alle Lebewesen haben wird, die Pflanzen konsumieren, einschließlich des Menschen. Die Autoren fordern eine bessere Untersuchung der Auswirkungen von erhöhtem CO 2atmosphärischen Einfluss auf andere Verbindungen pflanzlichen Ursprungs, die Auswirkungen auf die menschliche Gesundheit haben (z. B. Fettsäuren, Vitamine, pharmakologische Verbindungen, zumal in dieser Studie andere Folgen der CO 2, zu meteorologischen und biologischen Gefahren (erhöhte Plünderung etc.), zu Ernährungssicherheit, Zugang zu Nahrungsmitteln, deren Verwendung und Preisstabilität sowie zu räumlich und zeitlich verzögerten Folgenketten (Langzeitwirkungen insbesondere bei Unterernährung).
Die landwirtschaftlichen Erträge stagnieren oder verschlechtern sich in einem Teil der Welt insbesondere durch Erwärmung (Hitzewellen etc.) und veränderte Niederschlagsregime. Lebenswichtige Nutzpflanzen (insbesondere Weizen und Reis) sind bereits in tropischen und gemäßigten Zonen betroffen und prospektive Studien deuten darauf hin, dass Reis- und Maispflanzen allein aufgrund der erwarteten Temperaturerhöhungen in der Zone um 20 bis 40 % zurückgehen könnten. auch unter Berücksichtigung der Auswirkungen extremer Klimaereignisse. Dieser Kontext könnte dazu führen, dass die Lebensmittelpreise steigen und sie für die Ärmsten unerschwinglich werden, während der CO 2 -Gehalt in der Luft steigtkönnte auch die Nährwertqualität insbesondere von Getreide, das für die menschliche Gesundheit wichtig ist, und möglicherweise auch von Tieren (auch Milch- und Fleischquellen (und damit von Proteinen)) verringern , während auf See auch die Biomasse in Fischen abnimmt .
„Es ist noch nicht klar, ob der durch CO 2 . verursachte Rückgang des Nährwerts von Nahrungspflanzenlinear ist und die Ernährungsqualität aufgrund des CO2-Anstiegs seit Beginn der industriellen Revolution bereits abgenommen hat. "
Neben Maßnahmen zur Anpassung an den Klimawandel Maßnahmen zur Reduzierung der CO 2 -Emissionenund biologische Abscheidung von CO 2werden dringend benötigt. Einige Sorten , die in einem sich erwärmenden Klima weniger anfällig für Nährstoffdefizite sind, werden gesucht, schließen die Arbeit von Weyant und Kollegen.
Die Auswirkungen einer Erhöhung von CO 2auf Pflanzen sind besorgniserregender als dies von den ersten Modellen der 1990er und Anfang der 2000er Jahre vorhergesagt wurde Morgan et al. , auf der Grundlage von Labor- und In-situ- Experimenten bereits 2004 bestätigt, dass in entstandenen Ökosystemen CO 2Selbst dann , wenn sie die Produktivität in Bezug auf Biomasse verbessert, dennoch negative Auswirkungen haben , indem die modifizierende Zusammensetzung der Arten und durch die Verringerung der Verdaubarkeit von kurzen Gräsern beispielsweise in Steppen Vegetation ).
Treibhausgas und Säuerungsmittel
CO 2ist nach Wasserdampf das zweitwichtigste Treibhausgas in der Atmosphäre und trägt 26% bzw. 60% zu diesem Phänomen bei. Die Realität der seit dem letzten Jahrhundert auf planetarischer Ebene beobachteten globalen Erwärmung ist aus wissenschaftlicher Sicht nicht mehr umstritten, aber der genaue Anteil der Verantwortung von Kohlendioxid an diesem Prozess (insbesondere im Vergleich zu Methan ) muss noch geklärt werden, vor allem dank fossiler Aufzeichnungen von Paläoklimaten.
Darüber hinaus ist die Versauerung könnte sich aus der Auflösung von atmosphärischem Kohlendioxid das Überleben vieler Meeresorganismen gefährden vor dem XXI - ten Jahrhunderts, vor allem in Exoskelett verkalkt wie Korallen und Schalentiere , aber auch einige Fische.
Eine Reduzierung der anthropogenen Emissionen wird sowohl durch das Kyoto-Protokoll als auch durch die Richtlinie 2003/87/EG angestrebt ; seine langfristige geologische Sequestrierung ist Gegenstand der Forschung, aber eine umstrittene Lösung, wenn es um die einfache Injektion von CO 2 . geht in geologischen Schichten.
Ökosystemeffekte erhöhter CO 2 -Werte im Wasser und in der Luft
Im WasserCO 2hat eine gewisse eutrophische Wirkung (es ist ein Grundnährstoff , essentiell für Pflanzen), aber er ist auch ein Faktor bei der Versauerung der Ozeane und bestimmter Süßwasserkörper , die viele Arten (einschließlich bestimmter Mikroalgen und anderer Wasserpflanzen) negativ beeinflussen können Mikroorganismen, die durch kalkhaltige Strukturen geschützt sind, die Kohlensäure auflösen kann). Die Versauerung fördert auch die Freisetzung und Zirkulation und damit die Bioverfügbarkeit der meisten Schwermetalle , Metalloide oder Radionuklide (vor allem seit der industriellen Revolution natürlich in Sedimenten oder anthropogenen Ursprungs).
In der LuftDer Anstieg des CO 2 -Gehalts der Atmosphärekann je nach Häufigkeit, Umwelt- und biogeografischem Kontext sowie nach neueren Daten je nach Jahreszeit und jahreszeitlichen Schwankungen der Niederschläge (insbesondere über Wäldern) auch differenzierte oder sogar antagonistische Wirkungen haben ;
Unter Ökologen, die mit der Untersuchung der Auswirkungen des Klimawandels verbunden sind, besteht Konsens, dass über einen Anstieg von 2 ° C in einem Jahrhundert hinaus terrestrische und marine Ökosysteme ernsthaft beeinträchtigt werden.
Im Jahr 2013 ist die tatsächliche Reaktion der Ökosysteme auf CO 2und seine biogeographischen Modulationen gelten aufgrund zahlreicher " biogeochemischer Rückkopplungen " noch immer als komplex und müssen besser verstanden werden . Sie muss dennoch geklärt werden, wenn wir die planetarischen oder lokalen Kapazitäten von Ökosystemen im Hinblick auf die natürliche Kohlenstoffspeicherung und die Dämpfung der Auswirkungen des vom Menschen verursachten Klimawandels richtig einschätzen oder gar vorhersagen wollen .
Die durch den Wasserkreislauf vermittelten Rückkopplungen sind besonders wichtig und Niederschläge spielen eine große Rolle. Die Physiologie der Pflanzen hat mindestens eine bekannte Rolle; bis zu einem bestimmten Stadium (ab dem die Pflanze abstirbt), der Anstieg des CO 2- Gehaltsvon Luft verringert die stomatale Leitfähigkeit und erhöht die Effizienz der Wassernutzung durch Pflanzen (die Wassermenge, die benötigt wird, um eine Einheit Trockenmasse zu produzieren ), die Verringerung des Wasserverbrauchs führt zu einer größeren Verfügbarkeit von Bodenfeuchtigkeit. Es wurde im Jahr 2008 geschätzt, dass die Auswirkungen des steigenden CO 2in der Luft auf das Ökosystem sollte verschärft werden, wenn Wasser ein limitierender Faktor ist (aber auch Stickstoffeinträge sind zu berücksichtigen); dies wurde durch einige Experimente gezeigt, ist aber ein Faktor, der von vielen Studien "übersehen" wurde.
Dieser Zusammenhang scheint so stark zu sein, dass er es in gemäßigten Zonen ermöglicht, die jährlichen Schwankungen der Stimulierung der Luftbiomasse nach dem Anstieg des CO 2 -Gehalts genau vorherzusagen .in einem Mischgrünland mit Pflanzen der Typen C3 und C4 , basierend auf dem gesamten saisonalen Niederschlag ; der regnerische Sommer wirkt sich positiv aus, während Herbst und Frühjahr negative Auswirkungen auf die Reaktion auf CO 2 . haben. Die Wirkung steigender CO 2 -Werte wird daher hauptsächlich von den neuen Salden oder Ungleichgewichten abhängen, die zwischen Sommer und Herbst-/Frühlingsniederschlägen aufgestellt werden.
Die Verbindung zu Stickstoff (ein weiteres durch menschliche Aktivitäten gestörtes Element, einschließlich Emissionen aus industrieller Landwirtschaft, Industrie und Autoverkehr ) findet sich hier: Starke Niederschläge in kalten und nassen Jahreszeiten führen zu einer Einschränkung des Zugangs zu Fahrzeugen. Landpflanzen mit Stickstoff und daher reduzieren oder verbieten die Stimulierung von Biomasse durch einen CO 2- Gehalterzogen. Es wurde auch festgestellt , dass diese Vorhersage auch für Grundstücke gehalten „erwärmt“ von 2 ° C oder unbeheizten und war ähnlich für Pflanzen in C3 und Gesamtbiomasse, die die Meteorologen zu ermöglichen scheinen zu machen robust Vorhersagen. Auf den Antworten zu hohen CO 2 Konzentrationendes Ökosystems . Dies ist ein wertvolles Gut, da die Klimaprojektionen der hochauflösenden Modelle die sehr hohe Wahrscheinlichkeit großer Änderungen der jährlichen Niederschlagsverteilung bestätigen, selbst wenn sich die gesamte jährliche Niederschlagsmenge, die auf den Boden gefallen ist, nicht ändert. Diese wissenschaftlich bestätigten Daten (im Jahr 2013) sollten einige der Unterschiede erklären, die in den Ergebnissen von Experimenten aufgrund der Exposition von Pflanzen gegenüber erhöhten CO 2 -Werten auftraten., und Verbesserung der prospektiven Effizienz von Modellen, die die saisonalen Auswirkungen von Niederschlägen auf die Reaktion der Biodiversität auf CO 2 . nicht ausreichend berücksichtigten 14, besonders in Waldumgebungen.
CO 2 -Reduktion in der Luft
Es werden mehrere Wege erforscht oder umgesetzt, um die Ansammlung von CO 2 . zu begrenzenin der Luft. Sie können natürliche Prozesse wie die Photosynthese oder industrielle Prozesse beinhalten. Auch muss zwischen der Erfassung an der Quelle und der Erfassung in der Atmosphäre unterschieden werden.
Das Startup Indian Carbon Clean Solutions (CCSL) hat seine erste Anlage in Betrieb genommen, die 100 % CO 2 auffängt und wiederverwendet(60.000 Tonnen pro Jahr) aus einem kleinen Kohlekraftwerk in Indien in Chennai (Madras); dieses CO 2wird gereinigt und dann an einen lokalen Industriellen verkauft, der daraus Soda macht. CCSL-Technologie reduziert die CO 2 -Kostenin Indien mit 30 Dollar pro Tonne und in Europa oder den USA mit 40 Dollar weit unter dem Marktpreis verkauft: 70 bis 150 Dollar pro Tonne. Veolia hat mit CCSL einen Vertrag zur internationalen Vermarktung dieses Verfahrens unterzeichnet. Gleichzeitig will das Unternehmen Climeworks CO 2 durch Filtern der Umgebungsluft.
Das kanadische Unternehmen Carbon Engineering, das von dem Ingenieur David Keith gegründet und von Bill Gates und mehreren Öl- und Bergbauunternehmen finanziert wurde, hat einen Reaktor entwickelt, der CO 2 . extrahiertAtmosphäre zu geringeren Kosten als bestehende Erfassungstechnologien. Mit den von den Investoren bereitgestellten Mitteln wird dieser Direktabscheidungsprozess mit einem „Air to Fuels“-Prozess kombiniert, der es ermöglicht, den in der Atmosphäre gewonnenen Kohlenstoff in einen benzinähnlichen Kraftstoff umzuwandeln. In Zusammenarbeit mit Occidental Petroleum ist der Bau einer großen Anlage in Houston geplant . CO 2 -Sensorreaktorensind sehr energieintensiv und müssen daher mit erneuerbaren Energiequellen betrieben werden; der Scientific Council of the Academies of European Sciences (EASAC) hat Vorbehalte: Demnach ist die Eliminierung von CO 2 in der Luft wird den Klimawandel nicht verhindern und entspricht bisher nicht den IPCC-Empfehlungen.
Auf dem Weg zur Herstellung von „Solarmethan“ aus CO 2 ? .
Theoretisch die Umwandlung von CO 2in Kraftstoffen oder chemischen Rohstoffen würde den Einsatz fossiler Brennstoffe und den CO 2 -Ausstoß reduzieren.
Die elektrochemische Umwandlung aus erneuerbaren Stromquellen ist seit den 2010er Jahren Gegenstand vieler Forschungen.
Eine auf Photochemie basierende Hoffnung besteht darin, dass wir nur Sonnenlicht und umweltfreundliche Katalysatoren verwenden können, die auf der Erde billig und reichlich vorhanden sind. Unter den in der wissenschaftlichen Literatur der 2010er Jahre erwähnten Photokatalysatoren und molekularen Elektrokatalysatoren sind nur wenige stabil und selektiv für die Reduktion von CO 2 ; außerdem produzieren sie hauptsächlich CO oder HCOO, und Katalysatoren, die selbst geringe bis mäßige Ausbeuten stark reduzierter Kohlenwasserstoffe erzeugen können, bleiben selten.
Vier Forscher, darunter zwei Franzosen (Julien Bonin & Marc Robert), stellten einen Katalysator her, einen mit Trimethylammoniumgruppen funktionalisierten Eisentetraphenylporphyrin-Komplex , den sie (zum Zeitpunkt der Veröffentlichung) als den effizientesten und selektivsten für die Umwandlung von CO 2 . präsentierenin CO, weil es die Reduktion von acht Elektronen von CO 2 . katalysieren kannin Methan unter einfachem Licht, bei Umgebungstemperatur und -druck. Der Katalysator muss jedoch in einer Acetonitrillösung mit Photosensibilisator und Opferelektronendonator eingesetzt werden und arbeitet dann einige Tage stabil. CO 2wird zunächst hauptsächlich durch Photoreduktion in CO umgewandelt und bei zwei Reaktoren erzeugt CO dann Methan mit einer Selektivität von bis zu 82% und einer Quantenausbeute , d. h. einer Lichtausbeute, von 0 , 18%). Die Autoren glauben, dass andere molekulare Katalysatoren davon inspiriert werden könnten.
Denkbar sind auch Systeme der "Co-Katalyse" von molekularen Katalysatoren sowie Systeme auf Basis von Perowskit oder auf Basis von Komplexen von Übergangsmetallen .
Hinweise und Referenzen
- CARBON DIOXIDE , Sicherheitsdatenblatt(e) des International Program on Chemical Safety , eingesehen am 9. Mai 2009
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- „ Kohlendioxid “ , zur Gefahrstoffdatenbank (Zugriff am 8. März 2010 )
- Bernard M. und Busnot F. (1996), Usuel of General and Mineral Chemistry , Dunod, Paris, p. 229 .
- (en) Robert H. Perry und Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 S. ( ISBN 0-07-049841-5 ) , p. 2-50
- (in) WM Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 S. ( ISBN 978-1-4398-2077-3 ) , p. 14-40
- (in) Irvin Glassman und Richard A. Yetter, Combustion , Amsterdam / Boston, Elsevier,2008, 4 th ed. , 773 S. ( ISBN 978-0-12-088573-2 ) , p. 6
- (in) Carl L. Yaws, Handbook of Thermodynamic Diagrams , Vol. 2, No. 1-3, Huston, Texas, Golf Pub.,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 und 978-0-88415-859-2 )
- (in) David R. Lide, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 S. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- „ Kohlendioxid “ , auf www.reciprocalnet.org (Zugriff am 12. Dezember 2009 )
- Eintrag der CAS-Nummer "124-38-9" in die Chemikaliendatenbank GESTIS der IFA ( Deutsch , Englisch ), aufgerufen am 06.12.2008 (JavaScript erforderlich)
- SIGMA-ALDRICH
- " Kohlendioxid " in der Datenbank für chemische Produkte Reptox des CSST (Quebec-Organisation für Arbeitssicherheit und Gesundheitsschutz), abgerufen am 25. April 2009
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 S. , gebundenes Buch ( ISBN 978-1-4200-9084-0 ) , S. . 6-107
- Frédéric Datchi, " Das CO 2 -Molekülhält Druck besser aus als erwartet. » , Zum Institut für Mineralogie und Physik kondensierter Medien (IMPMC, Paris) ,April 2010(Zugriff am 28. Januar 2016 ) .
- T. Uchida, S. Mae, J. Kawabata und T. Hondoh, „Physical Data of CO 2Hydrate “ , in N. Handa und T. Ohsumi (dir), Direct Ocean Disposal of Carbon Dioxide , Terra Scientific Publishing Company (TERRAPUB),1995, 45-61 S. ( online lesen ).
- HS Chen, Die Thermodynamik und Zusammensetzung von Kohlendioxidhydraten , MS Thesis, Syracuse University, New York, 1972.
- H. Lee, C.-S. Lee, W.-M. Sung und S.-P. Kang, Hydrat-Phasengleichgewichte der Gastgemische mit CO 2 mixture, N2 und Tetrahydrofuran , Fluid Phase Equilib. , 2001, 185, 101
- P. Englezos, R. Kumar und J. Ripmeester, Der Gashydratprozess zur Abtrennung von CO 2aus Brenngasgemisch: Studien auf Makro- und Molekularebene , Proceedings of the 6th International Conference on Gas Hydrates (ICGH) , 2008
- P. Linga, R. Kumar und P. Englezos, Der Clathrathydratprozess zur Abscheidung von Kohlendioxid nach und vor der Verbrennung , J. Hazard. Mater. , 2007a, 149 (3), 625–629.
- NH Duc, F. Chauvy und J.-M. Herri, CO 2Einfangen durch Hydratkristallisation - Eine potenzielle Lösung für die Gasemission der Stahlindustrie , Energie. Konv. Verwalt. , 2007, 48, 1313–1322.
- Wassila Bouchafaa, Messung und Modellierung der Dissoziationsbedingungen von stabilisierten Gashydraten zur Anwendung auf die CO 2 -Abscheidung (Doktorarbeit der École Polytechnique), 22. November 2011
- YD Kim, HJ Lee, YS Kim und JD Lee, Eine Studie zur Entsalzung mit CO 2Hydrat - Technologie , Proceedings der 6. Internationalen Konferenz über Gashydrate (ICGH) 2008
- MD Max, K. Sheps, SR Tatro und LB Osegovic, Meerwasserentsalzung als nützlicher Faktor für CO 2sequestration , Proceedings of the 6th International Conference on Gas Hydrates (ICGH) , 2008
- Kap. I-4.3. Gleichzeitige Methanextraktion und CO 2 -Speicherung, s. 61 (bzw. S. 67 der [PDF] -Version ) der Dissertation von Nadia Mayoufi, Characterization of hydrate coulis with CO 2angewandt auf Kälteanlagen , Doktorarbeit, École Polytechnique, 8. Dezember 2010
- (in) „ Kohlendioxid: Sylvester Spiritus “ Ebbe Almqvist, Geschichte der Industriegase , Springer,2003, 472 S. ( ISBN 978-0-306-47277-0 , online lesen ), P.
- Sigaud de La Fond, Essay über verschiedene Arten von fester Luft oder Gas… , Paris, Chez P. Fr. Gueffier,1785( online lesen )
- (in) Joseph Priestley , „ Beobachtungen über verschiedene Arten von Luft “ , Phil. Übers. , Bd. 62,1772, s. 147–264 ( ISSN 0260-7085 , DOI 10.1098 / rstl.1772.0021 , online lesen )
- (in) Humphry Davy , „ Über die Anwendung der durch Kondensation von Gasen gebildeten Flüssigkeiten als mechanische Mittel “ , Phil. Übers. , Bd. 113,1823, s. 199–205 ( ISSN 0261-0523 , DOI 10.1098 / rstl.1823.0020 , online lesen [PDF] )
- (de) Charles Thilorier, " Verfestigung von Kohlensäure " , CR Hebd. Akad.-Sitzungen. Wissenschaft , Bd. 1,1835, s. 194-196 ( online lesen )
- (in) HD Roller Duane , „ Thilorier zuerst und die Verfestigung eines permanenten Gases (1835) “ , Isis , vol. 43, n o 21952, s. 109–113 ( ISSN 0021-1753 , DOI 10.1086 / 349402 )
- Dominique Pialot, „ CO2, ein neuer Markt? » , Auf latribune.fr ,17. Juni 2019(Zugriff am 6. August 2019 ) .
- (in) " Kohlendioxid Lebensmittel- und Getränkequalitätsquellenqualifizierung, Qualitätsstandards und Verifizierung: EIGA Doc 70/17 " auf eiga.eu ,2016(Zugriff am 12. Juli 2019 ) .
- (de) CO2 nutzen – aus Emissionen Mehrwert schaffen , Internationale Energieagentur , im September 2019.
- Neil A. Campbell und Jane B. Reece , Biologie , Erpi,2007, 1.400 S.
- Carboglace ist eine in Frankreich von Air Liquide eingetragene Marke
- von Baczko, K., Hrsg. Gmelins Handbuch der Anorganischen Chemie: Kohlenstoff , 8 th ed. , Chemie GMBH, Weinheim / Bergstr., 1970, Teil C. Abschnitt 1, S. 1 413–416 .
- Phillips, RJ, Davis, BJ, Tanaka, KL, Byrne, S., Mellon, MT, Putzig, NE, ... & Smith, IB (2011) Massive CO2-Eisablagerungen in den südpolaren geschichteten Ablagerungen des Mars . Wissenschaft, 332 (6031), 838-841.
- (in) " Das Reaktionsnetzwerk in der Propan-Oxidationsstufe über reinen MoVTeNb-M1-Oxidkatalysatoren " , Journal of Catalysis , Vol. 2, No. 311,2014, s. 369-385 ( online lesen )
- (in) " Oberflächenchemie der reinen Oxidphase M1 MoVTeNb während des Betriebs bei der selektiven Oxidation von Propan zu Acrylsäure " , Journal of Catalysis , Vol. 2, No. 285,2012, s. 48-60 ( online lesen )
- (in) Kinetische Studien der Propanoxidation sind Mo- und V-Mischoxidkatalysatoren ,2011( online lesen )
- (in) " Multifunktionalität von kristallinen MoV (NBPT) M1-Oxidkatalysatoren bei der selektiven Oxidation von Propan und Benzylalkohol 3 (6) " , ACS Catalysis , vol. 3, n o 6,2013, s. 1103-1113 ( online lesen )
- (in) Colin Finn , Sorcha Schnittger Lesley J. Yellowlees und Jason B. Love , „ Molekulare Ansätze zur elektrochemischen Reduktion von Kohlendioxid “ , Chemical Communications , vol. 48, n o 10,2012, s. 1392-1399 ( PMID 22116300 , DOI 10.1039 / c1cc15393e ).
- (de) CO2.erde Konzentration von CO 2 in der Erdatmosphäre.
- Vergiftung durch Einatmen von Kohlendioxid , Medizinisch-technische Akte 79, INRS, 1999.
- CO 2 -Konzentrationen in Innenraumluft und Auswirkungen auf die Gesundheit, ANSES-Gutachten, Sammelgutachten, ANSES, 2013/07, 294 S.
- Indoor Air Quality Observatory (Oqai), Ministerium für Ökologie, Ademe, CSTB, AirParif, Atmo ...
- (in) Chatzidiakou, L. Mumovic, D., & Summerfield, A. (2015). Ist CO 2ein guter Proxy für die Raumluftqualität in Klassenzimmern? Teil 1: Die Zusammenhänge zwischen thermischen Bedingungen, CO2-Werten, Lüftungsraten und ausgewählten Innenraumschadstoffen. Gebäudetechnik, Forschung und Technologie, 36 (2), 129-161 ( Abstract ).
- (in) Cetin Sevik M & H (2016) Indoor-Qualitätsanalyse von CO2 für die Kastamonu University . In Conference of the International Journal of Arts & Sciences (Vol. 9, Nr. 3, S. 71).
- (in) Jaber AR Dejan Marcella M & U (2017) The Effect of Indoor Temperature and CO2 Levels is Cognitive Performance of Adult Women in a University Building in Saudi Arabia , Energy Procedia , 122, 451-456.
- (in) Myhrvold AN, Olsen S & Lauridsen O Innenraumumgebung in Schulen, Schülern und Gesundheitsleistung in Bezug auf CO2-Konzentrationen , Indoor Air , 96 (4), 369-371, 1996
- (en) Prestmo LS (2018) Messungen von Raumklimaparametern in der Trainingszone einer Eishockeyhalle (Masterarbeit, NTNU).
- (in) Prestmo LS (2018) Messungen von Raumklimaparametern im Übungsbereich einer Eishockeyhalle (Masterarbeit, NTNU) (siehe Kapitel 7.2 Erhöhte CO 2 Konzentration während eines Spiels)
- (in) Ex: Kenneth W. Rundell (2004) „Lungenfunktionsverfall bei Eishockeyspielerinnen: Gibt es einen Zusammenhang mit der Luftqualität der Eisbahn? " Inhalationstoxikologie , 16 (3): 117–123
- Vergiftung durch Einatmen von Kohlendioxid , Medizinisch-technisches Dossier 79 TC 74, INRS
- D Dr. Pieter Tans (3. Mai 2008) Jährliches CO 2Molenbrucherhöhung (ppm) für 1959–2007 , National Oceanic and Atmospheric Administration , Earth System Research Laboratory , Global Monitoring Division ( weitere Details .)
- NOAA / Law Dome
- NOAA / Mauna Loa
- Klimaforschungseinheit (Univ. East Anglia)
- Solar Influences Data Analysis Center (SIDC)
- http://advances.sciencemag.org/content/3/1/e1601207
- Trends in Atmospheric Carbon Dioxide - Global Monthly Mean CO2 , National Oceanic & Atmospheric Administration (NOAA) - Earth System Research Laboratories (ESRL), abgerufen am 25. April 2021.
- (in) Kohlendioxid-Informationsanalysezentrum, im Juni 1998 , „ Historisches CO 2Aufzeichnung abgeleitet aus einem Spline-Fit (20-Jahres-Cutoff) der Law Dome DE08 und DE08-2 Eisbohrkerne “, DM Etheridge, LP Steele, RL Langenfelds, RJ Francey (Division of Atmospheric Research, CSIRO, Aspendale, Victoria, Australien), J.-M. Barnola ( Labor für Glaziologie und Umweltgeophysik , Saint-Martin-d'Hères , Frankreich) und VI Morgan (Antarctic CRC and Australian Antarctic Division, Hobart, Tasmanien, Australien)
- (in) Umweltprogramm der Vereinten Nationen (UNEP) - Dritter Sachstandsbericht Klimawandel 2001 , " Klimawandel 2001: Arbeitsgruppe I: Die wissenschaftliche Grundlage - Kapitel 3. Der Kohlenstoffkreislauf und atmosphärisches Kohlendioxid " Zusammenfassung
- Unser Planet Info, CO 2 -Gehaltvon 1990 bis 2004 stark angestiegen (Zugriff am 31. März 2012)
- Globale Überwachungsabteilung von ESRL
- Forschungsgruppe Treibhausgase im Kohlenstoffkreislauf
- Atmosphere Dossier , Pour la science , Juni 1996
- Earth Guide / UCSD, Klima und CO 2in the Atmosphere (Zugriff am 10. Oktober 2007)
- Robert A. Berner und Zavareth Kothavala, GEOCARB III: Ein überarbeitetes Modell des atmosphärischen CO 2über Phanerozoikum [PDF] , American Journal of Science , vol. 301, 2001, S. 2, S. 182-204, DOI : 10.2475 / ajs.301.2.182 (Zugriff am 15.02.2008 )
- Sigurdsson, Haraldur und Houghton, BF, Enzyklopädie der Vulkane , 2000, Academic Press, San Diego ( ISBN 0-12-643140-X )
- van Gardingen, PR; Grace, J.; Jeffree, CE; Byari, SH; Miglietta, F.; Raschi, A.; Bettarini, I., Kap. Langzeiteffekte von erhöhtem CO 2Konzentrationen am Blattgasaustausch: Forschungsmöglichkeiten mit CO 2Federn , Herausgeber: Raschi, A.; Miglietta, F.; Tognetti, R.; van Gardingen, PR (Hrsg.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , p. 69-86
- Martini M., Kap. CO 2Emissionen in vulkanischen Gebieten: Fallgeschichten und Gefahren , in Pflanzenreaktionen auf erhöhten CO 2: Nachweise aus natürlichen Quellen , Herausgeber: Raschi, A.; Miglietta, F.; Tognetti, R.; van Gardingen, PR (Hrsg.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , p. 69-86
- Die vulkanischen Gase und ihre Auswirkungen (in) , abgerufen am 07.09.2007
- Martin Wolf, " Klimawandel-Skeptiker verlieren an Boden ", auf The New Economist ,17. Juli 2014(Zugriff am 26. Juli 2014 ) .
- " Immer mehr CO 2in der Atmosphäre ”, La Croix ,30. Oktober 2017( ISSN 0242-6056 , online gelesen , abgerufen am 31. Oktober 2017 )
- Gamilloaug E., Atmosphärischer Kohlenstoff im letzten Jahr erreichte Werte wie seit 800.000 Jahren nicht mehr gesehen , Science News , 2. August 2018
- " Globale CO 2 -Emissionen„rutschte“ im Jahr 2018 mit + 2,7% “ , auf Liberation.fr (abgerufen am 6. Dezember 2018 )
- „ CO2 “ .
- Lobell DB & Field CB (2008) Abschätzung des Kohlendioxids (CO 2) Düngeeffekt durch Wachstumsratenanomalien von CO 2und Ernteerträge seit 1961 . Glob Chang Biol. ; 14 (1): 39–45.
- FN Tubiello , JF Soussana und SM Howden , „ Reaktion von Feldfrüchten und Weiden auf den Klimawandel “,2007( PMID 18077401 , PMCID 2148358 , DOI 10.1073 / pnas.0701728104 , Bibcode 2007PNAS..10419686T ) ,p. 19686–19690
- (in) Rob Norton et al .. Die Wirkung von erhöhtem Kohlendioxid auf Wachstum und Ertrag von Weizen im Australian Grains Free Air Carbon Dioxide Enrichment (AGFACE) Experiment , regional.org.au 2008
- (in) Daniel R. Taub, Auswirkungen steigender atmosphärischer Kohlendioxidkonzentrationen einer Pflanze , Natur , Bildung Wissen 3 (10): 21, 2010
- (in) Taub DR, Miller B, Allen H. Auswirkungen von erhöhtem CO2 auf die Proteinkonzentration von Nahrungspflanzen: eine Metaanalyse , Global Change Biology 1. März, 14 (3): 565-75, 27. November 2007
- (de) Myers SS Zanobetti A, Kloog I, P Huybers, Leakey AD, Bloom AJ, et al. (2014), Zunehmendes CO2 bedroht die menschliche Ernährung. Natur . Juni; 510 (7503): 139.
- (in) Zhu C, Kobayashi K, Loladze I, Zhu J, Jiang Q, Xu, et al. (2018), Kohlendioxid (CO2) in diesem Jahrhundert wird den Protein-, Mikronährstoff- und Vitamingehalt von Reiskörnern mit möglichen gesundheitlichen Folgen für die ärmsten von Reis abhängigen Länder verändern , Sci Adv. 2018: 4: eaaq1012.
- (in) Loladze I (2014) Versteckte Verschiebung des Ionoms von Pflanzen, die erhöhten CO2-abgereicherten Mineralien als Grundlage der menschlichen Ernährung ausgesetzt sind , Elifa . ; 3: e02245.
- (in) Andrew A. Meharg, Jeanette Hartley-Whitaker (2002)Arsenaufnahme und -metabolismus bei arsenresistenten und nicht resistenten Pflanzenarten, gepostet am 4. April 2002 DOI: 10.1046 / j.1469-8137.2002.00363.x Issue New Phytologist , Band 154, Ausgabe 1, Seiten 29–43, April 2002
- (en) Ebi KL, Ziska LH (2018) Anstieg des atmosphärischen Kohlendioxids: Erwartete negative Auswirkungen auf die Lebensmittelqualität. PLoS Med 15 (7): e1002600. https://doi.org/10.1371/journal.pmed.1002600 ; Studie veröffentlicht unter der Creative Commons CC0 Public Domain License
- (in) Helena Bottemiller evich, " Der große Nährstoffkollaps " , Politico ,13. September 2017( online lesen , eingesehen am 13. September 2017 ).
- (in) Weyant C Brandeau ML, Burke M, DB Lobell, Bendavid S & S Basu (2018), Erwartete Belastung und Mitigation von Kohlendioxid-induzierten Ernährungsdefizienzen und verwandten Krankheiten: eine Simulationsmodellierungsstudie, PLoS Med. ; 15 (7): e1002586
- Vickers MH (2014) Ernährung im frühen Leben, Epigenetik und Programmierung von Krankheiten im späteren Leben . Nährstoffe. 2. Juni, 6. (6): 2165–78.
- C. Zhu, Q. Zeng, A. McMichael, KL Ebi, K. Ni, AS Khan et al. (2015) Historische und experimentelle Beweise für eine erhöhte Konzentration von Artemesinin, einer globalen Anti-Malaria-Behandlung, mit dem jüngsten und prognostizierten Anstieg des atmosphärischen Kohlendioxids . Klimawandel. 1. September; 132 (2): 295–306
- Porter JR, Xie L, Challinor AJ, Cochrane K, Howden SM, Iqbal MM, et al. (2014) Ernährungssicherheit und Lebensmittelproduktionssysteme . In: Klimawandel 2014: Auswirkungen, Anpassung und Vulnerabilität. Teil A: Globale und sektorale Aspekte. Beitrag der Arbeitsgruppe II zum Fünften Sachstandsbericht des Zwischenstaatlichen Ausschusses für Klimaänderungen [Field CB, Barros VR, Dokken DJ, Mach KJ, Mastrandrea MD, et al. (Hrsg.)]. Cambridge University Press, Cambridge, Vereinigtes Königreich und New York, NY, USA, S. 485–533
- Battisti DS & Naylor RL (2009) Historische Warnungen vor zukünftiger Ernährungsunsicherheit mit beispielloser saisonaler Hitze . Wissenschaft 323, 240–244.
- (in) Nowak RS, SD Ellsworth DS und Smith (2004), Funktionelle Reaktionen von Pflanzen auf erhöhtes atmosphärisches CO 2- Unterstützen Photosynthese- und Produktivitätsdaten aus FACE-Experimenten frühe Vorhersagen? , Neues Phytol. , 162, 253–280 ( Zusammenfassung )
- (in) Morgan JA et al. (2004), CO 2steigert die Produktivität, verändert die Artenzusammensetzung und verringert die Verdaulichkeit der Steppenvegetation von Kurzgras , Ecol. Appl. , 14, 208–219
- (in) JT Kiehl und Kevin E. Trenberth, " Das jährliche globale mittlere Energiebudget der Erde " , Bulletin der American Meteorological Society , vol. 78, n o 2Februar 1997, s. 197-208 ( DOI 10.1175 / 2008BAMS2634.1 , online lesen )
- (in) Klimawandel: Woher wissen wir das? , NASA, undatiert
- (de) Emmanuel Quiroz, Temperatur und CO 2In Ice Core Records gefundene Korrelationen , undatiert
- (in) Bärbel Hönisch Andy Ridgwe Daniela N. Schmidt, Ellen Thomas, Samantha J. Gibbs, Appy Sluijs, Richard Zeebe, Lee Kump, Rowan C. Martindale, Sarah E. Greene, Wolfgang Kiessling, Justin Ries, James C. Zachos , Dana L. Royer, Stephen Barker, Thomas M. Marchitto Jr. , Ryan Moyer, Carles Pelejero Patrizia Ziveri, Gavin L. Foster und Branwen Williams, „ The Geological Record of Ocean Acidification “ , Science , vol. 335, n o 6072, 2. März 2012, s. 1058-1063 ( DOI 10.1126 / science.1208277 , online lesen )
- (in) Joe Romm, Geological Society: Säuernde Ozeane bedeuten einen biologischen Zusammenbruch der Meere "bis zum Ende des Jahrhunderts" , Klimafortschritt , 31. August 2010
- (en) C. Langdon und J. Atkinson, " Effekt von erhöhtem p CO 2zur Photosynthese und Verkalkung von Korallen und Wechselwirkungen mit jahreszeitlichen Veränderungen der Temperatur/Bestrahlungsstärke und Nährstoffanreicherung “ , Journal of Geophysical Research , vol. 110,7. September 2005, C09S07 ( DOI 10.1029 / 2004JC002576 , online lesen )
- (in) Katharina E. Fabricius, Chris Langdon, Sven Uthicke Craig Humphrey, Sam Noonan, Glenn De'ath, Remy Okazaki, Nancy Muehllehner, Martin S. Glas und Janice M. Lough, „ Losers and winners in coral reefs acclimatized to erhöhte Kohlendioxidkonzentrationen ” , Nature Climate Change , vol. 1,29. Mai 2011, s. 165-169 ( DOI 10.1038 / nclimate1122 , online lesen )
- (in) Joe Romm, Kohlendioxid macht Fische verrückt und bedroht ihr Überleben, Studienergebnisse , Klimafortschritt , 23. Januar 2012.
- Sebastian Leuzinger und Christian Korner, „Die Niederschlagsverteilung ist der Haupttreiber des Abflusses unter zukünftigem CO 2-Konzentration in einem gemäßigten Laubwald ”, Glob. Biol. ändern , Bd. 16,2010, s. 246–254 ( Zusammenfassung )
- Peters, GP et al. , Die Herausforderung, die globale Erwärmung unter 2 ° C zu halten , Nature Clim. Änderung , 3, 4–6, 2013
- Reich PB und Hobbie SE (2013), Jahrzehntelange Bodenstickstoffbeschränkung auf das CO 2Düngung pflanzlicher Biomasse , Nature Clim. Ändern , 3, 278-282 ( Zusammenfassung )
- Mark J. Hovenden, Paul CD Newton und Karen E. Wills, „ Saisonaler, nicht jährlicher Niederschlag bestimmt die Reaktion der Graslandbiomasse auf Kohlendioxid “, Nature , vol. 511,2014( DOI 10.1038 / nature13281 , Zusammenfassung )
- Sokolov AP et al. (2008), Konsequenzen der Betrachtung von Kohlenstoff-Stickstoff-Wechselwirkungen auf die Rückkopplungen zwischen Klima und dem terrestrischen Kohlenstoffkreislauf , J. Clim. , 21, 3776–3796 ( Zusammenfassung und Bibliographie )
- Morgan J. et al. (2011), C4-Gräser gedeihen, da Kohlendioxid die Austrocknung in erwärmten Halbtrockenrasen beseitigt , Nature , 476, 202–205 ( Zusammenfassung )
- (de) Leakey A. et al. (2009), Erhöhter CO 2Auswirkungen auf die Kohlenstoff-, Stickstoff- und Wasserbeziehungen von Pflanzen: sechs wichtige Lehren aus FACE , J. Exp. Bot. , 60, 2859–2876 ( Zusammenfassung )
- (in) McMurtrie, RE et al. (2008), Warum reagiert das Pflanzenwachstum auf erhöhtes CO 2verstärkt, wenn Wasser limitierend ist, aber reduziert, wenn Stickstoff limitierend ist? Eine Wachstumsoptimierungshypothese , Funct. Pflanzenbiol. , 35, 521-534
- PB Reich, SE Hobbie, T. Lee et al. , " Stickstofflimitierung schränkt die Nachhaltigkeit der Reaktion des Ökosystems auf CO 2 ein », Natur , vol. 440,2006, s. 922–925 ( Zusammenfassung )
- PB Reich, BA Hungate und Y. Luo, „ Kohlenstoff-Stickstoff-Wechselwirkungen in terrestrischen Ökosystemen als Reaktion auf steigendes atmosphärisches Kohlendioxid “, Annu. Rev. Schule. Entwicklung Syst. , Bd. 37,2006, s. 611-636 ( Zusammenfassung )
- J. A. Morgan, DE Pataki, C. Körner et al. , " Wasserbeziehungen in Grünland- und Wüstenökosystemen, die einem erhöhten atmosphärischen CO 2 . ausgesetzt sind », Ökologie , vol. 140,2004, s. 11–25 ( online lesen [PDF] )
- (de) Derner JD et al. , Über- und unterirdische Reaktionen von C3-C4-Speziesmischungen auf erhöhtes CO 2und Bodenwasserverfügbarkeit , Glob. Biol. ändern , 9, 452–460, 2003
- (de) Dukes JS et al. (2005), Reaktionen der Grünlandproduktion auf einzelne und mehrere globale Umweltveränderungen , PLoS Biol. , 3, 1829–1837 ( Zusammenfassung
- Grünzweig JM und Korner C. (2001), Wachstum, Wasser- und Stickstoffverhältnisse in Graslandmodellökosystemen des semi-ariden Negev of Israel, exponiert zu erhöhtem CO 2, Ökologie , 128, 251–262 ( Zusammenfassung )
- (en) Marissink M., Pettersson A. und Sindhoj E. (2002) Oberirdischer Pflanzenertrag unter erhöhtem Kohlendioxidgehalt in einem schwedischen naturnahen Grünland , Agric. Ökosystem. Über. , 93, 107–120 ( Zusammenfassung )
- (in) Singh D., Tsiang M., B. und Rajaratnam Diffenbaugh NS (2013) Niederschlagsextreme über den kontinentalen Vereinigten Staaten in einem transienten, hochauflösenden, gesamten Klimamodellexperiment , J. Geophys. Res. , D 118, 7063–7086 ( Zusammenfassung )
- (in) Piao S. et al. (2013), Evaluierung terrestrischer Kohlenstoffkreislaufmodelle hinsichtlich ihrer Reaktion auf Klimavariabilität und auf CO 2Trends , Globus. Biol. ändern , 19, 2117–2132 ( Zusammenfassung )
- (in) De Kauwe MG et al. (2013), Waldwassernutzung und Wassernutzungseffizienz bei erhöhtem CO 2: ein Modell-Daten-Vergleich an zwei kontrastierenden FACE-Standorten gemäßigter Wälder , Glob. Biol. ändern , 19, 1759–1779 ( Zusammenfassung )
- " Das Start-up CCSL und Veolia werden das CO 2 auffangen und weiterverkaufenim großen Stil " ,30. März 2017.
- Von Bill Gates unterstütztes kanadisches Unternehmen will CO 2 abfangenin der Luft , Le Figaro , 29. Juni 2019.
- (in) Richard Littlemore, "Kann dieses Unternehmen BC-Anteil an der Lösung des Klimawandels sein?" , The Globe and Mail , Bericht im Wirtschaftsmagazin , Oktober 2019
- Bonin J, Maurin A & Robert M (2017) Molekulare Katalyse der elektrochemischen und photochemischen Reduktion von CO 2mit Komplexen auf der Basis von Fe und Co. Jüngste Fortschritte . Koord. Chem.-Nr. Rev. 334, 184-198 | URL: https://www.researchgate.net/profile/Julien_Bonin/publication/308271980_Molecular_Catalysis_of_the_Electrochemical_and_Photochemical_Reduction_of_CO2_with_Fe_and_Co_Metal_Based_Complexes_Recent_Aecular-Advances/b-C-Of-Chemie-Electrical-Electrochemical-Electrochemical-Electrochemical-Electro-Catalysis-Electrochemical-Electro-Catalysis-Ec with-Fe-and-Co-Metal-Based-Complexes-Recent-Advances.pdf
- Jhong HR.M, Ma S & Kenis PJA (2013) Elektrochemische Umwandlung von CO 2zu nützlichen Chemikalien: aktueller Stand, verbleibende Herausforderungen und zukünftige Chancen . Curr. Meinung. Chem.-Nr. Eng. 2, 191–199 ( Zusammenfassung )
- Aresta M, Dibenedetto A & Angelini A (2014) Katalyse zur Verwertung von Abgaskohlenstoff : aus CO 2zu Chemikalien, Materialien und Kraftstoffen . Technologische Nutzung von CO2. Chem.-Nr. Rev. 114, 1709–1742 ( Zusammenfassung )
- Qiao J, Liu Y, Hong F & Zhang J (2014) Eine Überprüfung von Katalysatoren für die Elektroreduktion von Kohlendioxid zur Herstellung kohlenstoffarmer Kraftstoffe . Chem.-Nr. Soz. Rev. 43, 631–675
- Parajuli R et al. (2015) Integration von anodischen und kathodischen Katalysatoren von erdreichen Materialien für effizientes, skalierbares CO 2Reduzierung . Oberteil. katal. 58, 57–66
- Tatin A et al. (2016) Effizienter Elektrolyseur für CO 2Spaltung in neutralem Wasser mit erdreichen Materialien . Proz. Natl Acad. Wissenschaft USA 113, 5526–5529 | URL: https://www.pnas.org/content/pnas/113/20/5526.full.pdf
- Sahara G & Ishitani O (2015) Effiziente Photokatalysatoren für CO 2Reduzierung . Inorg. Chem.-Nr. 54, 5096–5104 | URL: https://pubs.acs.org/doi/full/10.1021/ic502675a
- Takeda H, Cometto C, Ishitani O & Robert M (2017) Elektronen, Photonen, Protonen und auf der Erde reichlich vorhandene Metallkomplexe für die molekulare Katalyse von CO 2Reduzierung . ACS-Katal. 7, 70–88 ( Zusammenfassung )
- Shen, J. et al. (2015) Elektrokatalytische Reduktion von Kohlendioxid zu Kohlenmonoxid und Methan an einem immobilisierten Kobalt-Protoporphyrin . Nat. Verbreitet. 6, 8177 | URL: https://www.nature.com/articles/ncomms9177
- Weng Z et al. (2016) Elektrochemisches CO 2Reduktion zu Kohlenwasserstoffen an einem heterogenen molekularen Cu-Katalysator in wässriger Lösung . J. Am.Chem. Soz. 138, 8076–8079 | URL: https://pdfs.semanticscholar.org/a69e/11c9a8e97716bdbd4a24aa5e687f447616fa.pdf .
- Manthiram K, Beberwyck BJ & Alivisatos AP (2014) Verbesserte elektrochemische Methanisierung von Kohlendioxid mit einem dispergierbaren nanoskaligen Kupferkatalysator . J. Am.Chem. Soz. 136, 13319–13325
- Xie MS et al. (URL: https://cloudfront.escholarship.org/dist/prd/content/qt4882v99t/qt4882v99t.pdf ) Aminosäuremodifizierte Kupferelektroden zur verbesserten selektiven Elektroreduktion von Kohlendioxid zu Kohlenwasserstoffen . Energie Ca. Wissenschaft 9, 1687–1695 (2016)
- WuT et al. (2014) Ein kohlenstoffbasierter Photokatalysator wandelt effizient CO 2 . umzu CH4 und C2H2 unter sichtbarem Licht . Grüne Chem. 16, 2142–2146
- AlOtaibi B, Fan S, Wang D, Ye J & Mi Z (2016) Künstliche Photosynthese auf Wafer-Ebene für CO 2Reduktion zu CH4 und CO mit GaN-Nanodrähten . ACS-Katal. 5, 5342–5348 ( Zusammenfassung )
- Liu X, Inagaki S & Gong J (2016) Heterogene molekulare Systeme für photokatalytisches CO 2Reduktion mit Wasseroxidation . Angew. Chem.-Nr. Int. Hrsg. 55, 14924–14950 ( Abstract )
- Wang Y et al. (2016) Erleichterte einstufige Synthese von hybridem graphitischem Kohlenstoffnitrid und Kohlenstoffverbundwerkstoffen als Hochleistungskatalysatoren für CO 2photokatalytische Umwandlung . ACS-Appl. Mater. Interf. 8, 17212–17219 ( Zusammenfassung )
- Zhu, S. et al. (2016) Photokatalytische Reduktion von CO 2mit H2O zu CH4 über ultradünnen SnNb2O6 2D-Nanoblättern unter Bestrahlung mit sichtbarem Licht . Grüne Chem. 18, 1355–1363 | URL: https://www.researchgate.net/profile/Ling_Wu10/publication/283244219_Photocatalytic_reduction_of_CO_2_with_H_2_O_to_CH_4_over_ultrathin_SnNb_2_O_6_2D_nanosheets_under_visible_light_irradiation/links/569dcad408ae950bd7a6b275.pdf )
- Yu L et al. (2016) Verbesserte Aktivität und Stabilität von kohlenstoffdekorierten mesoporösen Kupferoxid-Nanostäbchen für CO 2Reduzierung der künstlichen Photosynthese . ACS-Katal. 6, 6444–6454 ( Zusammenfassung )
- Azcarate I, Costentin C, Robert M & Savéant J.-M (2016) Eine Studie über Ladungswechselwirkungs- Ersatzeffekte durch den Raum in der molekularen Katalyse, die zum Design des effizientesten Katalysators für die elektrochemische CO2-zu-CO-Umwandlung führt . J. Am.Chem. Soz. 138, 16639–16644
- Costentin C, Robert M, Savéant JM. & Tatin A (2015) Effizienter und selektiver molekularer Katalysator für die elektrochemische CO2-zu-CO-Umwandlung in Wasser . Proz. Natl Acad. Wissenschaft USA 112, 6882–6886
- Heng Rao, Luciana C. Schmidt, Julien Bonin & Marc Robert (2018) „ Sichtbares Licht getriebene Methanbildung aus CO 2mit einem molekularen Eisenkatalysator ”; Buchstabe | 17. Juli 2017 Natur Band 548, Seiten 74–77 (03. August 2017) | URL: https://www.nature.com/articles/nature23016#ref2
- Li, X., Yu, J., Jaroniec, M., & Chen, X. (2019). Cokatalysatoren zur selektiven Photoreduktion von CO 2in Solarbrennstoffe. Chemische Übersichten, 119 (6), 3962-4179. ( Zusammenfassung )
- Zhang, B., & Sun, L. (2019). Künstliche Photosynthese: Chancen und Herausforderungen molekularer Katalysatoren . Chemical Society Reviews, 48 (7), 2216-2264.
- Andrei V, Reuillard B & Reisner E (2019) Bias-freie solare Synthesegasproduktion durch Integration eines molekularen Kobaltkatalysators mit Perowskit – BiVO 4 Tandems . Naturmaterialien, 1-6 ( Zusammenfassung )
- Dalle KE, Warnan J, Leung JJ, Reuillard B, Karmel IS & Reisner E (2019) Elektro- und solargetriebene Brennstoffsynthese mit Übergangsmetallkomplexen der ersten Reihe . Chemische Übersichten, 119 (4), 2752-2875 | URL: https://pubs.acs.org/doi/full/10.1021/acs.chemrev.8b00392 ( PDF-Version )
Siehe auch
Literaturverzeichnis
- Gérard Borvon, Geschichte von Kohlenstoff und CO 2. Vom Ursprung des Lebens bis zum Klimawandel , Vuibert, 2013, 256 S.