Luft
| Luft | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifizierung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-Code | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molmasse | 28,965 g / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° Fusion | –216,2 ° C ( 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kochen | –194,3 ° C ( 1 atm , 874,0 kg / m 3 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Löslichkeit | 0,0292 Vol./Vol. (Wasser, 0 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
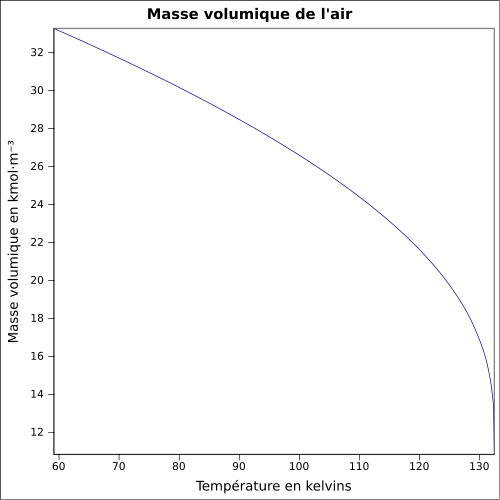
| Volumenmasse |
1,2 kg / m 3 ( 21,1 ° C , 1 atm )
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
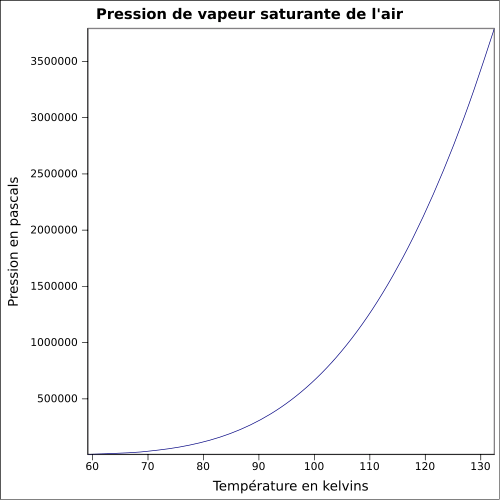
| Sättigender Dampfdruck |
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritischer Punkt | –140,6 ° C , 3.771 kPa , 351 kg / m 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 0,023 4 W m –1 K –1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
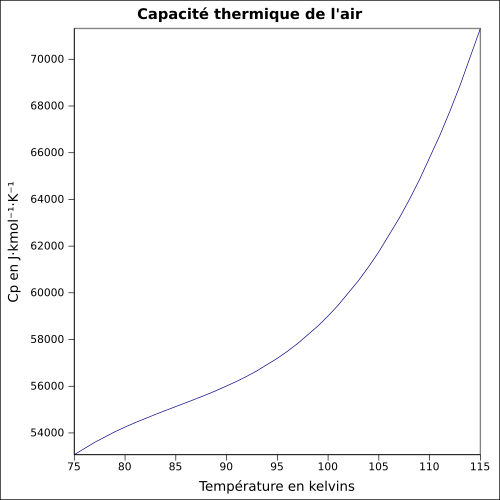
| C p |
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brechungsindex | 1.00026825 ( 100 kPa , trockene Luft mit 450 ppm CO 2) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Einheiten von SI und STP, sofern nicht anders angegeben. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Die Luft ist eine Mischung von Gasen, die die Erdatmosphäre bilden . Es ist normalerweise farblos, unsichtbar und geruchlos.
Komposition
Trockene Luft in Bodennähe ist ein homogenes Gasgemisch. Es setzt sich ungefähr zusammen aus Molenbruch oder Volumen von:
- 78,08% Stickstoff ;
- 20,95% Sauerstoff ;
- weniger als 1% der anderen Gase, einschließlich:
Es enthält auch Spuren von 0,000072% Diwasserstoff (0,72 ppmv ), aber auch Ozon sowie eine minimale Anwesenheit von Radon . Es kann auch Schwefeldioxid , Stickoxide , fein suspendierte Substanzen in Aerosolform , Staub und Mikroorganismen enthalten.
Meistens ist die Luft in der Erdumgebung feucht, weil sie Wasserdampf enthält . In Bodennähe ist die Menge an Wasserdampf sehr variabel. Dies hängt von den klimatischen Bedingungen und insbesondere von der Temperatur ab. Der Partialdruck von Wasserdampf in der Luft wird durch seinen gesättigten Dampfdruck begrenzt, der stark mit der Temperatur variiert:
| Lufttemperatur | -10 ° C. | 0 ° C. | 10 ° C. | 20 ° C. | 30 ° C. | 40 ° C. |
| % Wasserdampf
für einen Luftdruck von 1013 hPa |
0 bis 0,2% | 0 bis 0,6% | 0 bis 1,2% | 0 bis 2,4% | 0 bis 4,2% | 0 bis 7,6% |
Der prozentuale Anteil des in der Luft vorhandenen Wasserdampfs wird anhand der Feuchtigkeitsrate gemessen und ist ein wichtiges Element für Wettervorhersagen. Es gibt verschiedene Größen, um die Hydrometrie zu beschreiben: absolute Luftfeuchtigkeit , die der Masse des Wasserdampfs pro Luftvolumen entspricht; und relative Luftfeuchtigkeit , die der Prozentsatz des Partialdrucks von Wasserdampf relativ zum Sättigungsdampfdruck ist .
Der Kohlendioxidgehalt variiert im Laufe der Zeit. Auf der einen Seite, erfährt es eine jährliche Änderung von etwa 6,5 ppmv ( p ection p ar m illion in v olume) Amplitude. Andererseits steigt die durchschnittliche Jahresrate um 1,2 bis 1,4 ppmv pro Jahr. Bei 384 ppmv (0,0384%) Mitte 2008 waren es 278 ppmv vor der industriellen Revolution , 315 ppmv im Jahr 1958, 330 ppmv im Jahr 1974 und 353 ppmv im Jahr 1990. Dieses Treibhausgas-Gewächshaus spielt eine wichtige Rolle bei der globalen Erwärmung des Planeten .
Das Methan ist ein weiteres großes Gasgewächshaus, dessen Geschwindigkeit mit der Zeit zunimmt: 800 mm 3 / m 3 (0,8 ppmv ) im vorindustriellen Zeitalter, 1585 mm 3 / m 3 1985, 1663 mm 3 / m 3 im Jahr 1992 und 1.676 mm 3 / m 3 im Jahr 1996.
Bis zu einer Höhe von etwa 80 km ist die Zusammensetzung der trockenen Luft sehr homogen, wobei die einzige signifikante Variation in der Zusammensetzung der Luft die des Wasserdampfgehalts ist.
Luftzusammensetzung
|
|
||||||||||||||||||||||||||||||||||||||||||||
Die Massenanteile können bewertet werden, indem die Volumenanteile mit dem Verhältnis der Molmasse des betrachteten Gases geteilt durch die Molmasse der Luft multipliziert werden, d. H. 28,976 g mol –1 , beispielsweise im Fall von CO 2. Dieses Verhältnis ist nicht vernachlässigbar, da es gleich 44 / 28,976 = 1,5185 ist, daher der Massengehalt von CO 2in Luft gleich 415 × 1,5185 = 630 ppmm .
Volumenmasse
Da Luft ein komprimierbares Gas ist, hängt ihre Dichte (in kg / m 3 ) von Druck, Temperatur und Luftfeuchtigkeit ab.
Für trockene Luft bei normalem atmosphärischen Druck ( 1013,25 hPa ):
Im Allgemeinen nimmt 1,293 kg / m 3 zu 0 ° C und 1,204 kg / m 3 zu 20 ° C .
Dies wird verallgemeinert ( ideale Gasformel ) in: (mit T in Kelvin und P in Pascal gemäß den SI-Konventionen). Für eine Temperatur θ in Grad Celsius wird die Temperatur T in Kelvin durch Addition von 273,15 zu θ erhalten : T (K) = θ (° C) + 273,15 .
Treibhauspotenzial
Das globale Erwärmungspotential (GWP in Englisch : GWP: Globales Erwärmungspotential ) oder gleichwertiges CO 2ermöglicht es, die „Schädlichkeit“ jedes Treibhausgases zu messen .
Die folgende Tabelle gibt den Wert des GWP für die wichtigsten in der Luft vorhandenen Treibhausgase an:
| PRG | 1 (Referenz) | 8 | 23 | 310 | von 1.300 bis 1.400 | von 6.200 bis 7.100 | 6500 | 22.800 |
| Gas | Kohlendioxid | Wasserdampf | Methan | Lachgas (N 2 O) | Chlordifluormethan (H-FCKW) | Dichlordifluormethan (FCKW) | Tetrafluoridkohlenstoff (CF 4 ) | Schwefelhexafluorid (SF 6 ). |
Brechungsindex
Der Ausdruck für den Brechungsindex von Luft "unter Standardbedingungen" lautet:
wobei wo die Wellenlänge in Nanometern (nm) ausgedrückt wird, wo der Kehrwert der Wellenlänge in Mikrometern ist.Es ist für trockene Luft mit 0,03% Kohlendioxid bei einem Druck von 101.325 Pa (760 Millimeter Quecksilber) und einer Temperatur von 288,15 Kelvin ( 15 ° C ).
Wir können n für eine andere Temperatur oder einen anderen Druck erhalten, indem wir einen der folgenden zwei Ausdrücke verwenden:
mit:
- T , Temperatur ausgedrückt in Kelvin ;
- p , Druck in Pascal;
- T s , 288,15 K ;
- p s , 101,325 Pa ;
- n s der Brechungsindex von Luft oben angegebenen
oder :
mit:
- T , Temperatur in Grad Celsius ;
- T s , 15 ° C ;
- p , Druck in mmHg ;
- p s , 760 mmHg ;
- 0,00366 K –1 ;
- (1,049 - 0,015 T ) × 10 –6 mmHg –1 ;
- 8,13 × 10 –7 mmHg –1 ;
- n s der Brechungsindex von Luft oben angegebene.
Thermophysikalische Eigenschaften
Aus Tabellen von Frank M. White, Wärme- und Stoffübertragung , Addison-Wesley, 1988.
mit:
- T , Temperatur in Kelvin ;
- ρ , Dichte ;
- μ , dynamische Viskosität ;
- ν , kinematische Viskosität ;
- C p , spezifische Wärme bei konstantem Druck ;
- λ , Wärmeleitfähigkeit ;
- a , thermisches Diffusionsvermögen ;
- Pr , Prandtl Nummer .
| T. | ρ | μ | ν | C p | λ | beim | Pr |
|---|---|---|---|---|---|---|---|
| K. | kg m −3 | kg m −1 s −1 | m 2 s −1 | J kg −1 K −1 | W m −1 K −1 | m 2 s −1 | - - |
| 250 | 1.413 | 1,60 × 10 –5 | 0,949 × 10 –5 | 1.005 | 0,0223 | 1,32 × 10 –5 | 0,722 |
| 300 | 1.177 | 1,85 × 10 –5 | 1,57 × 10 –5 | 1.006 | 0,0262 | 2,22 × 10 –5 | 0,708 |
| 350 | 0,998 | 2,08 × 10 –5 | 2,08 × 10 –5 | 1.009 | 0,0300 | 2,98 × 10 –5 | 0,697 |
| 400 | 0,883 | 2,29 × 10 –5 | 2,59 × 10 –5 | 1.014 | 0,0337 | 3,76 × 10 –5 | 0,689 |
| 450 | 0,783 | 2,48 × 10 –5 | 2,89 × 10 –5 | 1.021 | 0,0371 | 4,22 × 10 –5 | 0,683 |
| 500 | 0,705 | 2,67 × 10 –5 | 3,69 × 10 –5 | 1.030 | 0,0404 | 5,57 × 10 –5 | 0,680 |
| 550 | 0,642 | 2,85 × 10 –5 | 4,43 × 10 –5 | 1.039 | 0,0436 | 6,53 × 10 –5 | 0,680 |
| 600 | 0,588 | 3,02 × 10 –5 | 5,13 × 10 –5 | 1.055 | 0,0466 | 7,51 × 10 –5 | 0,680 |
| 650 | 0,543 | 3,18 × 10 –5 | 5,85 × 10 –5 | 1.063 | 0,0495 | 8,58 × 10 –5 | 0,682 |
| 700 | 0,503 | 3,33 × 10 –5 | 6,63 × 10 –5 | 1.075 | 0,0523 | 9,67 × 10 –5 | 0,684 |
| 750 | 0,471 | 3,48 × 10 –5 | 7,39 × 10 –5 | 1.086 | 0,0551 | 10,8 × 10 –5 | 0,686 |
| 800 | 0,441 | 3,63 × 10 –5 | 8,23 × 10 –5 | 1.098 | 0,0578 | 12,0 × 10 –5 | 0,689 |
| 850 | 0,415 | 3,77 × 10 –5 | 9,07 × 10 –5 | 1 110 | 0,0603 | 13,1 × 10 –5 | 0,692 |
| 900 | 0,392 | 3,90 × 10 –5 | 9,93 × 10 –5 | 1.121 | 0,0628 | 14,3 × 10 –5 | 0,696 |
| 950 | 0,372 | 4,02 × 10 –5 | 10,8 × 10 –5 | 1,132 | 0,0653 | 15,5 × 10 –5 | 0,699 |
| 1000 | 0,352 | 4,15 × 10 –5 | 11,8 × 10 –5 | 1.142 | 0,0675 | 16,8 × 10 –5 | 0,702 |
| 1.100 | 0,320 | 4,40 × 10 –5 | 13,7 × 10 –5 | 1.161 | 0,0723 | 19,5 × 10 –5 | 0,706 |
| 1.200 | 0,295 | 4,63 × 10 –5 | 15,7 × 10 –5 | 1.179 | 0,0763 | 22,0 × 10 –5 | 0,714 |
| 1.300 | 0,271 | 4,85 × 10 –5 | 17,9 × 10 –5 | 1.197 | 0,0803 | 24,8 × 10 –5 | 0,722 |
Das Verhältnis zwischen Temperatur und Wärmeleitfähigkeit von Luft, gültig für eine Temperatur zwischen 100 K und 1600 K, ist wie folgt:
oder :
- : Temperatur ausgedrückt in K.
- : Wärmeleitfähigkeit in W m −1 K −1
Die Beziehung zwischen der dynamischen Viskosität von Luft und der Temperatur ist:
oder :
- : Temperatur in K.
- : dynamische Viskosität in kg m −1 s −1
Die Beziehung zwischen der kinematischen Viskosität von Luft und der Temperatur ist:
oder :
- : Temperatur in K.
- : kinematische Viskosität in m 2 / s
Nach der Information WPI (en) ist die Beziehung zwischen der spezifischen Luftwärme und der Temperatur:
oder :
- : Temperatur in K.
- : spezifische Wärme in J kg −1 K −1
Druck
Aufgrund des mit der Höhe abnehmenden Luftdrucks ist es erforderlich, die Kabinen von Flugzeugen und anderen Flugzeugen unter Druck zu setzen . In der Praxis ist der in den Kabinen ausgeübte Druck größer als der Außendruck, jedoch geringer als der Druck in Bodennähe.
Die Druckluft wird auch beim Tauchen verwendet .
Verflüssigung
Luft besteht aus verschiedenen Gasen, die, wenn sie ausreichend gekühlt werden, schließlich in den flüssigen Zustand und dann in den festen Zustand übergehen . Zum Beispiel kann der Sauerstoff bei einer Temperatur von fest wird -218 ° C , die Stickstoff verflüssigt sich bei -195 ° C . Bei einer Temperatur von –270 ° C (ca. 3 K ) sind dann alle Gase außer Helium fest und wir erhalten "gefrorene Luft".
Die Luft konnte nicht verflüssigt werden, bevor die kritischen Drücke und Temperaturen bekannt sind, die die theoretischen Grenzen markieren, ab denen eine Verbindung nur im gasförmigen Zustand existieren kann. Da Luft ein Gemisch ist, haben diese Werte keine strenge Bedeutung, aber tatsächlich ist die Luft bei einer Temperatur über –140 ° C nicht mehr verflüssigbar.
Siedetemperatur von Luftkomponenten
| Nachname | Formel | Temperatur |
|---|---|---|
| Distickstoff | Nr. 2 | –195,79 ° C , flüssiger Stickstoff |
| Disauerstoff | O 2 | –183 ° C , flüssiger Sauerstoff |
| Argon | Ar | –185,85 ° C. |
| Kohlendioxid | CO 2 | –56,6 ° C bei 5,12 atm |
| Neon | Geboren | -246,053 ° C. |
| Helium | Hallo | –268,93 ° C , flüssiges Helium |
| Stickstoffmonoxid | NEIN | –151,8 ° C. |
| Krypton | Kr | –154,34 ° C. |
| Methan | CH 4 | –161,52 ° C. |
| Dihydrogen | H 2 | –252,76 ° C , flüssiger Wasserstoff |
| Lachgas | N 2 O. | –88,5 ° C. |
| Xenon | Xe | –108,09 ° C. |
| Stickstoffdioxid | NEIN 2 | 21,2 ° C. |
| Ozon | O 3 | –111,9 ° C. |
| Radon | Rn | –61,7 ° C. |
Der erste Tropfen flüssiger Luft wurde fast gleichzeitig erhält Louis Paul Cailletet und Raoul-Pierre Pictet in 1877 , durch plötzliche Ausdehnung zwischen 300 und 1 Atmosphäre.
In 1894 , der niederländischen Physiker Heike Kamerlingh Onnes entwickelte die erste Flüssigkeit Luftanlage. In den nächsten 40 Jahren haben Forscher in Frankreich, Großbritannien, Deutschland und Russland den Prozess erheblich verbessert.
Sir James Dewar erste verflüssigte Wasserstoff in 1898 und Heike Kamerlingh Onnes Helium, das schwierigste Gas zu verflüssigen, in 1908 .
Unabhängig von Carl von Linde , Georges Claude entwickelte in 1902 ein industrielles Verfahren zur Verflüssigung von Luft.
Symbolisch
- In einem unwissenschaftlichen Bereich ist Luft eines der vier Elemente (neben Feuer , Wasser und Erde ), die einst als Substanzen angesehen wurden (und in einigen Kulturen immer noch als solche angesehen wurden), auf denen das ganze Leben lang basieren würde. Er ist das Symbol des Geistes.
- Luft wird auch oft mit verschiedenen anderen Konzepten in Verbindung gebracht, beispielsweise mit der Familie der Schwerter in Tarotdecks .
Anmerkungen und Referenzen
Anmerkungen
- Dies ist die Molmasse trockener Luft.
Verweise
- " Air " auf olivier.fournet.free.fr (abgerufen am 4. März 2010 )
- (en) Compressed Gas Association, Handbuch für Druckgase , Springer,1999, 4 th ed. 702 p. ( ISBN 0-412-78230-8 , online lesen ) , p. 234
- (en) Robert H. Perry und Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- (in) Philip E. Ciddor, " Brechungsindex von Luft: Neue Gleichungen für das sichtbare und nahe Infrarot " , Applied Optics , Vol. 35, n O 9,1996, p. 1566-1573 ( DOI 10.1364 / AO.35.001566 )
- (in) Aktuelles globales CO2 auf noaa.gov, abgerufen am 21. April 2021.
- (in) The Keeling Curve , die Website keelingcurve.ucsd.edu, abgerufen am 23. April 2015
- CO 2 -Konzentration in der Erdatmosphäre
- CO 2 -Konzentration gemessen in Mauna Loa (Hawaii), NOAA.
- Methankonzentration gemessen in Mauna Loa (Hawaii), NOAA.
- In der Praxis enthält stark getrocknete Luft noch Spuren von Wasserdampf.
- Datenquelle: Kohlendioxid: (en) NASA - Earth Fact Sheet , Januar 2007. Methan: IPCC TAR; Tabelle 6.1, 1998 (de) IPCC Third Assessment Report "Climate Change 2001" von GRID-Arendal im Jahr 2003. Die NASA-Summe betrug 17 ppmv von 100% und der CO 2hier um 15 ppmv erhöht . Zur Normalisierung sollte N 2 um 25 ppmv und O 2 um 7 ppmv reduziert werden .
- " Air Brechungsindex " , auf olivier.fournet.free.fr (zugegriffen 4. März 2010 )
- Chemiker
- Chemiker , nicht gefunden 11. August 2013
- Dieses Dokument von der WPI-Website auf der Website wpi.edu
Siehe auch
Zum Thema passende Artikel
- Luftdichte
- Luftmasse
- Psychrometrie
- Feuchte Luft
- Luftverschmutzung und Artikel aus der Kategorie: Luftverschmutzung
- Luftqualität