Argon
| Argon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Festes und flüssiges Argon. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Position im Periodensystem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | Ar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Familienname, Nachname | Argon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordnungszahl | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zeitraum | 3 e Periode | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | p . blockieren | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementfamilie | Edelgas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronische Konfiguration | [ Ne ] 3 s 2 3 p 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronen nach Energieniveau | 2, 8, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomare Eigenschaften des Elements | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 39,948 ± 0,001 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | ( 71 Uhr ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 106 ± 22 Uhr | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 188 Uhr | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustand | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxid | Unbekannt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionisierungsenergien | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 Re : 15,759610 eV | 2 e : 27,62966 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 e : 40,74 eV | 4 e : 59,81 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 e : 75,02 eV | 6 th : 91.009 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 e : 124,323 eV | 8 e : 143.460 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 9 e : 422,45 eV | 10 e : 478,69 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 11 e : 538,96 eV | 12 e : 618,26 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 13 e : 686,10 eV | 14 e : 755,74 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 15 e : 854,77 eV | 16 th : 918,03 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 e : 4 120,8857 eV | 18 e : 4 426.2296 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stabilste Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Einfache physikalische Eigenschaften des Körpers | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normalzustand | Gas (nicht magnetisch) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
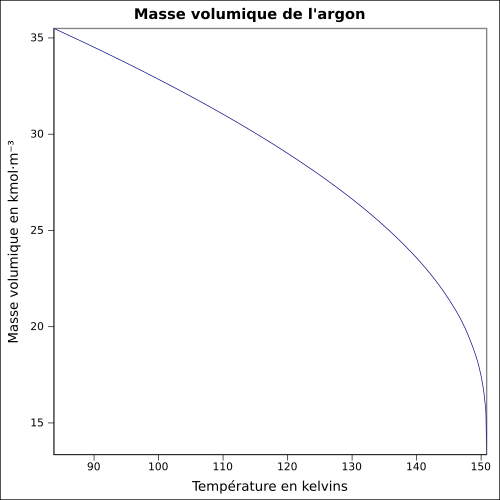
| Volumenmasse |
1,7837 g · L -1 ( 0 ° C , 1 atm ) Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallsystem | Flächenzentriert kubisch | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Farbe | farblos | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusionspunkt | −189,36 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | −185,85 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusionsenergie | 1.188 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenergie | 6,43 kJ · mol -1 ( 1 atm , -185,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritische Temperatur | −122.3 °C ° | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dreifacher Punkt | −189,3442 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarvolumen | 22.414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampfdruck |
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 319 m · s -1 bis 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenhitze |
520 J · kg -1 · K -1
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 0,01772 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verschieden | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.028.315 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EG | 231-147-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vorsichtsmaßnahmen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Warnung H280 und P403 H280 : Enthält Gas unter Druck; kann bei Erwärmung explodieren P403 : An einem gut belüfteten Ort aufbewahren. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 ZU, A : Kritische Temperatur des komprimierten Gases = −122,4 ° C Angabe bei 1,0 % gemäß Klassifizierungskriterien |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : erstickendes Gas oder Gas, das kein Nebenrisiko darstellt UN-Nummer : 1006 : KOMPRIMIERTES ARGON Klasse: 2.2 Klassifizierungscode: 1A : komprimiertes Gas, aspxiant; Etikett: 2.2 : Nicht brennbare, nicht giftige Gase (entspricht den mit einem A oder einem großen O gekennzeichneten Gruppen); 
22 : tiefgekühlt verflüssigtes Gas, erstickend UN-Nummer : 1951 : gekühltes flüssiges Argon Klasse: 2.2 Klassifizierungscode: 3A : tiefgekühlt verflüssigtes Gas, erstickend; Etikett: 2.2 : Nicht brennbare, nicht giftige Gase (entspricht den mit einem A oder einem großen O gekennzeichneten Gruppen);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Einheiten von SI & STP, sofern nicht anders angegeben. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Das Argon ist das chemische Element der Ordnungszahl 18 und Symbol Ar. Es gehört zur Gruppe 18 des Periodensystems und gehört zur Familie der Edelgase , auch "Edelgase" genannt, zu denen auch das Helium , das Neon , gehört. Krypton , Xenon und Radon . Argon das ist 3 rd häufigste Bestandteil der Erdatmosphäre , mit einem Massenanteil von 1,288%, zu einem entsprechenden Volumenanteil von 0,934% (oder 9.340 ppm ) und ist das am häufigsten vorkommende Edelgas in der Welt. " Erdkruste , 1,5 ppm ausmachen . Argon in der Erdatmosphäre ist fast vollständig aus dem Argon - 40 , ein radiogenen Nuklid resultierenden aus dem Zerfall von Kalium - 40 , während das Argon in dem beobachteten Universum ist in erster Linie aus dem Argon - 36 , hergestellt von den stellaren nucleosynthesis im Supernovä .
Der Name Argon kommt aus dem Altgriechischen ἀργόν, was "faul", "faul" bedeutet [abgeleitet vom griechischen Wort ἀεργός, gebildet aus ἀ-εργός, was "ohne Arbeit", "müßig" bedeutet], in Bezug auf die Tatsache, dass dies Element ist chemisch inert. Seine elektronische Konfiguration stellt eine gesättigte Valenzschicht dar, die den Ursprung seiner Stabilität und die praktisch Unmöglichkeit, kovalente Bindungen aufzubauen , darstellt . Die Temperatur von 83.805 8 K seines Tripelpunktes ist einer der Referenzpunkte der Internationalen Temperaturskala von 1990 (ITS-90).
Argon wird industriell durch fraktionierte Destillation von verflüssigter Luft hergestellt . Es wird hauptsächlich als inerte Atmosphäre beim Schweißen und bei verschiedenen industriellen Prozessen bei hohen Temperaturen mit reaktiven Substanzen verwendet. In Graphit- Elektrolichtbogenöfen wird daher eine Argonatmosphäre verwendet , um deren Verbrennung zu verhindern . Es verwendet auch Argon bei der Beleuchtung durch Glühlampen , Leuchtstoffröhren und Gasröhren . Es wird verwendet, um blau-grüne Gaslaser herzustellen .
Haupteigenschaften
Argon ist farblos, geruchlos, nicht brennbar und ungiftig in gasförmigem, flüssigem oder festem Zustand. Seine Löslichkeit in Wasser ist ungefähr mit der von Sauerstoff vergleichbar und beträgt das 2,5-fache von Stickstoff . Es ist unter fast allen Bedingungen chemisch inert und bildet bei Raumtemperatur keine nachgewiesenen Chemikalien .
Argon ist jedoch in der Lage, unter bestimmten extremen Bedingungen außerhalb des Gleichgewichts chemische Verbindungen zu bilden. Das Argon- Fluorwasserstoff thusarf wurde somit durch Ultraviolett- Photolyse von Fluorwasserstoff HF in einer kryogenen Matrix aus Cäsiumiodid CsI und Ar-Argon erhalten; stabil unter 27 K ( −246.15 °C ) und wurde durch Infrarotspektroskopie identifiziert . Argonfluorhydrid ist die einzige bekannte Argonverbindung, die neutral und im Grundzustand stabil ist .
Argon kann auch bilden Clathrate in Wasser , wenn seine Atome in dem dreidimensionalen Gitter von gebildeten gefangen sind Eis . Es gibt auch mehratomige Ionen, die Argon enthalten, wie das Argonhydrid- Kation ArH + , und Exciplexe wie Ar 2* und ArF*. Verschiedene Verbindungen mit den Bindungen Ar C und Ar If stabil wurden durch numerische Simulation vorhergesagt , aber nicht im Labor synthetisiert.
Die Hauptisotope von Argon in der Erdkruste sind das Argon 40 ( 40 Ar) zu 99,6%, das Argon 36 ( 36 Ar) zu 0,34% und das Argon 38 ( 38 Ar) zu 0,06%. Das Kalium-40 ( 40 K) zerfällt spontan zu 11,2 % in Argon 40 durch Elektroneneinfang oder Emissionstomographie und in einer Menge von 88,8 % in Calcium 40 ( 40 Ca) durch β-Zerfall - mit einer Halbwertszeit (halb -Leben) von 1,25 Milliarden Jahren. Diese Dauer und das Verhältnis der gebildeten Nebenprodukte ermöglichen die Altersbestimmung von Gesteinen durch die Methode der Kalium-Argon-Datierung .
In der Erdatmosphäre wird das Argon 39 hauptsächlich durch die Wechselwirkung der kosmischen Strahlung auf das Argon 40 durch Neutroneneinfang gefolgt von einer doppelten Neutronenemission erzeugt . Im Untergrund kann es auch aus Kalium 39 durch Neutroneneinfang gefolgt von Protonenemission hergestellt werden .
Das Argon 37 wird bei unterirdischen Tests aus Calcium 40 durch Neutroneneinfang gefolgt von α-Zerfall hergestellt ; es hat eine Halbwertszeit von 35 Tagen.
Argon ist insofern bemerkenswert, als seine Isotopenzusammensetzung von einer Region des Sonnensystems zur anderen erheblich variiert . Argon, dessen Hauptquelle der radioaktive Zerfall von Kalium 40 in Gesteinen ist, besteht hauptsächlich aus Argon 40 , wie auf terrestrischen Planeten, die eine Atmosphäre bewahren: Venus , Erde und Mars . Andererseits besteht das Argon, das direkt durch die stellare Nukleosynthese gebildet wird, im Wesentlichen aus Argon 36, das durch die Alpha-Reaktion erzeugt wird , wie es bei der Sonne der Fall ist , deren Argon nach den Messungen des Sonnenwinds 84,6% von Argon 36 ausmacht . Ähnlich ist es bei Riesenplaneten , wo die relative Häufigkeit der Isotope 36 Ar: 38 Ar: 40 Ar 8400: 1600:1 beträgt.
Neben der terrestrischen Atmosphäre , die einen Volumenanteil von 0,934 % Argon oder 9.340 ppm hat , enthält die Atmosphäre des Merkur 0,07 ppm , die der Venus 70 ppm und die des Mars 19.300 ppm oder 1,93%.
Die Dominanz des radiogenen Argons 40 in der Erdatmosphäre ist dafür verantwortlich, dass die Atommasse des Argons der Erde in der Größenordnung von 39,95 u um 0,85 u größer ist als die des Kaliums , das ihm im Periodensystem der Elemente folgt und dessen Atommasse in der Größenordnung von 39,10 u liegt . Dies erschien bei der Entdeckung von Argon im Jahr 1894 paradox, da Dmitri Mendeleïev sein Periodensystem nach zunehmender Atommasse geordnet hatte, was dazu führte, dass Argon zwischen Kalium und Calcium mit einer Atommasse von etwa 40, 08 u platziert und mit verwechselt werden musste die von Argon auf 0,13 u genau , während es einen atomaren Massenunterschied von 3,65 u zwischen Chlor (35,45 u ) und Kalium (39,10 u ) gab. Dieses Problem wurde von Henry Moseley gelöst , der 1913 demonstrierte, dass das Periodensystem nach steigender Ordnungszahl geordnet werden sollte und nicht nach steigender Atommasse, was die Elemente in die richtige Reihenfolge bringt.
Der atmosphärische Fluss relativ Argon im Vergleich zu anderen Edelgasen - 9340 ppm an Argon, gegen 5,24 ppm von Helium , 18.18 ppm von Neon , 1,14 ppm von Krypton und 0.087 ppm von Xenon - kann auch auf zurückzuführen radiogenic Argon 40 : Argon 36 hat in der Tat eine Häufigkeit von nur 31,5 ppm (0,337% von 9340 ppm ), in der gleichen Größenordnung wie die von Neon (18,18 ppm ).
Verbindungen
Das Argon - Atom besitzt eine Elektron gesättigte Valenz Schale , mit vollständigen s und p Subschichten . Dadurch ist dieses Element chemisch inert und sehr stabil, dh es geht nur sehr schwer eine chemische Bindung mit anderen Atomen ein. Bis 1962 , Edelgase wurden als vollständig inert und nicht geeignet für die Bildung von zu chemischen Verbindungen ; zu diesem Zeitpunkt jedoch die Synthese von Xenonhexafluoroplatinat XePtF 6 ebnete den Weg für die Chemie der Edelgase .
Die erste Verbindung von Argon mit Wolframpentacarbonyl, der chemischen Formel W (CO) 5 Ar, wurde 1975 veröffentlicht, aber seine tatsächliche Existenz bleibt umstritten. Im August 1962 wurde an der Universität Helsinki das Argonfluorhydrid Harf durch ultraviolette Photolyse von Fluorwasserstoff HF in einer kryogenen Matrix aus Cäsiumiodid CsI und Ar argonstabiler Verbindung unter 27 K ( −246.15 °C ) synthetisiert, die durch Infrarotspektroskopie identifiziert wurde . Diese Entdeckung führte zu der Idee, dass Argon schwach gebundene Verbindungen bilden könnte.
Die Dikation metastabilen ARCf 22+ , isoelektronisch mit Carbonylfluorid COF 2und Phosgen COCl 2aus der Sicht der Valenzelektronen wurde 2009 beobachtet, dass eine Kohlenstoff- Argon- Bindung implementiert wurde . Das dem Argonhydrid- Kation 36 (Argonium) entsprechende Molekülion 36 ArH + wurde im interstellaren Medium auf Höhe des Krebsnebels nachgewiesen ; es ist die erste im Weltraum nachgewiesene Edelgasverbindung .
Das feste Argonhydrid Ar (H 2 ) 2ist eine Van-der-Waals- Verbindung mit der gleichen Kristallstruktur wie die Laves-Phase (en) MgZn 2. Es bildet sich bei Drücken zwischen 4,3 und 220 GPa , obwohl die Ergebnisse der Raman-Spektroskopie nahelegen, dass die H 2 -Moleküleder Verbindung Ar (H 2 ) 2über 175 GPa dissoziieren .
Industrielle Produktion und Anwendungen
Argon wird industriell durch hergestellte fraktionierte Destillation von verflüssigter Luft in Einheiten kryogenen die Destillation von Luft (in) , eine Methode für die Trenn flüssigen Stickstoffs , der bei Furunkeln 77,3 K , Argon, die bei Furunkeln 87,3 K , und dem flüssigen Sauerstoff , der bei Furunkeln 90,2 K . Die Weltproduktion von Argon liegt in der Größenordnung von 700.000 Tonnen pro Jahr.
Argon hat mehrere interessante Eigenschaften, die seinen industriellen Einsatz rechtfertigen:
- es ist ein chemisch inertes Gas;
- es ist eine billige Alternative, wenn der Stickstoff nicht ausreichend inert ist;
- es hat eine geringe Wärmeleitfähigkeit (es ist daher ein Wärmeisolator );
- seine elektronischen Eigenschaften ( Ionisation , Emissionsspektrum ) werden in bestimmten Beleuchtungsanwendungen genutzt.
Andere Edelgase weisen ähnliche Eigenschaften auf und könnten ebenfalls verwendet werden, aber Argon ist mit Abstand das billigste von allen, da es als Nebenprodukt bei der Extraktion von Sauerstoff und Stickstoff aus der Luft durch kryogene fraktionierte Destillation gewonnen wird.
Industrielle Anwendungen
Argon wird in bestimmten industriellen Hochtemperaturprozessen verwendet, bei denen chemisch inerte Substanzen dazu neigen, reaktiv zu werden. Eine Argonatmosphäre verwendet wird somit in Elektroöfen mit Graphitelektroden in , um die zur Verhinderung der Verbrennung dieses Materials.
Bei einigen dieser Prozesse würde die Anwesenheit von Stickstoff oder Sauerstoff Defekte im Material verursachen. Argon wird in bestimmten Arten von verwendeten Lichtbogenschweißen , wie beispielsweise Gas - Metall - Lichtbogenschweißen und TIG - Schweißen , sowie bei der Behandlung von Titan und anderen Elementen Reagenzien. Auch Silizium- und Germaniumkristalle für die Halbleiterindustrie werden in Argonatmosphäre gezüchtet , um ihre kristalline Qualität zu gewährleisten.
Argon wird in der Geflügelindustrie als Inertgas-Erstickungsmethode verwendet, um das Geflügel zu ersticken , entweder bei einer Massenschlachtung nach dem Ausbruch einer Krankheit oder als Mittel zur abwechselnden Schlachtung der Elektronarkose . Die relative Dichte von Argon zu Luft bewirkt, dass es beim Vergasen nahe am Boden bleibt. Seine nicht reaktive Natur macht es mit Lebensmitteln kompatibel, und die Tatsache, dass es Sauerstoff im Gewebe teilweise ersetzt, verlängert die Haltbarkeit von Lebensmitteln.
Argon wird manchmal verwendet, um Brände zu löschen, indem wertvolle Ausrüstung wie Computerserver aufbewahrt wird , die durch die Verwendung von Wasser oder Schaum beschädigt würden.
Medizinische Anwendungen
Kryochirurgische Verfahren (in) wie Kryoablation (in) verwenden flüssiges Argon, um Gewebe wie Krebszellen zu zerstören . Es war möglich, es in einem Verfahren namens Argon-verstärkte Koagulation zu verwenden , das eine Form der Elektrochirurgie (in) mit einem Plasmabrenner ist , aber das Risiko einer Gasembolie birgt, die durch den Tod mindestens eines Patienten eintritt.
Argon Blue Laser werden in der Chirurgie verwendet, um die Arterien zu nähen , Tumore in der Augenchirurgie zu zerstören oder für die Elektrokoagulation durch endoskopische Läsionen von Magen-Darm-Blutungen.
Argon wird auch ersetzt wurde getestet Stickstoff in dem Atemgas genannt Argox in Entfernung von gelöstem Stickstoff von dem zu beschleunigen , um Blut .
Wissenschaftliche Forschung
Flüssiges Argon wird als Ziel für die Neutrinodetektion und die Erforschung der Dunklen Materie verwendet . Wechselwirkungen zwischen hypothetischen WIMPs und die Kerne von Argonatomen sollte einen produzieren beobachtbaren Szintillation durch Photovervielfacherröhren . Zwei-Phasen-Detektoren, die Argongas enthalten, werden verwendet, um Elektronen zu detektieren, die durch Ionisation während WIMP-Argon-Kernwechselwirkungen erzeugt werden.
Flüssiges Argon hat wie andere verflüssigte Edelgase eine hohe Szintillationsrate (ca. 51 Photonen / keV ), ist für seine eigene Szintillation transparent und relativ leicht zu reinigen. Es ist kostengünstiger als Xenon und hat ein anderes Szintillationszeitprofil, das es ermöglicht, elektronische Wechselwirkungen von nuklearen Wechselwirkungen zu unterscheiden. Es hat jedoch eine stärkere Radioaktivität β aufgrund der Kontamination durch das Argon 39 , außer wenn Argon aus dem an 39 Ar abgereicherten Grundgestein verwendet wird, dessen Halbwertszeit nur 269 Jahre beträgt und dessen Vorrat nicht durch das 40 Ar rekonstituiert wird ( n , 2 n ) 39 Ar Wechselwirkung der kosmischen Strahlung auf atmosphärische Argon .
In einem anderen Register wurde Argon 39 insbesondere für die Datierung von Grundwasser- und Eisbohrkernen in der Antarktis verwendet . Die K-Ar-Datierung und die Argon-Argon-Datierung werden auch für die radiometrische Datierung von sedimentären , metamorphen und magmatischen .
Konservativ
Argon, Nummer E938 , wird als Konservierungsmittel für Lebensmittel verwendet , um Sauerstoff und Feuchtigkeit aus der Atmosphäre in Verpackungen zu entfernen und das Verfallsdatum zu verlängern. Die Luftoxidation , die Hydrolyse und andere produktabbauende Reaktionen werden somit verzögert oder ganz blockiert. Chemische Reagenzien und pharmazeutische Moleküle werden manchmal in einer Argonatmosphäre verpackt. Dieses Edelgas wird auch als Konservierungsmittel für Lacke , Polyurethan oder auch Farben verwendet .
Argon wird auch in verwendet Weinbereitung zu schützen Wein aus Sauerstoff und zu verhindern , deren Oxidation sowie unerwünschte Bakterien Wechselwirkungen (insbesondere Essigsäurebakterie , die produzieren Essigsäure und wiederum in Weinessig ). Es kann auch als Treibmittel für Sprays verwendet werden .
Laborgeräte
Das Argon kann als Inertgas für eine Vakuumleitung und ein Handschuhfach verwendet werden ; er wird gegenüber Stickstoff bevorzugt , der weniger teuer ist, da Stickstoff mit besonders reaktiven Verbindungen sowie mit bestimmten Geräten reagieren kann. Darüber hinaus hat Argon den Vorteil, dass es im Gegensatz zu Stickstoff dichter als Luft ist, was die Anwendung in der Praxis erleichtert.
Argon kann als Trägergas in der Gaschromatographie und in der Elektrospray-Ionisation verwendet werden . Es ist das Gas der Wahl für Plasma, das in der induktiv gekoppelten Plasmaspektrometrie verwendet wird . Argon wird vorzugsweise verwendet Sputterabscheidung (In) auf den Proben von zu untersuchenden Rasterelektronenmikroskopie und für die Reinigung von Wafern in Mikrofabrikations .
Beleuchtung
Eine Glühlampe ist in der Regel mit Argon zu erhalten , um sein gefüllt Filament von Hochtemperaturoxidation . Argon wird auch für seine Strahlung durch Ionisation verwendet , wie in den Plasmalampen und den Kalorimetern in der Teilchenphysik . Die mit reinem Argon gefüllten Entladungslampen erzeugen helles blasses Violett, das Lebleu-Lavendel zieht, das durch Zugabe von etwas Quecksilber blau wird .
Argon wird auch für Ionenlaser (in) blau und grün verwendet.
Verschiedene Anwendungen
Argon wird als Wärmeisolator für Doppelverglasung verwendet . Aufgrund seiner chemischen Inertheit und geringen Wärmeleitfähigkeit wird es auch zum Füllen von Trockentauchanzügen beim Gerätetauchen verwendet .
Argon ist eines der Gase, die in der Raumfahrt als Treibstoff für VASIMRs verwendet werden können . Im Bereich der Luftwaffen wird es unter Druck verwendet, um die Köpfe bestimmter Luft-Luft- Raketen, einschließlich AIM-9 Sidewinder-Raketen , durch Entspannen zu kühlen .
Argon wurde in der Leichtathletik als Dotierstoff verwendet , der Hypoxie simuliert . Es wurde daher zusammen mit Xenon in die Liste der von der Welt-Anti-Doping-Agentur 2014 verbotenen Methoden und Substanzen aufgenommen, bevor es 2020 zurückgezogen wurde.
Geschichte und Etymologie
Das Wort Argon leitet sich vom altgriechischen ἀργός / argós ("faul", "faul", "steril") ab, gebildet aus dem privaten griechischen Präfix ἀ und dem Wort ἔργον / ergon ("Arbeit"), diese Etymologie erinnert an den trägen Charakter des 'Elements.
Die Anwesenheit eines chemisch inerten Gases in der Luft wurde bereits 1785 von Henry Cavendish vermutet, aber seine Entdeckung durch Lord Rayleigh und Sir William Ramsay am University College London dauerte bis 1894 . Sie taten dies, indem sie Sauerstoff , Kohlendioxid , Wasserdampf und Stickstoff aus einer Probe sauberer Luft entfernten und ein Inertgas hinterließen, das sie Argon nannten . Diese beiden Wissenschaftler teilten der Royal Society offiziell ihre Entdeckung mit31. Januar 1895.
Sie wurden dadurch auf die Spur gebracht, dass der chemisch erzeugte Stickstoff um 0,5 % leichter war als der, der durch Entfernung anderer damals bekannter atmosphärischer Gase aus der Luft gewonnen wurde. Die fraktionierte Destillation von verflüssigter Luft erlaubt , sie in eine signifikante Menge von Argon zu erzeugen , 1898 und den gleichzeitig zwei andere zu isolieren , Edelgasen , das Neon und Xenon .
Argon wurde auch 1882 während unabhängiger Arbeiten von HF Newall und WN Hartley beobachtet, die Spektrallinien im Emissionsspektrum von Luft feststellten, die keinem bekannten chemischen Element entsprachen .
Das chemische Symbol für Argon war bis 1957 A, dann wurde es Ar.
Gefahren
Argon ist wie Helium in geringen Konzentrationen ungefährlich. Es ist jedoch 38% dichter als Luft , und das Einatmen einer großen Menge Argon birgt die Gefahr des Erstickens durch Sauerstoffmangel ( Anoxie ); dies kann beispielsweise bei Schweißarbeiten auf engstem Raum geschehen .
Hinweise und Referenzen
- (in) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia und Santiago Barragan Alvarez , „ Kovalente Radien revisited “ , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10.1039 / b801115j )
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , TF-CRC,2006, 87 th ed. ( ISBN 0849304873 ) , p. 10-202
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 S. , Hardcover ( ISBN 978-1-420-09084-0 )
- (en) Robert H. Perry und Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 S. ( ISBN 0-07-049841-5 ) , p. 2-50
- Minuten des Internationalen Komitees für Maß und Gewicht , 78 th Sitzung, 1989, pp. T1-T21 (und S. T23-T42, englische Version).
- Chemical Abstracts Datenbank abgefragt über SciFinder Web 15. Dezember 2009 (Suche Ergebnisse )
- Eintrag der CAS-Nummer "7440-37-1" in die Chemikaliendatenbank GESTIS der IFA ( Deutsch , Englisch ), aufgerufen am 30.01.2009 (JavaScript erforderlich)
- " Argon " in der Datenbank für chemische Produkte Reptox des CSST (Quebec-Organisation für Arbeitssicherheit und Gesundheitsschutz), abgerufen am 25. April 2009
- (in) Markku Räsänen , " Argon aus dem Nichts " , Nature Chemistry , vol. 6, n o 1, Januar 2014Artikel n o 82 ( PMID 24345939 , DOI 10.1038 / nchem.1825 , online lesen )
- (en) Leonid Khriachtchev, Mika Pettersson, Nino Runeberg, Jan Lundell und Markku Räsänen , „ Eine stabile Argonverbindung “ , Nature , vol. 406 n o 6798, 24. August 2000, s. 874-876 ( PMID 10972285 , DOI 10.1038 / 35022551 , Bibcode 2000Natur.406..874K , online lesen )
- (in) VR Belosludov OS Subbotin DS Krupskii, Prokuda OV, RV und Y. Belosludov Kawazoe , " Mikroskopisches Modell von Clathratverbindungen " , Journal of Physics: Conference Series , Vol. 2, No. 29, n o 1, Januar 2006, s. 1-7 ( DOI 10.1088 / 1742-6596 / 29/1/001 , Bibcode 2006JPhCS..29 .... 1B , online lesen )
- (in) Arik Cohen, Jan Lundell und R. Benny Gerber , „ Erste Verbindungen mit chemischen Argon-Argon- und Kohlenstoff-Silizium-Bindungen “ , Journal of Chemical Physics , vol. 119, n o 13, Oktober 2003, s. 6415-6417 ( DOI 10.1063 / 1.1613631 , Bibcode 2003JChPh.119.6415C , online lesen )
- (en) J. Emsley, Nature's Building Blocks , Oxford University Press, 2001, p. 44–45 . ( ISBN 978-0-19-960563-7 )
- Étienne Roth ( Richt. ), Bernard Poty ( Richt. ), Robert Delmas et al. ( Präf. Jean Coulomb ), Methoden der Datierung durch natürliche Kernphänomene , Paris, ditions Masson , Coll. " CEA- Sammlung ",1985, 631 S. ( ISBN 978-2-225-80674-2 , Hinweis BnF n o FRBNF34836710 ) , Kap. 17 ("Silizium 32 und Argon 39")
- (in) The Science Case for 37 Ar als Monitor für unterirdische nukleare Explosionen , Seite 1, 2010
- (in) Katharina Lodders , " The Solar Abundance Argon " , The Astrophysical Journal , vol. 674, n o 1, 10. Februar 2008, s. 607-611 ( DOI 10.1086 / 524725 , Bibcode 2008ApJ ... 674..607L , arXiv arXiv: 0710.4523 , online lesen )
- (in) AGW Cameron , " Elementar- und Isotopenhäufigkeit der flüchtigen Elemente in den äußeren Planeten " , Space Science Reviews , vol. 14, n Knochen 3-4, März 1973, s. 392-400 ( DOI 10.1007 / BF00214750 , Bibcode 1973SSRv ... 14.392C , online lesen )
- (in) Marco Fontani , Mariagrazia Costa und Mary Virginia Orna , The Lost Elements: The Periodic Table's Shadow Side , New York, Oxford University Press ,2015( 1 st ed. 2014), 531 p. ( ISBN 9780199383344 ) , p. 182.
- (in) Neil Bartlett , " Xenonhexafluoroplatinat Xe + [PtF 6 ] - " , Proceedings of the Chemical Society , n o 6,Juni 1962, s. 197-236 ( DOI 10.1039 / PS9620000197 , online lesen )
- (in) Nigel A. Young , " Hauptgruppen-Koordinationschemie bei niedriger Temperatur: Eine Übersicht über matrixisolierte Komplexe der Gruppe 12 bis Gruppe 18 " , Koordinationschemie- Übersichten , vol. 257 n Knochen 5-6, März 2013, s. 956-1010 ( DOI 10.1016 / j.ccr.2012.10.013 , online lesen )
- (in) Neil Bartlett , " The Noble Gases " , Chemical & Engineering News , Vol. 2 , No. 81, n o 36, 8. September 2003, s. 32-34 ( DOI 10.1021 / cen-v081n036.p032 , online lesen )
- (in) Jessica F. Lockyear Kevin Douglas, Stephen D. Price, Małgorzata Karwowska, Karol J. Fijalkowski Wojciech Grochala Marek Remeš Jana Roithová und Detlef Schroeder , „ Generation of the ARCf 2 2+ Dication “, The Journal of Physical Chemistry Letters ,vol. 1,n o 1,8. Dezember 2009, s. 358-362 ( DOI 10.1021 / jz900274p , online lesen )
- (en) J. Barlow, BM Swinyard, PJ Owen, J. Cernicharo, HL Gomez, RJ Ivison, O. Krause, TL Lim, M. Matsuura, S. Miller, G. Olofsson und AND Polehampton , „ Erkennung von a Edelgas- Molekular-Ion, 36 ArH + , im Krebsnebel “ , Science , vol. 342, n o 6164, 13. Dezember 2013, s. 1343-1345 ( PMID 24337290 , DOI 10.1126 / science.1243582 , Bibcode 2013Sci ... 342.1343B , online lesen )
- (in) Annette K. Kleppe, Mónica Amboage und Andrew P. Jephcoat , „ Neue Hochdruck-van-der-Waals-Verbindung Kr (H 2) 4 im Krypton-Wasserstoff-Binärsystem entdeckt “ , Scientific Reports , vol. 4,16. Mai 2014Artikel, n o 4989 ( DOI 10.1038 / srep04989 , Bibcode 2014NatSR ... 4E4989K , online lesen )
- " Periodensystem der Elemente: Argon-Ar " , Environmentalchemistry.com (Zugriff am 12. September 2008 )
- (in) Sara J. Shields und ABM Raj , „ Ein kritischer Überblick über elektrische Wasserbad-Betäubungssysteme für die Geflügelschlachtung und jüngste Entwicklungen bei alternativen Technologien “ , Journal of Applied Animal Welfare Science , vol. 13, n o 4, 2012, s. 281-299 ( PMID 20865613 , DOI 10.1080 / 10888705.2010.507119 , online lesen )
- DL Fletcher , " Slaughter Technology ", Symposium: Jüngste Fortschritte in der Geflügelschlachttechnologie ,1999( Read Online zugegriffen 1 st Januar 2010 )
- (in) MJ Fraqueza und AS Barreto , „ Die Wirkung ist die Haltbarkeit von Putenfleisch von Verpackungen unter modifizierter Atmosphäre mit einer Argonmischung “ , Poultry Science , vol. 88, n O 9, September 1999, s. 1991-1998 ( PMID 19687286 , DOI 10.3382 / ps.2008-00239 , online lesen )
- (in) Joseph Z. Su, Andrew K. Kim, George P. Crampton und Zhigang Liu , „ Brandbekämpfung mit Inertgasmitteln “ , Journal of Fire Protection Engineering , vol. 11, n o 2 2001, s. 72-87 ( DOI 10.1106 / X21V-YQKU-PMKP-XGTP , online lesen )
- (in) " Tödliche Gasembolie verursacht durch Überdruck während der laparoskopischen Verwendung von Argon-verstärkter Koagulation " , Health Devices , vol. 23, n o 6, Juni 1994, s. 257-259 ( online lesen )
- (in) Jerome Canady , Kimberly Wiley und Biagio Ravo , „ Argonplasma-Koagulation und die zukünftigen Anwendungen für endoskopische Sonden Dual-Mode “ , Reviews in Gastroenterological Disorders , Vol. 2 , No. 6, n o 1,2006, s. 1-12 ( ISSN 1533-001X , PMID 16520707 , online gelesen , abgerufen am 9. Oktober 2017 ).
- (in) Andrew A Pilmanis Ulf I. Balldin, James T. Webb und Kevin M. Krause , „ Stufenweise Dekompression auf 3,5 Psi unter Verwendung von Argon-Sauerstoff- und Sauerstoff-Atmungs-100%-Mischungen “ , Luftfahrt, Raumfahrt und Umweltmedizin , Flug. 74, n o 12, Dezember 2003, s. 1243-1250 ( PMID 14692466 , online lesen )
- (in) Dan Gastler Ed Kearns, Andrew Hime, Laura C. Stonehill Stan Seibert, Josh Klein, Hugh W. Lippincott, Daniel N. McKinsey und James A. Nikkel , „ Messung der Szintillationseffizienz für nukleare Rückstöße in flüssigem Argon “ , Physische Übersicht C , vol. 85, n o 6, 27. Juni 2012Artikel, n o 065811 ( DOI 10.1103 / PhysRevC.85.065811 , Bibcode 2012PhRvC..85f5811G , arXiv 1004,0373 , online lesen )
- (in) J. Xu F. Calaprice, C. Galbiati, A. Goretti Guray G., T. Hohman, D. Holtz, An. Ianni, Herr Laubenstein, Loer B., C. Lovec, CJ Martov, D Montanari, S. Mukhopadhyay, A. Nelson, SD Rountree, RB Vogelaar und A. Wright , „ Eine Untersuchung des Spurengehalts von 39 Ar in Argon aus tiefen unterirdischen Quellen “ , Astroteilchenphysik , vol. 66, Juni 2015, s. 53-60 ( DOI 10.1016 / j.astropartphys.2015.01.002 , Bibcode 2015APh .... 66 ... 53X , arXiv 1204.6011 , online lesen )
- Paul Depovere, Das Periodensystem der Elemente. Das grundlegende Wunder des Universums , De Boeck Supérieur ,2002, s. 98.
- (de) Henry Cavendish , " XXIII. Experimente an der Luft. “ , Philosophische Transaktionen der Royal Society of London , vol. 75, 1785, s. 372-384 ( DOI 10.1098 / rstl.1785.0023 , Bibcode 1785RSPT ... 75..372C , online lesen )
- (in) Robert John Strutt und William Ramsay , „ I. Argon, eine neue Form der Atmosphäre “ , Proceedings of the Royal Society of London , vol. 57, 1895, s. 265-287 ( DOI 10.1098 / rspl.1894.0149 , JSTOR 115394 , online lesen )
- (in) John William Strutt und William Ramsay , " VI. Argon, ein neuer Bestandteil der Atmosphäre “ , Philosophical Transactions of the Royal Society of London , 1895, s. 187-241 ( DOI 10.1098 / rsta.1895.0006 , JSTOR 90645 , Bibcode 1895RSPTA.186..187R , online lesen )
- (in) Sir William Ramsay, " The Rare Gases of the Atmosphere " , auf https://www.nobelprize.org/ , Nobelpreis für Chemie , 12. Dezember 1904(Zugriff am 14. Juni 2020 ) .
- (in) John H. Holloway, Edelgaschemie , Methuen,1968, s. 6
- (in) John Emsley, Nature's Building Blocks: An AZ Guide to the Elements , Oxford University Press, 2003, p. 36 . ( ISBN 0198503407 )
- (in) Norman E. Holden, " History of the Origin of the Chemical Elements and Their Discoverers " , 41. IUPAC-Generalversammlung in Brisbane, Australien, 29. Juni - 8. Juli 2001 , unter https://www.nndc.bnl. gov / , Nationales Nukleardatenzentrum , 12. März 2004(Zugriff am 14. Juni 2020 ) .
Siehe auch
Verwandte Artikel
Externe Links
- (de) „ Technische Daten für Argon “ (abgerufen am 24. April 2016 ) , mit den bekannten Daten für jedes Isotop in Unterseiten
- (In) Bilder von Argon in verschiedenen Formen
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | fünfzehn | 16 | 17 | 18 | ||||||||||||||||
| 1 | h | Hey | |||||||||||||||||||||||||||||||
| 2 | Li | Sei | B | VS | NICHT | Ö | F | Geboren | |||||||||||||||||||||||||
| 3 | N / A | Mg | Al | Jawohl | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Dass | SC | Ti | V | Cr | Mn | Fe | Co | Oder | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Ja | Zr | Nb | Mo | Tc | Ru | NS | Pd | Ag | CD | In | Sn | Sb | Sie | ich | Xe | |||||||||||||||
| 6 | Cs | Ba | Das | Dies | Pr | Nd | Uhr | Sm | Hätten | Gott | Tb | Dy | Ho | Er | Tm | Yb | Lesen | Hf | Ihre | W | D | Knochen | Ir | Pt | Bei | Hg | Tl | Pb | Bi | Po | Bei | Rn | |
| 7 | NS | Ra | Ac | NS | Pa | U | Np | Könnten | Bin | Cm | Bk | Vgl | Ist | Fm | Md | Nein | Lr | Rf | Db | Sg | Bh | Hs | Berg | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Alkalimetalle |
alkalische Erde |
Lanthanoide |
Übergangsmetalle |
Schlechte Metalle |
Metal- loids |
Nicht Metalle |
Halo- Gene |
edler Gase |
Nicht klassifizierte Artikel |
| Aktiniden | |||||||||
| Superactiniden | |||||||||