Pyruvatkinase
Die Pyruvatkinase ist eine Phosphotransferase , die die Reaktion katalysiert :
Phosphoenolpyruvat + ADP → ATP + Pyruvat .Dieses Enzym wird in den beteiligten 10 - ten und letzten Stufe der Glykolyse in der Richtung der obigen Reaktion zu katalysieren die Phosphorylierung eines Moleküls von ADP in ATP aus einem Molekül Phosphoenolpyruvat (PEP) zu umgewandelt Pyruvat , unter Verwendung eines Kations von Magnesium Mg 2+ als Cofaktor .
Diese Art der Reaktion wird als Phosphorylierung auf Substratebene bezeichnet . Möglich wird dies durch die große Variation der freien Standardenthalpie der Hydrolyse der Phosphatgruppe von Phosphoenolpyruvat nahe ΔG ° '= - 61,9 kJ · mol -1 . Es ist daher irreversibel, da sein Name nicht anzeigt: Kinasen katalysieren normalerweise die Phosphorylierung des Substrats und nicht die Übertragung einer Phosphatgruppe vom Substrat auf ein anderes Molekül:

|
+ ADP → ATP + |

|
| PEP | Pyruvat |
Isoformen, Regulation und Glukoneogenese
Pyruvatkinase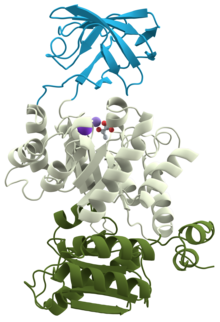 Pyruvatkinase Muskel des Kaninchens , komplexiert mit Mn 2+ , K + und Pyruvat , die drei zeigen Bereiche in blau, weiß und grün ( PDB 1PKN )
Pyruvatkinase Muskel des Kaninchens , komplexiert mit Mn 2+ , K + und Pyruvat , die drei zeigen Bereiche in blau, weiß und grün ( PDB 1PKN )
| EG-Nr. | EG |
|---|---|
| CAS-Nummer | |
| Cofaktor (en) | Mg 2+ , K + |
| IUBMB | IUBMB-Eintrag |
|---|---|
| IntEnz | IntEnz-Ansicht |
| BRENDA | BRENDA Eingang |
| KEGG | KEGG-Eingang |
| MetaCyc | Stoffwechselweg |
| PRIAM | Profil |
| PDB | Strukturen |
| GEHEN | AmiGO / EGO |
Bei Säugetieren wurden drei Haupttypen von Pyruvatkinasen - Isoenzyme - nachgewiesen, die sich durch ihre Regulationsweise unterscheiden:
- Pyruvatkinase vom L-Typ ( Leber ), gefunden in der Leber ; es wird durch ATP und Alanin allosterisch gehemmt und durch Fructose-1,6-bisphosphat aktiviert ; wird durch Phosphorylierung-Dephosphorylierung reguliert, so dass kontrolliertes Hormon unter Verwendung der Proteinkinase A unter der Wirkung von Adrenalin und Glucagon das phosphorylierte Enzym inaktiviert wird.
- Pyruvatkinase M ( PKM1 und PKM2 ), die in Muskeln vorhanden ist und nicht durch Phosphorylierung-Dephosphorylierung reguliert wird,
- Pyruvatkinase A, die in anderen Geweben vorhanden ist, deren Regulation intermediär ist und von den Geweben abhängt.
Eine genetische Mutation in diesem Enzyme kann dazu führen , Pyruvatkinasemangel , eine genetische Krankheit , dass vor allem die Auswirkungen Stoffwechsel von Zellen fehlen Mitochondrien , in denen die Glykolyse zu produzieren Energie in Abwesenheit wesentlich ist ein Krebs - Zyklus . Dies ist insbesondere bei roten Blutkörperchen der Fall , die zu einer hämolytischen Anämie führen können .
Pyruvatkinase ist auch als Schalterenzym für die Glukoneogenese beteiligt , ein Stoffwechselweg in der Leber zur Herstellung von Glukose aus Pyruvat und anderen Substraten. Wenn die Pyruvatkinase durch Phosphorylierung gehemmt wird , beispielsweise während des Fastens unter der Wirkung von Glucagon , verhindert dies die Umwandlung von Phosphoenolpyruvat in Pyruvat und fördert daher dessen Umwandlung in Glucose über Glucagonogenese.
Beziehung zur Pyruvatphosphat-Dikinase
In einigen Bakterien gibt es ein Enzym, das eine ähnliche Funktion erfüllt, Pyruvatphosphat-Dikinase (PPDK), das die Reaktion katalysiert :
Phosphoenolpyruvat + AMP + PP i P i + ATP + Pyruvat .Dieses Enzym, das, im Gegensatz zu Pyruvatkinase, eine reversible Reaktion katalysiert, ist auch in Pflanzen von anaeroben Eukaryonten wie Streblomastix (en) , Giardia , Entamoeba und Trichomonas , die zweifellos die erworben haben entsprechende Gen durch Übertragung. Horizontal Gene auf mindestens zwei Gelegenheiten; Einige dieser Organismen verwenden sowohl Pyruvatkinase als auch Pyruvatphosphatdikinase.
Pyruvatkinase-Fass| Pfam | PF00224 |
|---|---|
| Clan Pfam | CL0151 |
| PROSITÄT | PDOC00101 |
| SCOP | 1pkn |
| SUPERFAMILIE | 1pkn |
Anmerkungen und Referenzen
- Die hier angegebenen Werte für die Masse und die Anzahl der Reste sind diejenigen des Proteinvorläufers, die aus der Translation des Gens vor posttranslationalen Modifikationen resultieren , und können erheblich von den entsprechenden Werten abweichen für das funktionelle Protein .
- (in) freie Energieänderung auf dem Gelände von Marc Kirschner (in) , Harvard Medical School .
- (in) Todd Larsen, Timothy L. Laughlin, Hazel M. Holden, Ivan Rayment und George H. Reed , " Struktur der mit Mn 2+, K + und Pyruvat komplexierten Kaninchenmuskelpyruvatkinase " , Biochemistry , vol. 33, n o 20, Mai 1994, p. 6301-6309 ( PMID 8193145 , DOI 10.1021 / bi00186a033 , online lesen )
- (in) David J. Pocalyko, Lawrence J. Carroll, Brian Martin, Patricia C. Babbitt und Debra Dunaway-Mariano , " Analyse von Sequenzhomologien in pflanzlichem und bakteriellem Pyruvat, Phosphatdikinase, I-Enzym des bakteriellen Phospoenolpyruvats: Zuckerphosphotransferase System und andere PEP-nutzende Enzyme. Identifizierung möglicher katalytischer und regulatorischer Motive “ , Biochemistry , vol. 29, n o 48, Dezember 1990, p. 10757-10765 ( PMID 2176881 , DOI 10.1021 / bi00500a006 , online lesen )

