Pseudomonas aeruginosa
Pseudomonas aeruginosa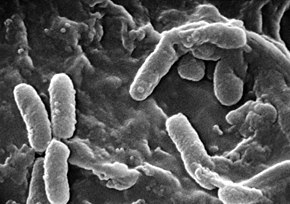 Pseudomonas aeruginosa
Pseudomonas aeruginosa unter dem Rasterelektronenmikroskop
| Herrschaft | Bakterien |
|---|---|
| Einteilung | Proteobakterien |
| Klasse | Gammaproteobakterien |
| Auftrag | Pseudomonaden |
| Familie | Pseudomonadengewächse |
| Nett | Pseudomonas |
( Schroeter , 1872 ) Migula , 1900
Pseudomonas aeruginosa , auch bekannt als Pseudomonas aeruginosa , Bacillus blue pus oder pyo , ist ein gramnegatives Bakterium der Gattung Pseudomonas . Die Bazillen sind dünn, gerade und dank einespolaren Flagellums sehr beweglich: monotriche Zilien, frei von Sporen und Kapseln. Sie treten meist isoliert oder als Diplobacillen auf.
Es kann unter bestimmten Bedingungen pathogen sein . Es ist sehr resistent und wird – zusammen mit anderen gramnegativen Bakterien – immer häufiger für nosokomiale Infektionen verantwortlich . Es ist eines der am schwierigsten klinisch zu behandelnden Bakterien. Die Sterblichkeitsrate erreicht bei gefährdeten Patienten ( immungeschwächt ) 50% .
Allgegenwärtiger Keim , der in Böden und in feuchten Umgebungen (Wolken, Wasserhähne, Stöpsel) lebt, sehr resistent gegen viele Antiseptika , häufig in Krankenhäusern , verursacht das Auftreten (aufgrund seiner Resistenz gegen Antibiotika) echter Krankenhausstämme . Es kann in destilliertem oder gesalzenem Wasser überleben oder sich sogar in bestimmten antiseptischen oder antibiotischen Lösungen entwickeln.
Es ist einer der Keime, nach denen häufig bei einer mikrobiologischen Analyse einer Wasserprobe gesucht wird.
Es wird angenommen, dass es in Krankenhäusern durch die Früchte, Pflanzen und Gemüse, die in sie gelangen, erneuert wird. Dies ist einer der Gründe, warum Blumen und Grünpflanzen in Krankenhauszimmern verboten sind.
Die Krankheitsformen, die es verursacht, sind vielfältig: Infektion des Auges , Wunden (insbesondere Verbrennungen und Operationswunden ), Urin (insbesondere nach Sondierung), Magen-Darm- und Lungen (zB nach Bronchoskopie ), Meningitis- Impfung, Sepsis als Endstadium schwerer Infektionen oder als Komplikation bei Patienten unter immunsuppressiver Behandlung , Leukämie usw. Es induziert leicht systemische Infektionen bei immungeschwächten (durch Chemotherapie oder AIDS ) und bei Opfern von Verbrennungen und Mukoviszidose ( zystische Fibrose ).
Etymologie
Das Wort setzt sich zusammen aus den griechischen Wörtern ψεῦδος ( pseũdos ), „simili“ oder „Nachahmung“ und μόνας ( mónas ), „Einheit“. Es wurde in den Anfängen der Mikrobiologie zur Bezeichnung von „ Keimen “ verwendet. Aeruginosa , das heisst verdigris in Latin (das Ergebnis der Korrosion von Kupfer ), bezieht sich auf ein Pigment , das diese Bakterien enthalten.
Identifizierung
Wie andere Pseudomonas , P. aeruginosa sezerniert eine Reihe von Pigmenten: unter anderem Pyocyanin (blau-grün), Pyoverdin (fluoreszierend gelb-grün) und pyorubin (braun-rot). In vivo bildet es einen Biofilm , die Hauptquelle seiner Resistenz. Es handelt sich um ein laktosenegatives Bakterium , dh ohne Enzyme, die Lactose abbauen , und in vitro mit einem Geruch von Syringa (Blume der Familie Philadelphaceae, auch "Jasmin der Dichter" genannt) versehen . Eine vorläufige Laborerkennung identifiziert seine Kolonien auf Agartyp MacConkey (Agar, der ua Laktose enthält) auf ihr Aussehen perlbeige, während die Kolonien von Bakterien, die Laktose positiv sind, rosa sind. Für eine sichere Identifizierung suchen wir nach Enzymen vom Typ Hydrolase ( ua Elastase und Protease ), die dieses Bakterium absondert. Die Herstellung der beiden Pigmente Pyocyanin und Pyoverdin sowie die optimale Wachstumstemperatur von 42 °C bestätigt die Identifizierung.
P. aeruginosa verwendet Flagellen für die Mobilität, Systeme, die Effektorproteine in Wirtszellen einführen, und ein Lipopolysaccharid, das die Immunantwort des Wirts unterdrückt und zusätzlich direkt in die Etablierung persistenter Infektionen eingreift. Unter den Sekreten von P. aeruginosa gibt es daher Proteine ( Elastase und Protease ), die die Integrität des Wirtsgewebes zerstören, indem sie ihre Proteine wie Elastin , Kollagen und Transferrin abbauen . Es gibt auch Toxine mit niedrigem Molekulargewicht wie Pyocyanin, die verschiedene Stellen in der Wirtszelle beeinflussen.
Wie in Serratia marcescens gibt es Stämme von P. aeruginosa (z. B. Stämme GS9–119, LBI, DS10–129 ... insbesondere in verschmutzten Böden und flüssigen Abfällen der Erdölindustrie zu finden), die ein emulgierendes Tensid ( Glykolipid ) absondern können und ernähren sich von Kohlenwasserstoffen und sind aus diesem Grund eine Quelle des mikrobiellen Abbaus von Diesel , Benzin , Kerosin und sogar Schmierölen , was wahrscheinlich zur Reinigung des durch Kohlenwasserstoffe belasteten Bodens beiträgt.
In Pflanzen, P. aeruginosa induzieren Symptome der Weichfäule (soft rot) in der Ackerschmalwand ( Arabidopsis thaliana ) und Kopfsalat ( Lactuca sativa ). Es ist ein potenter Krankheitserreger bei Arabidopsis und bei bestimmten Tieren: Caenorhabditis elegans , Drosophila und Galleria mellonella . Die Assoziationen von Virulenzfaktoren sind bei Pflanzen- und Tierinfektionen gleich.
Sie sind Gram - Bazillen , oft mit isoliert polar ciliature . Dieses Bakterium hat Oxidase .
- Es ist Atemtyp AS
- Oxidatives VAG.
- Es ist Nitrat - Reduktase +++.
- Glukose -.
- Es produziert kein H 2 S .
- Sie verwendet Mannit .
- Es verwendet das Citrat- Ion als einzige Kohlenstoffquelle .
- Es ist Gelatinase +.
- ADH +, Urease +, Indol –, TDA –.
Auch Isolationsmedien wie Müller-Hinton oder Cetrimid werden verwendet. Auf Müller-Hinton ist die Produktion von Fluorescein ( diffusionsfähiges grünes Farbpigment ) durch das Bakterium zu beobachten. An Cetrimid ist die Produktion von Pyocyanin (diffusibler blauer Farbpigment) durch die Bakterien zu erkennen, wie beispielsweise Resistenzen gegen Cetrimid ( Antiseptikum ) und Nalidixinsäure ( Antibiotikum ).
King A- und King B-Tests können auch durchgeführt werden, um die Produktion von Pyocyanin bzw. Fluorescein zu sehen.
Identifizierungsmatrix von Pseudomonas aeruginosa und fluorescens
-1 = negativ oder abwesend, Zeichen abwesend; 1 = positiv oder Präsenz, Charakter vorhanden; 0 oder freier Speicherplatz = variable Zeichen oder keine Informationen
| Nett | Spezies | Subtyp / Beobachtungen | Oxidase | 42 ° C ( thermophil ) | 4 °C ( kryophil ) | ng A (für Pyoverdin) i | ng B (für Pyocyanin) i | Anderes Pigment | Poly-Beta-Hydroxy-Butyrat | Mobilität | ADH = L-Arginin-DeHydrogenase | NO3 Nitratreduktase (Farbe)> Nitrite (rot) | Gelatinase = Collagenase | Amylase = Stärkehydrolase | Lecithinase = Reaktion auf Eigelb | Lipase ( Tween80 Hydrolyse) | NO2> N2 | Cathécol ortho-Spaltung | Procathénuate ortho-Spaltung | Meta-Spaltung prokathenuieren | Levan (Metaspaltung) hergestellt aus Saccharose | D-Glukose- Assimilation | D-Trehalose- Assimilation | Saccharose- Assimilation | Propionatassimilation | Butyratassimilation | D-Sorbit- Assimilation | Adonitol- Assimilation | Meso-Inositol- Assimilation | Geraniol- Assimilation | L-Valin- Assimilation | D-Alanin- Assimilation | L-Arginin- Assimilation | Arginin | Galle-Esculin-Hydrolyse = (Beta-Glucosidase) | Citrat (von Simmons) | Assimilation von Trinatriumcitrat | D-Glukose- Fermentation | D-Glukose- Assimilation |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pseudomonas | sp | 0,99 | 0,9 | -0,68 | -1 | -1 | -1 | -0,86 | |||||||||||||||||||||||||||||||
| Pseudomonas | aeruginosa | 0,97 | 0,9 | -1 | 0,9 | 0,9 | Pyomelanin = schwarzbraun oder Mahagoni; Pyorubin = Aeruginosin A = Phenazinrot | -1 | 0,94 | 0,7 | 0,92 | 0.84 | -0,9 | -0,9 | 0,1 | 0,9 | 0,9 | 0,9 | -0,9 | -0,9 | 0,98 | -1 | -1 | 0,9 | 0,9 | -0,9 | -1 | -0,9 | 0,9 | 0,1 | 0,9 | 0,9 | -0,98 | 0,98 | -0,38 | 0,98 | |||
| Pseudomonas | fluoreszierend | ich | 0,99 | -1 | 0,98 | 0,9 | -0,9 | -0,9 | -0,9 | 1 | 0,35 | -0,46 | 0,4 | -0,9 | 0,9 | 0,1 | 0,9 | 0,9 | 0,9 | -0,9 | 0,9 | 0,98 | 1 | 0,9 | 0,9 | -0,9 | 0,01 | 0,01 | 0,9 | -0,9 | 0,9 | 0,9 | 0,9 | -0,98 | 0,98 | -0,75 | 0,98 | ||
| Pseudomonas | fluoreszierend | II | 0,99 | -1 | 0,98 | 0,1 | -0,9 | -0,9 | -0,9 | 0,9 | 0,9 | -0,46 | 0,6 | -0,9 | 0,3 | -0,9 | 0,9 | 0,9 | 0,9 | -0,9 | 0,9 | 0,9 | 1 | 0,9 | 0,9 | 0,1 | 1 | -1 | 0,9 | -0,9 | 0,9 | 0,9 | 0,9 | -0,98 | 0,98 | -0,75 | 0,9 | ||
| Pseudomonas | fluoreszierend | III | 0,99 | -1 | 0,98 | 0,9 | -0,9 | -0,9 | -0,9 | 0,9 | 0,9 | -0,46 | -0,22 | -0,9 | 0,9 | 0,1 | 0,9 | 0,9 | 0,9 | -0,9 | -0,9 | 0,9 | 1 | -0,9 | 0,1 | 0,1 | 0,1 | 0,1 | 0,9 | -0,9 | 0,9 | 0,9 | 0,9 | -0,98 | 0,98 | -0,75 | 0,9 | ||
| Pseudomonas | fluoreszierend | IV | 0,99 | -1 | 0,98 | 0,9 | -0,9 | -0,9 | -0,9 | 0,9 | 0,9 | -0,46 | 0,9 | -0,89 | 0,9 | 0,1 | 0,9 | 0,9 | 0,9 | -0,9 | 0,9 | 0,9 | 1 | 0,9 | 0,9 | 0,9 | 0,9 | -0,9 | 0,9 | -0,9 | 1 | 1 | 1 | -0,98 | 0,98 | -0,75 | 0,9 | ||
| Pseudomonas | fluoreszierend | V | 0,99 | -1 | 0,5 | 0,1 | -0,9 | -0,9 | -0,9 | 0,9 | 0,9 | -0,46 | 0,9 | -0,9 | 0,1 | 0,1 | 0,9 | 0,9 | 0,9 | -0,9 | -0,9 | 0,98 | 1 | 0,1 | 0,9 | 0,1 | 0,1 | 0,2 | 0,9 | -0,9 | 0,9 | -0,9 | 0,9 | -0,98 | 0,98 | -0,75 | 0,98 |
Behandlungen
Antibiotika und Antibiotikaresistenz
P. aeruginosa ist ein robustes Bakterium, das von Natur aus sehr resistent gegen Antibiotika ist und sich schnell an Medikamentenangriffe anpasst.
Ohne Selektion oder Verstärkung durch vorangegangene Antibiotikatherapien wird es oft nur auf wenige Antibiotika empfindlich reagieren: Ticarcillin mit Clavulansäure , Gentamicin , Ciprofloxacin , Ceftazidim und Piperacillin allein oder unter Zusatz von Tazobactam und Borsäure . 2008 waren Fluorchinolone , Gentamicin oder Imipenem noch wirksam, allerdings nur bei wenigen Bakterienstämmen.
Hat der Patient kürzlich mehrere Antibiotika bekommen, sind die Bakterien wahrscheinlich noch resistenter und umso gefährlicher. Diese Antibiotikaresistenz wurde teilweise auf " Effluxpumpen " in seinem Biofilm zurückgeführt , die die antimikrobiellen Komponenten aktiv ausstoßen. P aeruginosa ist auch dafür bekannt, Duox- Proteine anzugreifen, die die Bausteine des Abwehrsystems der Lunge sind .
Bei Resistenzen gegen die zuvor genannten Antibiotika können die Kombinationen Ceftazidim / Avibactam (Handelsname: Zavicefta ) und Ceftolozan / Tazobactam (Handelsname: Zerbaxa ) wirksam sein. Die Colistin ist das Mittel der letzten Ausweg angesichts der Keime Gram-negative Mehr resistent gegen Antibiotika wie Pseudomonas aeruginosa .
Bakteriophagen-Behandlungen
Die Phagentherapie wird in Frankreich und anderen Ländern Europas wenig verwendet , wird jedoch in den ehemaligen Sowjetrepubliken und in geringerem Maße in Polen häufig gegen Pseudomonas aeruginosa eingesetzt . In Frankreich müssen Ärzte mangels eines zugelassenen Arzneimittels (das aus wirtschaftlichen Gründen bis zum Verschwinden der Bakteriophagen-Laboratorien existierte ) für jeden mit einem ausländischen Arzneimittel behandelten Patienten auf spezielle Genehmigungen zurückgreifen, aber die Phagentherapie an sich ist nicht verboten. die von der ANSM im Jahr 2019 bestätigt wurde . Ein weiterer legaler Weg in Frankreich, der jedoch seit den 1980er Jahren nicht mehr verwendet wird, ist die improvisierte Herstellung von Bakteriophagen- Magistralpräparaten , die bis in die 1980er Jahre am Institut Pasteur in Paris, Straßburg oder Lyon für die resistentesten Bakterien durchgeführt wurde und insbesondere für P. aeruginosa .
Die Bakteriophagen gegen P. aeruginosa liegen in Form eines flüssigen Cocktails von Phagen vor, die spezifisch für den Angriff auf die Bakterien sind. Pseudomonas aeruginosa ist im Allgemeinen eines der Ziele der in diesen Ländern erhältlichen Breitspektrum-Bakterien-Phagen-Cocktails ( Pyobacteriophage , Intestibacteriophage ). Es gibt auch andere Cocktails, die für dieses Bakterium spezifisch sind.
Die guten Ergebnisse haben die Aufmerksamkeit der Westler auf sich gezogen und viele Forschungsprojekte zum Einsatz von Bakteriophagen gegen Pseudomonas aeruginos laufen sowohl in Amerika als auch in Europa, der Entwurf Phagoburn (in) das Verbrennungs- und PneumoPhage- Projekt für Atemwegsinfektionen.
Konfrontiert mit Situationen einer therapeutischen Sackgasse, kommen Patienten, die einer Infektion mit multiresistenten P. aeruginosa zum Opfer gefallen sind , zusammen, um den Zugang zu Behandlungen mit fremden Bakteriophagen zu erleichtern.
Der erste Bakteriophage gegen P. aeruginosa , der in französischen Arzneimittelempfehlungsstellen auftaucht , ist P. aeruginosa PHAGE PP113 , der nur bei ATUn erhältlich ist .
Ansteckung
Dieses Bakterium scheint leicht durch Wasser, Luft und Partikel (Staub) oder kontaminierte Oberflächen ( fomites ) transportiert werden zu können. Die Ansteckungsgefahr erklärt sich durch seine allgegenwärtige Natur und - in einer Krankenhausumgebung - durch die Tatsache, dass es leicht „Antibiotikaresistenz“-Gene von anderen Bakterien verwandter Stämme, aber auch von entfernteren Arten übertragen oder erwerben kann.
Seine Entwicklungsumgebung: der Biofilm
Arten der Gattung Pseudomonas sind weit verbreitet und kommen in den meisten terrestrischen Ökosystemen vor, mit Ausnahme bestimmter extremer Umgebungen wie Umgebungen mit sehr hohen Temperaturen. P. aeruginosa ist die am besten untersuchte Art, insbesondere in Bezug auf die geografische Verbreitung.
In seiner freien Form ist es in Böden nicht sehr konkurrenzfähig, zeigt aber eine gewisse Anziehungskraft auf Wasserumgebungen. Tatsächlich besitzt es aufgrund seiner Fähigkeit, in einer oligotrophen, dh nährstoffarmen Umgebung zu überleben und zahlreichen Bioziden, Produkten, die Schadorganismen abtöten, abwehren oder unschädlich machen sollen, zu widerstehen, ein hohes Potenzial zur Besiedelung nasser Oberflächen.
P. aeruginosa wächst wie einige andere gramnegative Bakterien als strukturierte Aggregate, die Biofilme genannt werden , wobei seine Zellen mit einer Matrix aus komplexen extrazellulären Polymeren beschichtet sind. Diese Biofilme bilden eine physikalische Barriere gegen das Eindringen antimikrobieller Wirkstoffe und sind teilweise verantwortlich für persistierende Lungeninfektionen durch P. aeruginosa bei immungeschwächten Patienten mit Mukoviszidose . Die Bildung von und durch den Biofilm wird durch Signale von Zelle zu Zelle und durch Quorum-Sensing kontrollierte Mechanismen gesteuert, die auf dem Konzept der „Quoten-Wahrnehmung“ (Quorum-Sensing) und der „ kritischen Masse “ basieren : Natur und damit die Funktion von Molekülen, die Zellen signalisieren -Der Zellaustausch ändert sich ab einer bestimmten Bakterienkonzentration. Die in einem Biofilm vorhandenen Bakterien sind weniger stoffwechselaktiv und daher weniger empfänglich für antimikrobielle Wirkstoffe und Umwelteinflüsse. Der Biofilm spielt eine aktive Rolle bei der Kommunikation zwischen Bakterienzellen.
Sobald diese Biofilme fixiert sind, setzen sie Bakterien in mehr oder weniger beabstandeten Frequenzen in den Körper frei, folglich ist der infizierte Patient aufgrund der Omnipräsenz von P. aeruginosa schwer zu behandeln.
So findet sich P. aeruginosa in Rohrleitungen, öffentlichen Wasserversorgungsnetzen (EDV), Abwasser, Wasserhähnen, Siphons sowie Gegenständen und Handtüchern im Krankenhausumfeld oder in medizinischen Geräten, die Flüssigkeiten enthalten (künstliche Atemluftbefeuchter). Auf diese Weise kann diese Art von Bakterien insbesondere die in der Abfüllindustrie vorhandenen Mineralwässer besiedeln und bei mehreren Verbrauchern Verunreinigungen verursachen. Es kann auch bestimmte Lebensmittel wie Rohmilch oder Käse und manchmal Gemüse, insbesondere in Wasser gewaschene Salate und Pilze, kontaminieren.
Das in der Schleimhaut vorhandene Lactoferrin reduziert die Biofilmbildung in Pseudomonas aeruginosa , die vor anhaltenden Infektionen schützen kann. Geforscht werden Behandlungen durch die Destrukturierung von Biofilmen, die Hemmung bekannter Virulenzfaktoren durch den Abbau von Botenenzymen und die Regulation von Genen, die interzelluläre Signale und Quorum Sensing Mechanismen steuern .
P. aeruginosa und Salicylsäure
Die Salicylsäure ist ein phenolischer Metabolit, der von Pflanzen produziert wird. Es spielt insbesondere eine Rolle bei der Induktion der Abwehrreaktion von Pflanzen gegen pathogene Angriffe. Arbeiten mit Arabidopsis thaliana Pflanzen und mit Caenorhabditis elegans Tieren , Cryz et al. (1984) zeigten, dass Arabidopsis t. genetisch modifiziert ( lox2 und cpr5-2 ), um mehr Salicylsäure zu produzieren, die Bildung und Anheftung des Biofilms von P. aeruginosa PA14 an ihren Wurzeln zu reduzieren. Die gleiche Wirkung wurde bei wilder Arabidopsis gezeigt, die mit Salicylsäure (die die innere Konzentration dieser Säure in der Pflanze erhöht) angereichert wurde.
Salicylsäure beeinflusst drei bekannte Virulenzfaktoren von PA14: Pyocyanin, Protease und Elastase. P. aeruginosa produziert mehr Pyocyanin, wenn der Wirt gentechnisch verändert wird (transgene NahG-Linie), um weniger Salicylsäure anzureichern als die natürliche Pflanze. Salicylsäure hemmt daher die Synthese und Sekretion von Pyocyanin in vivo .
P. aeruginosa- Zellen, die in einer pepton-tryptischen Sojakultur gezüchtet wurden, zeigen eine 50%ige Verringerung der Elastase- und Protease-Aktivität, wenn Salicylsäure oder Derivate hinzugefügt werden: Acetylsalicylsäure, Salicylamid, Methylsalicylsäure; oder auch Benzoesäure , eine metabolische Vorstufe von Salicylsäure.
Salicylsäure, die mit P. aeruginosa infizierten Rasen zugesetzt wurde, verringerte die Fähigkeit von P. aeruginosa , Würmer abzutöten, ohne die Ansammlung von Bakterien im Nematodendarm zu verringern . Salicylsäure würde daher direkt auf P. aeruginosa wirken und die Virulenzfaktoren der Bakterien reduzieren.
Durch Microarray analysiert , zeigt sich, dass Salicylsäure die physiologische Expression von 331 Genen in P. aeruginosa beeinflusst, indem sie selektiv die Transkription von Exoproteinen und anderen Virulenzfaktoren unterdrückt, wodurch ihre Virulenz reduziert wird, ohne die Gene des Interviews zu beeinträchtigen. Dies kommt zusätzlich zu seiner bekannten Rolle als Signalmolekül zur Aktivierung des pflanzlichen Abwehrsystems hinzu.
Schwellenwerte oder Grenzwerte
Frankreich Das Dekret von 14. März 2007hinsichtlich der Qualitätskriterien von abgepacktem Wasser, die Behandlung und besondere Kennzeichnung von natürlichem Mineralwasser und abgepackter Quelle sowie von in öffentlichen Erfrischungen verteiltem natürlichem Mineralwasser erfordert für Pseudomonas aeruginosa eine Anzahl von Nullkeimen pro 250 ml beim Auflaufen und während der Vermarktung (Analysen mindestens drei Tage nach der Entnahme im Einzugsgebiet beginnen, Konditionierung mit bei Raumtemperatur gelagerten Proben).Pseudomonas aeruginosa- Infektion
Es ist möglich, sich beim Menschen mit Pseudomonas aeruginosa zu infizieren . Es ist in der Regel ein Krankenhauskeim, der für nosokomiale Infektionen verantwortlich ist , wird aber auch ambulant bei Patienten mit Mukoviszidose gefunden . Es kann auch bei einer Otitis externa vom äußeren Gehörgang isoliert werden.
Pseudomonas aeruginosa ist gegen eine Vielzahl von Antibiotika resistent. Sie sollten daher niemals als Monotherapie behandelt werden. Gegen P. aeruginosa wirksame Antibiotika sind Carbapeneme, bestimmte Fluorchinolone (ein Beispiel hochdosiertes Ciprofloxacin), bestimmte Penicilline (Piperacillin-Tazobactam) sowie Cephalosporine der dritten Generation (z. B. Ceftazidim)
.
Forschung
Ein AEROPATH- Projekt zielt darauf ab, wirksame Antibiotika gegen Antibiotika zu entwickeln, die antibiotikaresistent gegen Multi-Drug-Behandlungen sind, die nosokomiale Epidemien aufrechterhalten, und Pseudomonas aeruginosa steht im Mittelpunkt dieser Arbeit, die durch die Untersuchung und auch Modellierung von Schwachstellen im Stoffwechsel und Proteinen durchgeführt wird. von P. aeruginosa und nosokomialen Stämmen von Stenotrophomonas und Acinetobacter , einschließlich durch das Studium ihrer Genome.
Andere suchen nach alternativen Behandlungen (Impfung mit einem weniger gefährlichen mikrobiellen Stamm, der den Raum einnehmen würde, ohne Pseudomonas zu weichen, oder mikrobielle Ökologie ). Schließlich gibt es noch andere Ansätze wie Astikotherapie , Phytotherapie usw. Eine an der Universität Johannesburg verteidigte Dissertation (2020) hat gezeigt, dass der Guavenextrakt ( Psidium guajava ) L. das Wachstum von P. aeruginosa in vitro hemmt .
Hinweise und Referenzen
- [PDF] S. Mans, D r S. Canouet, „ Pseudomonas aeruginosa: Eine Wassergeschichte “ , auf www.cclin-sudouest.com , Koordinierungszentrum für den Kampf gegen nosokomiale Infektionen im Südwesten ,27. März 2008(Zugriff am 5. November 2013 )
- Manchmal hat der Keim kein Pyocyanin oder gar kein Fluorescein, das für die fluoreszierende Gruppe charakteristisch ist → verlassen Sie sich nicht nur auf das Aussehen der Kultur; für das Wachstum bei 42 °C immer eine Kontrollbrühe bei 37 °C herstellen, da der Stamm tot sein kann und ohne Kontrolle könnte man meinen, der Wachstumstest bei 42 °C sei negativ, obwohl der Keim tatsächlich tot ist.
- [1] , Cryz, SJ, Jr., TL Pitt, E. Furer und R. Germanier, 1984, Role of lipopolysaccharide in virulence of Pseudomonas aeruginosa. Infizieren. Immun. 44: 508-513
- Aumercier, M., Murray DM und Rosner JL, 1990, Potentiation of susceptibility to aminoglycosides by salicylates in Escherichia coli. Antimikrob. Agenten Chemother, 23: 835-845
- Kawaharajo, K., JY Homma, Y. Aoyama, K. Okada, K. Morihara, 1975, Effekte von Protease und Elastase aus Pseudomonas aeruginosa auf die Haut. Jpn. J. Erw. Med. 45: 79-88
- Lau, GW, H. Ran, F. Kong, DJ Hassett und D. Mavrodi, 2004, Pseudomonas aeruginosa Pyocyanin ist entscheidend für eine Lungeninfektion bei Mäusen. Infizieren. Immun. 72: 4275-4278
- Ran, H., DJ Hassett und GW Lau, 2003, Human Targets of Pseudomonas aeruginosa Pyocyanin. Proz. Natl. Akad. Wissenschaft USA 100: 14315-14320
- Wei, YH, Chou, CL, & Chang, JS (2005). Rhamnolipid-Produktion durch einheimische Pseudomonas aeruginosa J4 aus petrochemischem Abwasser . Biochemical Engineering Journal, 27 (2), 146-154 ( Zusammenfassung ).
- Rahman, KSM, Rahman, TJ, McClean, S., Marchant, R. & Banat, IM (2002) [Rhamnolipid-Biotensidproduktion durch Stämme von Pseudomonas aeruginosa unter Verwendung kostengünstiger Rohstoffe] . Biotechnologischer Fortschritt, 18 (6), 1277-1281.
- Wongsa, P., Tanaka, M., Ueno, A., Hasanuzzaman, M., Yumoto, I. & Okuyama, H. (2004). Isolierung und Charakterisierung neuer Stämme von Pseudomonas aeruginosa und Serratia marcescens mit hoher Effizienz beim Abbau von Benzin, Kerosin, Dieselöl und Schmieröl . Aktuelle Mikrobiologie, 49 (6), 415-422.
- Hong, JH, Kim, J., Choi, OK, Cho, KS & Ryu, HW (2005) Charakterisierung eines dieselabbauenden Bakteriums, Pseudomonas aeruginosa IU5, isoliert aus ölverseuchtem Boden in Korea . World Journal of Microbiology and Biotechnology, 21 (3), 381-384.
- Rahme, L., E. Stevens, S. Wolfort, J. Shao, R. Tompkins und FM Ausubel. 1995. Gemeinsame Virulenzfaktoren für bakterielle Pathogenität bei Pflanzen und Tieren. Wissenschaft 268: 1899-1902
- Rahme, LG, MW. Tan, L. Le, SM Wong, RG Tompkins, SB Calderwood und FM Ausubel, 1997, Verwendung von Modellpflanzenwirten zur Identifizierung von Pseudomonas aeruginosa-Virulenzfaktoren. Proz. Natl. Akad. Wissenschaft USA 94: 13245-13250
- Walker, TS, HP Bais, E. Déziel, HP Schweizer, LG Rahme, R. Fall und JM Vivanco. 2004. Pseudomonas aeruginosa-Pflanzenwurzel-Interaktionen. Pathogenität, Biofilmbildung und Wurzelexsudation. Pflanzenphysiologie. 134: 320-331
- Mahajan-Miklos, S., MW Tan, LG Rahme und FM Ausubel. 1999. Molekulare Mechanismen bakterieller Virulenz aufgeklärt unter Verwendung eines Pseudomonas aeruginosa-Caenorhabdititis elegans-Pathogenesemodells. Zelle 96: 47-56
- Martinez, C., E. Pons, G. Prats und J. Leon. 2004. Salicylsäure reguliert die Blütezeit und verknüpft Abwehrreaktionen und Fortpflanzungsentwicklung. Plant J. . 37: 209-217
- D'Argenio, DA, LA Gallagher, CA Berg und C. Manoil. 2001. Drosophila als Modellwirt für Pseudomonas aeruginosa-Infektion. J. Bakteriol. 183: 1466-1471
- Miyata, S., M. Casey, DW Frank, FM Ausubel und E. Drenkard., 2003, Verwendung der Galleria mellonella-Raupe als Modellwirt zur Untersuchung der Rolle des Typ-III-Sekretionssystems bei der Pathogenese von Pseudomonas aeruginosa. Infizieren. Immun. 71: 2404-2413
- Rahme, LG, FM Ausubel, H. Cao, E. Drenkard, BC Goumnerov, GW Lau, S. Mahajan-Miklos, J. Plotnikova, MW Tan, J. Tsongalis, CL Walendziewicz und RG Tompkins, 2000, Plants and Tiere teilen funktionell gemeinsame bakterielle Virulenzfaktoren. Proz. Natl. Akad. Wissenschaft USA 97: 8815-8821
- (in) George M. Garrity , Julia A. Bell und Timothy Lilburn , "Pseudomonadales Orla-Jensen 1921, 270AL" in Bergeys MANUAL® of Systematic Bacteriology: The Proteobacteria Volume Two Part B The Gammaproteobacteria Springer US,2005( ISBN 9780387280226 , DOI 10.1007 / 0-387-28022-7_9 , online lesen ) , S . 323-442.
- Cordis Pressemitteilung , Europa, im November 2008
- Aeschlimann, JR 2003, Die Rolle von Multidrug-Efflux-Pumpen bei der Antibiotikaresistenz von Pseudomonas aeruginosa und anderen gramnegativen Bakterien: Erkenntnisse der Society of Infectious Diseases Pharmacists. Pharmakotherapie 23: 916-924
- Von Kievit, TR, MD Parkins, RJ Gillis, R. Srikumar, H. Ceri, K. Poole, BH Iglewski und DG Storey, 2001, Multidrug - Efflux - Pumpen: Expressionsmuster und Beitrag zur Antibiotika - Resistenz in Pseudomonas aeruginosa Biofilme. Antimikrob. Chemother-Agenten. 45: 1761-1770
- Poole, K. 2001, Multidrug-Efflux-Pumpen und antimikrobielle Resistenz bei Pseudomonas aeruginosa und verwandten Organismen. J.Mol. Mikrobiol. Biotechn. 3: 255-264
- Rada B, Lekstrom K, Damian S, Dupuy C, Leto TL. Das Pseudomonas-Toxin Pyocyanin hemmt das duale Oxidase-basierte antimikrobielle System, da es den Epithelzellen der Atemwege oxidativen Stress auferlegt. J Immunol . 1. Oktober 2008, 181 (7): 4883-93. http://www.jimmunol.org/cgi/reprint/181/7/4883
- Rada B, Leto TL. Redoxkrieg zwischen Atemwegsepithelzellen und Pseudomonas: duale Oxidase versus Pyocyanin. Immunol. Res. 2008. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2776630/pdf/nihms-156213.pdf
- Doktor Paul-Hervé Riche, Handbuch der Phagentherapie für Ärzte des 21. Jahrhunderts , Nîmes, W3edition.com,2013, 260 S. ( ISBN 978-2-9544885-0-9 ) , S. 236-238-
- Nationale Agentur für die Sicherheit von Arzneimitteln und Gesundheitsprodukten, " CSST Phagothérapie - Feedback und Perspektiven " [PDF] , auf ansm.sante.fr ,21. März 2019(Zugriff am 20. Februar 2018 )
- Jacques Charpin, " Bericht - Über den Antrag auf Genehmigung zur Herstellung von Bakteriophagen und therapeutischen Impfstoffen, vorgelegt von MM Pérouse de Montclos, Drouet, Denoyel und Mme Richoud ", Bulletin de l'Académie Nationale de Médecine ,26. Januar 1988, s. 115-116 ( online lesen )
- Pascale Cossart , The new microbiology: from microbiota to CRISPR , Paris, Odile Jacob editions , coll. "Wissenschaften",2016, 255 S. ( ISBN 978-2-7381-3331-1 und 2738133312 , OCLC 951.732.499 , Bekanntmachung BnF n o FRBNF45061401 ) , "La phagothérapie".
- Elaine M. Waters , Daniel R. Neill , Basak Kaman und Jaspreet S. Sahota , „Die Phagentherapie ist hochwirksam gegen chronische Lungeninfektionen mit Pseudomonas aeruginosa “, Thorax , vol. 72, n O 7,Juli 2017, s. 666–667 ( ISSN 1468-3296 , PMID 28265031 , PMCID PMC5520275 , DOI 10.1136 / thoraxjnl-2016-209265 , online gelesen , abgerufen am 23. April 2018 )
- Anne Jeanblanc , " Bakteriophagen gegen Antibiotikaresistenz ", Le Point ,22. Februar 2016( online lesen , eingesehen am 23. April 2018 )
- " Europäische Kommission: CORDIS: Projekte und Ergebnisse: Zusammenfassung des Abschlussberichts - PHAGOBURN (Evaluation of Phagen Therapy for the Treatment of Escherichia coli and Pseudomonas aeruginosa burn Wundinfektionen (Phase I-II klinische Studie)) " , auf cordis.europa.eu (Zugriff am 23. April 2018 )
- „ http://www.pherecydes-pharma.com/pneumophage.html “ , auf www.pherecydes-pharma.com (Zugriff am 26. April 2018 )
- " Phagen-Sans-Frontières - Gemeinsam können wir versuchen, das Schicksal zu ändern!" » , Auf phages-sans-frontieres.com (Zugriff am 24. April 2018 )
- " EuroPhages - Das Leben Tausender Franzosen dank Bakteriophagen retten " , auf EuroPhages (Zugriff am 24. April 2018 )
- " Association PHAG ESPOIRS " , auf Association PHAG ESPOIRS (abgerufen am 24. April 2018 )
- " P. aeruginosa-Phage PP1131, Lösung zur lokalen Anwendung " , auf doctissimo.fr , Doctissimo
- P r Gunter Schneider vom Karolinska-Institut , in der von Cordis zitierten Stellungnahme vom November 2008.
- G. A. O'Toole, LA Pratt, PI Watnick, DK Newman, VB Weaver und R. Kolter, „ Genetic approach to study of biofilms “, Methods Enzymol. , Bd. 310,1999, s. 91-109 ( DOI 10.1016 / S0076-6879 (99) 10008-9 )
- Costerton, JW, 2001, Pathogenese der Mukoviszidose und die Rolle von Biofilmen bei persistierenden Infektionen. Trends Mikrobiol. 9: 50-52
- Hall-Stoodley, L., JW Costerton und P. Stoodley, 2004, Bakterielle Biofilme: von der natürlichen Umgebung zu Infektionskrankheiten. Nat. Rev. Mikrobiol. 2: 95-108
- Singh, PK, MR Parsek, EP Greenberg und MJ Welsh, 2002, Eine Komponente der angeborenen Immunität verhindert die bakterielle Biofilmentwicklung. Natur 417: 552-555
- Singh, PK, AL Schäfer, MR Parsek, TO Moninger, MJ Welsh und EP Greenberg. 2000. Quorum-sensing-Signale weisen darauf hin, dass Mukoviszidose-Lungen mit bakteriellen Biofilmen infiziert sind. Natur 407: 762-764
- Davies, DG, MR Parsek, JP Pearson, BH Iglewski, JW Costerton und EP Greenberg, 1998, Die Beteiligung von Signalen von Zelle zu Zelle an der Entwicklung eines bakteriellen Biofilms. Wissenschaft 280: 295-298
- Mah, T.-F., B. Pitts, B. Pellock, GC Walker, PS Stewart und GA O'Toole, 2003, Eine genetische Grundlage für die Antibiotikaresistenz von Pseudomonas aeruginosa biofilm. Natur 426: 306-310
- Parsek, MR, und PK Singh, 2003, Bakterielle Biofilme: eine neue Verbindung zur Krankheitspathogenese. Annu. Rev. Mikrobiol. 57: 677-701
- Smith, RS und BH Iglewski, 2003, P. aeruginosa Quorum Sensing Systems and Virulence. Curr. Meinung. Mikrobiol. 6: 56-60
- Drenkard, E. 2003, Antimikrobielle Resistenz von Pseudomonas aeruginosa-Biofilmen. Mikrob. Infizieren. 5: 1213-1219
- Hentzer, M. und M. Givskov, 2003, Pharmakologische Hemmung des Quorum Sensing zur Behandlung chronischer bakterieller Infektionen. J. Clin. Investieren. 112: 1300-1307
- Hentzer, M., L. Eberl, J. Nielsen und M. Givskov. 2003. Quorum Sensing: ein neuartiges Ziel für die Behandlung von Biofilminfektionen. BioDrugs 17: 241-250
- Hentzer, M., M. Givskov und L. Eberl. 2004. Quorum Sensing in Biofilmen: Klatsch in der Schleimstadt. Mikrob. Biofilme 1: 118-140
- Hentzer, M., H. Wu, JB Andersen, K. Riedel, TB Rasmussen, N. Bagge, N. Kumar, MA Schembri, Z. Song, P. Kristoffersen, M. Manefield, JW Costerton, S. Molin, L. Eberl, P. Steinberg, S. Kjelleberg, N. Hoiby und M. Givskov, 2003, Attenuation of Pseudomonas aeruginosa virulence by Quorum Sensing Inhibitors. EMBO J. 22: 3803-3815
- Wu, H., Z. Song, M. Hentzer, JB Andersen, S. Molin, M. Givskov und N. Hoiby. 2004. Synthetische Furanone hemmen das Quorum-Sensing und verbessern die bakterielle Clearance bei Pseudomonas aeruginosa-Lungeninfektionen bei Mäusen. J. Antimikrob. Chemother. 53: 1054-1061
- Verordnung vom 14. März 2007 über die Qualitätskriterien von verpacktem Wasser, Behandlung und besondere Kennzeichnung von natürlichem Mineral- und Quellwasser sowie von natürlichem Mineralwasser, das in öffentlichen Erfrischungen verteilt wird, ABl. Nr. 81 vom 5. April 2007, Seite 6431
- PharmaWiki.ch
- Projekt koordiniert von der University of Dundee (Vereinigtes Königreich), mit Deutsch, Englisch und Schwedisch - Teams, die von der EU in Höhe finanziert werden (im Jahr 2008) von 4,6 Millionen Euro, über das Siebte Rahmenprogramm ( 7 th PC)
- (in) Celeste Vermaak, Die Wirkung von Psidium guajava L. (Kräuterextrakt, Urtinktur und 3CH) ist multiresistente Pseudomonas aeruginosa in vitro , Johannesburg, Fakultät für Gesundheitswissenschaften,Dezember 2020, 120 S. ( online lesen ) , Abschlussarbeit