Isoflavon
Die Isoflavone sind eine Unterfamilie von Flavonoiden, die weitgehend auf ihre Pseudo-Eigenschaften Östrogen untersucht wurden . Dies sind die Isomere von Flavonen mit einer nahezu identischen Struktur. Der einzige Unterschied besteht in der Position der Phenylgruppe, die an Kohlenstoff 3 anstelle von Kohlenstoff 2 für Flavone gebunden ist.
Hauptisoflavone
| Nachname | Struktur | R 5 | R 6 | R 7 | R 8 | R 3 ' | R 4 ' | R 5 ' | FALL | IUPAC-Name |
|---|---|---|---|---|---|---|---|---|---|---|
| Isoflavon | 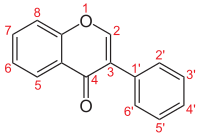 |
H. | H. | H. | H. | H. | H. | H. | 3-Phenylchromen-4-on | |
| Biochanin A. | OH | H. | OH | H. | H. | OCH 3 | H. | 5,7-Dihydroxy-3- (4-methoxyphenyl) chromen-4-on | ||
| Calycosin | H. | H. | OH | H. | OH | OCH 3 | H. | 7-Hydroxy-3- (3-hydroxy-4-methoxyphenyl) chromen-4-on | ||
| Daidzein | H. | H. | OH | H. | H. | OH | H. | 7-Hydroxy-3- (4-hydroxyphenyl) chromen-4-on | ||
| Formononetin | H. | H. | OH | H. | H. | OCH 3 | H. | 7-Hydroxy-3- (4-methoxyphenyl) chromen-4-on | ||
| Genistein | OH | H. | OH | H. | H. | OH | H. | 5,7-Dihydroxy-3- (4-hydroxyphenyl) -4H-chromen-4-on | ||
| Glycitein | H. | OCH 3 | OH | H. | H. | OH | H. | 7-Hydroxy-3- (4-hydroxyphenyl) -6-methoxy-4-chromenon | ||
| Irigenin | OH | OCH 3 | OH | H. | OH | OCH 3 | OCH 3 | 5,7-Dihydroxy-3- (3-hydroxy-4,5-dimethoxyphenyl) -6-methoxychromen-4-on | ||
| 5-O-Methylgenistein | OCH 3 | H. | OH | H. | H. | OH | H. | 7-Hydroxy-3- (4-hydroxyphenyl) -5-methoxychromen-4-on | ||
| Orobol | OH | H. | OH | H. | OH | OH | H. | 3- (3,4-Dihydroxyphenyl) -5,7-dihydroxychromen-4-on | ||
| Pratensein | OH | H. | OH | H. | OH | OCH 3 | H. | 5,7-Dihydroxy-3- (3-hydroxy-4-methoxyphenyl) chromen-4-on | ||
| Prunetin | OH | H. | OCH 3 | H. | H. | OH | H. | 5-Hydroxy-3- (4-hydroxyphenyl) -7-methoxychromen-4-on | ||
| Psi-Tectorigenin | OH | H. | OH | OCH 3 | H. | OH | H. | 5,7-Dihydroxy-3- (4-hydroxyphenyl) -8-methoxychromen-4-on | ||
| Retusine | H. | H. | OH | OH | H. | OCH 3 | H. | 7,8-Dihydroxy-3- (4-methoxyphenyl) chromen-4-on | ||
| Sandelholz | OH | H. | OCH 3 | H. | OH | OH | H. | 5-Hydroxy-3- (3,4-dihydroxyphenyl) -7-methoxychromen-4-on | ||
| Tectorigenin | OH | OCH 3 | OH | H. | H. | OH | H. | 5,7-Dihydroxy-3- (4-hydroxyphenyl) -6-methoxychromen-4-on |
Natürliches Vorkommen
Isoflavone sind in allen Pflanzen vorhanden, aber nur Pflanzen der Familie der Fabaceae ("Hülsenfrüchte") enthalten signifikante Mengen an Isoflavonen. Durchgeführte Analysen mit vielen Arten haben gezeigt , dass die höchsten Ebenen von Genistein und Daidzein - die häufigsten Isoflavone in der Natur - finden sich in psoralea ( Psoralea corylifolia ). Viele Hülsenfrüchte, einschließlich Sojabohnen (Glycine max L.), grüne Bohnen (Phaseolus vulgaris L.), Luzerne- Sprossen (Medicago sativa L.), Mungbohnen (Vigna radiata L.), Voeme (Vigna unguiculata L.), Kudzu- Wurzeln ( Pueraria lobata L.) sowie die Blüte und der Spross von Wiesenklee (Trifolium pratense L.) wurden auf ihre östrogene Aktivität untersucht . Hochverarbeitete Lebensmittel aus Hülsenfrüchten wie Tofu behalten den größten Teil ihres Isoflavongehalts bei, mit Ausnahme von fermentiertem Miso mit höheren Gehalten.
Unter den anderen Nahrungsquellen für Isoflavone können Kichererbsen ( Biochanin A ), Luzerne ( Formononetin ) und Erdnüsse ( Genistein ) erwähnt werden.
In Pflanzengeweben sind die am häufigsten vorkommenden Isoflavone die Heteroside von Isoflavonen oder ihren jeweiligen Malonaten oder Acetylkonjugaten, wodurch sie in Wasser noch löslicher werden (siehe Isoflavon-7-O-beta-Glucosid-6 "-O-Malonyltransferase ) letztere Formen sind jedoch instabil und werden daher beispielsweise durch Decarboxylierung umgewandelt . Wenn Hülsenfrüchte mit einer Virus- oder Pilzinfektion fertig werden müssen, wird häufig die wasserlösliche Form zum Transport verwendet und am entsprechenden zu dem entsprechenden Aglycon hydrolysiert Zielseite.
Das Actein und das Cimicifucosid sind zwei Isoflavon- Triterpene, die in der Actaea racemosa vorhanden sind .
Es gibt eine Datenbank mit Isoflavongehalten vieler Lebensmittelprodukte.
Biosynthese
Isoflavone werden über einen Zweig des allgemeinen Phenylpropanoid-Weges biosynthetisiert , der insbesondere in höheren Pflanzen Flavonoide produziert . Dieser Weg beginnt mit einer Aminosäure , Phenylalanin, die in Zimtsäure oder eines ihrer Derivate umgewandelt wird und selbst in ein Derivat der Paracoumarsäure umgewandelt wird, das ein Chalkon ergibt , den Vorläufer der meisten Flavonoide. In der Natur sind die Hauptisoflavone, die in Sojabohnen vorkommen , Genistein und Daidzein . Das erste wird aus Naringinin hergestellt , einem Flavanon (Flavonoid), das durch die Wirkung von zwei spezifischen Enzymen, Isoflavon-Synthase und Dehydratase, umgewandelt wird . In ähnlicher Weise wird Naringinin-Chalcon durch die aufeinanderfolgende Wirkung von drei spezifischen Enzymen, Chalcon-Reduktase, Chalcon-Isomerase Typ II und Isoflavon-Synthase, in Daidzein umgewandelt.
Biologisches Interesse
Pflanzen
Pflanzen verwenden Isoflavone und ihre Derivate als Phytoalexin , um sich vor pathogenen Pilzen und anderen Mikroben zu schützen . Sojabohnen verwenden auch Isoflavone, um Rhizobien zu stimulieren und stickstofffixierende Knötchen zu bilden .
Menschliche Ernährung
Isoflavone von ernährungsphysiologischem Interesse sind die hydroxylierten Derivate von Isoflavon, wobei letztere keine aufweisen.
Aufgrund ihrer relativen Seltenheit mit Ausnahme von Soja ist die Isoflavonaufnahme in Europa mit Ausnahme der Sojamilch (einige Säuglinge usw.) vernachlässigbar , in Ländern des Fernen Ostens (30-40 mg / Tag ) ist die Nahrungsaufnahme jedoch sehr wichtig ). Die östrogene Wirkung scheint nicht systematisch zu sein, da die Studien gemischte Ergebnisse liefern; Isoflavone zeigen jedoch zahlreiche metabolische Wechselwirkungen.
Biologisch gesehen erhöhen Isoflavone die Insulinsensitivität und senken den Cholesterinspiegel geringfügig .
Sie haben positive Auswirkungen auf:
- das Risiko, an Herz-Kreislauf-Erkrankungen zu erkranken ;
- Aufrechterhaltung des Knochenkapitals bei Frauen nach der Menopause ;
Es wurden jedoch bestimmte unerwünschte Wirkungen beobachtet, die jedoch seitdem diskutiert wurden, wobei die indirekte Wirkung auf die Schilddrüse zu einer relativen Hypothyreose führte ;
Französische Empfehlungen für Kinder und schwangere oder stillende Frauen
Die AFSSA hat folgende Empfehlungen abgegeben:
- Zubereitungen für Protein- Soja sollten Kindern nicht vor 3 Jahren gegeben werden, wenn sie keinen reduzierten Gehalt an Isoflavonen haben. Aufgrund seiner Zusammensetzung sind Tonyus ( Sojasaft ) für die Ernährung von Säuglingen und Kleinkindern (von der Geburt bis zu drei Jahren) kontraindiziert.
- Die schwangere Frau und die stillende Frau sollten einen hohen Konsum von Isoflavonen vermeiden, insbesondere in Form von Nahrungsergänzungsmitteln .
Tierversuche zeigen, dass die frühen Stadien der Entwicklung der Geschlechtsorgane (während der Schwangerschaft und Stillzeit ) besonders empfindlich auf die Exposition gegenüber Phytoöstrogenen reagieren .
Es werden morphologische Anomalien beobachtet, die zu einer Abnahme der Fruchtbarkeit, aber auch zu einer höheren Empfindlichkeit gegenüber Karzinogenen führen können.
Der Verzehr von Formeln auf Sojaproteinbasis sollte bei Säuglingen und schwangeren Frauen weniger als 1 mg · L -1 der rekonstituierten Formel (Aglycon 46-Äquivalente oder etwa 0,15 mg · kg -1 Körpergewicht) betragen.
Anmerkungen und Referenzen
- (in) Mud, S. Wiese, T. Nehls, S., Burow, M., Elliott, S., Carter-Wientjes, C. Shih, B. McLachlan, J., Cleveland, T., „ Evaluation of die östrogenen Wirkungen von Hülsenfruchtextrakten, die Phytoöstrogene enthalten “ , Journal of Agriculture and Food Science , vol. 53, n o 8,2003, p. 2193–2199 ( DOI 10.1021 / jf0211145 )
- (in) Long-ze Lin et al., " LC-ESI-MS-Studie der Flavonoidglycosidmalonate von Rotklee (Trifolium pretense) " , Journal of Agricultural and Food Chemistry , Vol. 3 , No. 2, n o 48,2000, p. 354–365 ( DOI 10.1021 / jf991002 )
- Gérard Chenuet et al., Phytotherapie: Gesundheit durch Pflanzen , Vidal - Sélection du Reader's Digest,2007320 p. ( ISBN 978-2-7098-1851-3 )
- (in) [PDF] USDA-Isoflavondatenbank
- Siehe auf exam.com .
- (de) Überprüfen Sie bekannte Interaktionen auf goodearthnaturalfoods.net .
- Curtis PJ, Sampson M., Potter J., Dhatariya K., Kroon PA, Cassidy A. Die chronische Einnahme von Flavan-3-olen und Isoflavonen verbessert die Insulinsensitivität und den Lipoproteinstatus und verringert das geschätzte 10-Jahres-CVD-Risiko bei medikamentös behandelten Frauen nach der Menopause mit Typ 2 Diabetes: eine 1-jährige, doppelblinde, randomisierte, kontrollierte Studie , Diabetes Care, 2012; 35: 226–232
- Ma L., Liu G., Ding M. et al. Isoflavonaufnahme und das Risiko einer koronaren Herzkrankheit bei Männern und Frauen in den USA: Ergebnisse aus 3 prospektiven Kohortenstudien , Circulation, 2020; 141: 1127–1137
- Auflage , 2001; 103: 258-262, zitiert von Nutranews0501.
- (in) Mark Messina und Geoffrey Redmond , "Die Wirkung von Sojaprotein und Sojabohnenisoflavon ist die Schilddrüsenfunktion bei gesunden Erwachsenen und Patienten mit Hypothyreose: Eine Überprüfung der relevanten Literatur " , Thyroid , Vol. 16, n o 3,März 2006, p. 249–258 ( ISSN 1050-7256 und 1557-9077 , DOI 10.1089 / thy.2006.16.249 , online gelesen , abgerufen am 29. März 2020 )
- AFSSA-Bericht über Phytoöstrogene