Acetylen
| Acetylen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dreidimensionale Struktur von Acetylen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifizierung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-Name | Ethin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.743 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EG | 200-816-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6326 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LÄCHELN |
C # C , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C2H2 / c1-2 / h1-2H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | farbloses Gas in Aceton unter Druck gelöst | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute Formel |
C 2 H 2 [Isomere] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molmasse | 26,0373 ± 0,0017 g / mol C 92,26%, H 7,74%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° Fusion | -80,7 ° C ( Tripelpunkt ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kochen | –84,7 ° C. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Löslichkeit | 1,185 g l –1 (Wasser, 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumenmasse |
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selbstentzündungstemperatur | 305 ° C. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammpunkt | Brennbares Gas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Explosionsgrenzen in der Luft | 2,3 - 100 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sättigender Dampfdruck | bei 20 ° C : 4.460 kPa
Gleichung:
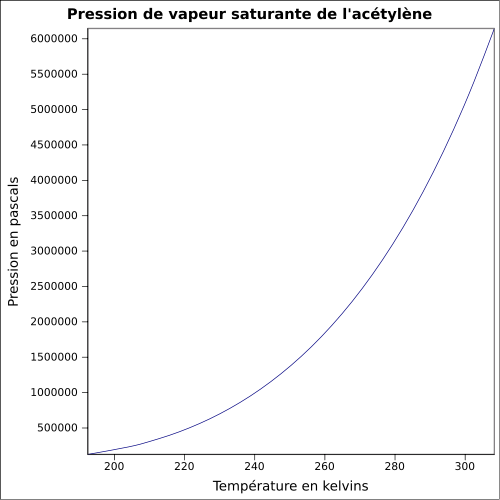
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritischer Punkt |
35,2 ° C 61,38 bar 0,1122 l / mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dreifacher Punkt | –80,8 ° C bei 1,2825 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 Gas, 1 bar | 200,93 J mol –1 K –1 ( 1 bar ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 Gas | 226,73 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
44,04 J mol –1 K –1 bei 25 ° C.
Gleichung:
Gleichung:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stck | 1 301,1 kJ · mol -1 ( 25 ° C , Gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re lonisierungsenergie | 11.400 ± 0,002 eV (Gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallographie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallklasse oder Raumgruppe | Pa 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Netzparameter |
a = 6,140 Å b = 6,140 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumen | 231,48 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vorsichtsmaßnahmen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Achtung H220, EUH006, H220 : Extrem brennbares Gas EUH006 : Explosionsgefahr bei Kontakt oder ohne Kontakt mit Luft |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, B1, F, A : Kritische Temperatur des Druckgases = 36,3 ° C B1 : Untere Entflammbarkeitsgrenze für brennbares Gas = 2,5% F : Gefährlich reaktives Material, das einer heftigen Zersetzungsreaktion ausgesetzt ist. Angabe bei 1,0% gemäß Klassifizierungskriterien Anmerkungen: Bitte beachten Sie auch die WHMIS-Klassifizierung von gelöstem Acetylen . |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 0 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
239 : brennbares Gas, das spontan eine heftige Reaktion hervorrufen kann. UN-Nummer : 1001 : Gelöstes Acetylen Klasse: 2.1 Klassifizierungscode: 4F : Unter Druck gelöstes Gas, brennbar; Kennzeichnung : 2.1 : Entzündbare Gase (entspricht den mit einem Großbuchstaben F bezeichneten Gruppen); 
- UN-Nummer : 3374 : ACETYLEN OHNE LÖSUNGSMITTEL Klasse: 2.1 Klassifizierungscode: 2F : Flüssiggas, brennbar; Kennzeichnung : 2.1 : Entzündbare Gase (entspricht den mit einem Großbuchstaben F bezeichneten Gruppen);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ökotoxikologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,37 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Geruchsschwelle | niedrig: 226 ppm hoch: 2.584 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Einheiten von SI und STP, sofern nicht anders angegeben. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Das Acetylen ( von der Nomenklatur IUPAC Ethin genannt ) ist eine chemische Verbindung der Kohlenwasserstoffklasse von Alkinen der Summenformel C 2 H 2 . Es wurde von entdeckt Edmund Davy in England in 1836 . Es ist der einfachste Alkin, bestehend aus zwei Kohlenstoffatomen und zwei Wasserstoff . Die beiden Kohlenstoffatome sind durch eine Dreifachbindung verbunden, die den größten Teil ihrer chemischen Energie enthält.
Beschreibung
Berthelot , in 1862 war, wobei die erste Acetylen zu synthetisieren, in einer Vorrichtung „Berthelot Ei“ genannt wird , durch einen Lichtbogen zwischen zwei Herstellung Elektroden von Graphit in einer Atmosphäre gebadet Wasserstoff : 2 C + H 2 → C 2 H 2
Acetylen ist ein farbloses Gas , das in reinem Zustand praktisch geruchlos ist (es wird jedoch im Allgemeinen ein charakteristischer Knoblauchgeruch zugeschrieben, der von Verunreinigungen herrührt, insbesondere von Phosphin, wenn es aus Calciumcarbid hergestellt wird ).
Acetylen ist bei normaler Temperatur und normalem Druck extrem entflammbar . Es ist endoenergetisch in Bezug auf Kohlenstoff und Wasserstoff und kann sich spontan, explosionsartig zersetzen, wenn der Druck größer als 100 kPa ist , und bis zu einigen bar, wo diese spontane Zersetzung unvermeidlich auftritt . Aus diesem Grund wird es gelöst in Aceton oder Dimethylformamid (DMF) gelagert , das selbst in einem porösen Stabilisierungsmaterial enthalten ist.
benutzen
Anwendungen von Acetylen:
- Der hohe Kohlenstoffgehalt ergibt eine sehr leuchtende Flamme, die beispielsweise in Acetylenlampen (Calabomb) für Bergleute oder Höhlenforscher verwendet wird.
- Die hohe Verbrennungswärme von Acetylen erreicht hohe Temperaturen ( 3200 ° C in reinem Sauerstoff) und ist daher ein idealer Kandidat als Brennstoff zum Schweißen. Eine der Besonderheiten der Verbrennung von Acetylen ist die zweistufige Verbrennung: Acetylen reagiert zuerst mit Sauerstoff unter Bildung von Kohlenmonoxid und Wasserstoff , dann reagieren diese Produkte in einer zweiten Stufe unter Bildung von Kohlendioxid und Wasser. Kohlenmonoxid und Wasserstoff sind reduzierende Gase, was sie zu beliebten Reagenzien beim Stahlschweißen macht, um Eisenoxide zu reduzieren, die aus der Reaktion zwischen Eisen und Sauerstoff bei hoher Temperatur resultieren, wodurch eine bessere Homogenisierung der Schweißnaht und damit eine bessere Qualität der Schweißnaht ermöglicht wird. Schweißen mit Acetylen ermöglicht die Montage von verschiedenen Metallen ( Stahl , Edelstahl, Kupfer - Legierungen ), aber auch unter bestimmten Bedingungen aus Aluminium mit legiertem Silicium .
- Acetylen wird auch als Kraftstoff in Analysegeräten verwendet. In der Atomabsorptionsspektrometrie (AAS), die mit verschiedenen Oxidationsmitteln (Luft, reiner Sauerstoff, Lachgas) assoziiert ist, ermöglicht sie die Ionisierung typischer Erdalkalielemente und die Bestimmung ihrer Konzentration dank des Beer-Lambert-Gesetzes .
- Acetylen wird auch in Autogenschneidbrennern verwendet. Propan wird jedoch bevorzugt, da es weniger teuer ist. Bei sehr dicken Schnitten ist Acetylen jedoch unerlässlich, um den Stahl ausreichend zu erwärmen und das Flammenschneiden über eine geringe Breite einzuleiten.
- Die Reaktion von Acetylen mit Salzsäure ist eine Möglichkeit zur Herstellung von Vinylchlorid ( Polyvinylchloridmonomer ).

Physikochemischen Eigenschaften
Die chemischen Eigenschaften von Acetylen werden größtenteils durch das Vorhandensein einer Dreifachbindung in seinem Molekül erklärt, die aus der Überlagerung einer Einfach- s- Bindung (resultierend aus der Fusion zweier sp- Orbitale ) und zwei p- Bindungen infolge der Fusion zweier 2p- Orbitale resultiert . Diese 0,124 nm lange Bindung, die durch eine Energie von 811 kJ gekennzeichnet ist , ist weniger stabil als Einfachbindungen (614 kJ ) und Doppelbindungen (347,3 kJ ) und daher reaktiver.
Die Reaktionen von Acetylen
- Acetylen und Monoalkylacetylene sind die einzigen Kohlenwasserstoffe, die Wasserstoff mit saurem Charakter aufweisen und gegen ein Metall ausgetauscht werden können.
- Einige Acetylenide wie zünden beim Aufprall.
- Acetylen reagiert mit Blausäure unter Bildung von Acrylnitril , einem Monomer aus Acrylnitril-Butadien-Styrol (ABS) und Styrol-Acrylnitril (SAN).
- Acetylen ergibt Benzol durch Polymerisation unter Einwirkung von Wärme.
- Durch die Dimerisierung in Gegenwart von Katalysatoren werden Vinylacetylen erhalten , zu dem Chlorwasserstoff wird zugegeben Chloropren, eine zu erhalten , Polychloropren oder Neopren Monomer .
Produktion und Synthese
Acetylen existiert nicht auf natürliche Weise (andere Alkine kommen gelegentlich in Kohlenwasserstoffen vor). Die wichtigsten industriellen Verfahren zur Herstellung von Acetylen sind:
Carbochemische Methode
Als Rohstoffe werden Kalkstein und Koks oder Holzkohle verwendet . In einem Hochtemperaturofen ( mindestens 1700 ° C ), der durch elektrischen Strom erhitzt wird, der durch das geschmolzene Reaktionsmedium fließt , wird Calciumcarbid gemäß den folgenden Reaktionen hergestellt: CaCO 3 → CaO + CO 2, CaO + 3 C + 108.300 Kalorien → CaC 2 + CO.
Beim Benutzer reagiert das Carbid mit Wasser unter Bildung von Acetylen, wobei 1 kg Carbid mit 562,5 g Wasser kombiniert werden, um 350 l Acetylen freizusetzen: CaC 2 + 2 H 2 O → C 2 H 2 + Ca (OH) 2 + 31.000 Kalorien.
Teilverbrennung von Methan
Bei teilweiser Verbrennung von Methan entsteht auch Acetylen: 3 CH 4 + 3 O 2 → C 2 H 2 + CO + 5 H 2 O..
Dehydrierung von Alkanen
Die schwersten Alkane in Erdöl und Erdgas werden in leichtere Moleküle gespalten, die bei hohen Temperaturen dehydriert werden: C 2 H 6 → C 2 H 2 + 2 H 2.
Anmerkungen und Referenzen
- ACETYLEN , Sicherheitsblatt (e) des Internationalen Programms zur Sicherheit chemischer Substanzen , konsultiert am 9. Mai 2009
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- (en) David R. Lide , CRC-Handbuch für Chemie und Physik, 89. Ausgabe , Boca Raton, CRC Press / Taylor und Francis,2009, "Physikalische Konstanten organischer Verbindungen"
- Eintrag "Acetylen" in der Chemiedatenbank GESTIS der IFA (deutsch, für Arbeitssicherheit und Gesundheitsschutz zuständig) ( deutsch , englisch ), abgerufen am 14. April 2009 (JavaScript erforderlich)
- (en) Robert H. Perry und Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- Clark, AM; Din, F., Gleichgewichte zwischen festen, flüssigen und gasförmigen Phasen bei binären Niedertemperatursystemen Acetylen-Kohlendioxid, Acetylen-Ethylen und Acetylen-Ethan, Trans. Faraday Soc., 1950, 46, 901.
- Tsonopoulos, C.; Ambrose, D., Dampf-Flüssigkeits-kritische Eigenschaften von Elementen und Verbindungen. 6. Ungesättigte aliphatische Kohlenwasserstoffe, J. Chem. Eng. Data, 1996, 41, 645 & ndash; 656.
- " Acetylen " unter http://www.nist.gov (abgerufen am 14. April 2009 )
- (in) Carl L. Yaws, Handbuch der thermodynamischen Diagramme , Bd. 1, 2 und 3, Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 und 978-0-88415-859-2 )
- (in) David R. Lide , CRC-Handbuch für Chemie und Physik , Boca Raton, CRC Press,18. Juni 2002, 83 th ed. 2664 p. ( ISBN 0849304830 , Online-Präsentation ) , p. 5-89
- (in) David R. Lide, Handbuch für Chemie und Physik , CRC,2008, 89 th ed. 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- " Acetylen " unter www.reciprocalnet.org (abgerufen am 12. Dezember 2009 )
- Index Nummer in Tabelle 3.1 des Anhangs VI der EG - Verordnung 1272/2008 (16. Dezember 2008)
- " Acetylen " in der Datenbank der Chemikalien Reptox der CSST (Quebec Organisation, die für Sicherheit und Gesundheitsschutz am Arbeitsplatz zuständig ist), abgerufen am 24. April 2009
- " Acetylen " unter hazmap.nlm.nih.gov (abgerufen am 14. November 2009 )
- . Nowak Ph (1999) - "L‘ Azetylen ", " Le P'tit Usania n o 7 " , auf USAN (abgerufen 5. Januar 2021 ) ( ISSN 1292-5950 ) , USAN, Nancy, p. 1











