Proline
| Proline | |
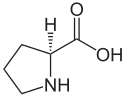 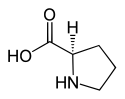 L oder S (-) - Prolin und D oder R (+) - Prolin |
|
| Identifizierung | |
|---|---|
| IUPAC-Name | Säure Pyrrolidin -2- carbon |
| Synonyme |
P, Pro |
| N o CAS |
(racemisch) (L) oderS(-) (D) oderR(+) |
| N o ECHA | 100.009.264 |
| N o EG | 205-702-2 (L) |
| FEMA | 3319 |
| LÄCHELN |
[H] N1CCCC1C (O) = O , |
| InChI |
InChI: InChI = 1 / C5H9NO2 / c7-5 (8) 4-2-1-3-6-4 / h4,6H, 1-3H2, (H, 7,8) |
| Chemische Eigenschaften | |
| Brute Formel |
C 5 H 9 N O 2 [Isomere] |
| Molmasse | 115,1305 ± 0,0054 g / mol C 52,16%, H 7,88%, N 12,17%, O 27,79%, |
| pKa | 1,95 - 10,64 |
| Biochemische Eigenschaften | |
| Codons | CCA , CCU , CCG , CCC |
| isoelektrischer pH | 6.30 |
| Essentielle Aminosäure | Nein |
| Vorkommen bei Wirbeltieren | 5,0% |
| Vorsichtsmaßnahmen | |
| WHMIS | |
|
Unkontrolliertes ProduktDieses Produkt wird nicht gemäß den WHMIS-Klassifizierungskriterien kontrolliert. |
|
| Einheiten von SI und STP, sofern nicht anders angegeben. | |
Das Prolin (Abkürzungen IUPAC - IUBMB : Pro und P ) ist eine saure α-Aminosäure, deren Enantiomer L eine der 22 proteinogenen Aminosäuren ist , die von den Codons CCU, CCC, CCA und CCG auf der Messenger-RNA kodiert werden . Es ist die einzige proteinogene Aminosäure mit einem sekundären und nicht primären Amin , was ihr eine bestimmte Geometrie verleiht, die dazu neigt, die Sekundärstrukturen von Proteinen wie den α-Helices und den β-Faltblättern zu unterbrechen .
Prolin bildet unpolare Reste, die bei der Polymerisation verschiedene Arten von Proteinen in einer Familie bilden können, die als Polyproline bezeichnet wird .
Das Vorhandensein vieler Prolinreste kann der Ursprung einer Prolinhelix sein; Dies ist insbesondere bei Kollagen der Fall . Der Prolin-Zyklus ist fast flach. Dies kann unter Berücksichtigung der Bindungswinkel in diesem Ring gezeigt werden.
In der Tierwelt
Prolin ist insbesondere an der Synthese von Kollagen beteiligt, das die Sequenz ( Gly- Pro- Hyp ) n aufweist und Narben.
In der Pflanzenwelt
Prolin ist an der ordnungsgemäßen Keimung von Samen, der Blüte und anderen Phasen der Pflanzenentwicklung beteiligt.
Bei vielen Pflanzenarten wurden Ansammlungen von Prolin beobachtet, wenn sie verschiedenen Arten von Umweltbelastungen ausgesetzt waren.
Eine wachsende Zahl von Beweisen stützt eine positive Korrelation zwischen diesen Ansammlungen und dem metabolischen Management dieser Belastungen durch Pflanzen. Es hat eine Osmolyts Rolle, aber es ist auch ein Metall - Chelator und hat antioxidative Eigenschaften. "Exogen und in niedrigen Dosen angewendet, verbessert es die Stresstoleranz in Pflanzen", aber mehrere Springer haben auch nachteilige Auswirkungen bei höheren Dosen festgestellt.
Daten
- Van der Waals Stärke : 90
- pK1 (α-COOH): 1,95
- pK2 (αN-H): 10,64
Prolin enthält eine cyclische sekundäre Aminfunktion in seinem Molekül.
Eine andere Aminosäure, Hydroxyprolin , wird durch 4- Hydroxylierung von Prolin abgeleitet .
Anmerkungen und Referenzen
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- (in) Francis A. Carey, " Tabelle der pK- und pH-Werte " , am Department of Chemistry der University of Calgary , 2014(abgerufen am 26. Juli 2015 )
- (in) Herr Beals, L. Gross, S. Harrell, " Aminosäurefrequenz " am Institut für Umweltmodellierung (ITSH) an der Universität von Tennessee (abgerufen am 26. Juli 2015 )
- " Proline (l-) " in der Datenbank für Chemikalien Reptox der CSST (Organisation für Sicherheit und Gesundheitsschutz am Arbeitsplatz in Quebec), abgerufen am 25. April 2009
- J. Behre, R. Voigt, I. Althöfer, S. Schuster: Zur evolutionären Bedeutung der Größe und Planarität des Prolinrings . Naturwissenschaften 99 (2012) 789 & ndash; 799.
- (en) Mudasir Irfan Dar , Mohd Irfan Naikoo , Farha Rehman , Fauzia Naushin und Fareed Ahmad Khan , „Prolinakkumulation in Pflanzen: Rollen in Stresstoleranz und Pflanzenentwicklung“ , in Noushina Iqbal, Rahat Nazar und Nafees A. Khan, Osmolyte und Pflanzen gewöhnen sich an veränderte Umweltbedingungen: Emerging Omics Technologies , New Delhi, Springer,2016( ISBN 978-81-322-2615-4 und 978-81-322-2616-1 , DOI 10.1007 / 978-81-322-2616-1_9 ) , p. 155-166.
Siehe auch
Literaturverzeichnis
- Ali Q, Ashraf M, Athar HUR (2007) Exogen appliziertes Prolin in verschiedenen Wachstumsstadien fördert das Wachstum von zwei Maissorten, die unter Wasserdefizitbedingungen gezüchtet wurden. Pak J Bot 39: 1133 & ndash; 1144
- (en) Patrick Armengaud , Laurent Thiery , Nathalie Buhot und Ghislaine Grenier-de March , „Die Transkriptionsregulation der Prolinbiosynthese in Medicago truncatula zeigt entwicklungs- und umweltspezifische Merkmale “ , Physiologia Plantarum , vol. 120, n o 3,März 2004, p. 442–450 ( ISSN 0031-9317 und 1399-3054 , DOI 10.1111 / j.0031-9317.2004.00251.x , online gelesen , abgerufen am 21. Oktober 2020 )
- (en) M. Ashraf und MR Foolad , "Die Rolle von Glycinbetain und Prolin bei der Verbesserung der Resistenz gegen pflanzlichen abiotischen Stress " , Environmental and Experimental Botany , vol. 59, n o 2März 2007, p. 206–216 ( DOI 10.1016 / j.envexpbot.2005.12.006 , online gelesen , abgerufen am 21. Oktober 2020 )