Indoxyl
| Indoxyl | |
| |
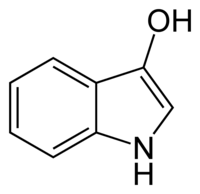
| Enol - Form von ultra-Moll lndoxyl | |
| Identifizierung | |
|---|---|
| IUPAC-Name |
1,2-Dihydro-3H-indol-3-on 1H-indol-3-ol (Enolform) |
| N o CAS | |
| N o ECHA | 100,216,308 |
| PubChem | 50591 |
| LÄCHELN |
O = C2CNc1ccccc12 , |
| InChI |
InChI: InChI = 1 / C8H7NO / c10-8-5-9-7-4-2-1-3-6 (7) 8 / h1-4,9H, 5H2 |
| Aussehen | hellgelbe Kristalle |
| Chemische Eigenschaften | |
| Brute Formel |
C 8 H 7 N O [Isomere] |
| Molmasse | 133,1473 ± 0,0074 g / mol C 72,17%, H 5,3%, N 10,52%, O 12,02%, |
| Physikalische Eigenschaften | |
| T ° Fusion | 85 ° C. |
| Löslichkeit | Löslich in Wasser, Laugen , Ethanol und Ether |
| Verwandte Verbindungen | |
| Isomer (e) | Oxindol |
| Einheiten von SI und STP, sofern nicht anders angegeben. | |
Das Indoxyl ist eine chemische Verbindung der Summenformel C 8 H 7 NO. Es ist ein Derivat von Indol , einem natürlichen oder synthetischen Vorläufer von Indigotin, dem Hauptmolekül der Indigo-Tinktur .
Eigenschaften
Indoxyl ist ein Keton und weist als solches ein keto-enolisches Gleichgewicht zwischen zwei Formen auf:
Spektroskopische Analysen zeigen, dass tatsächlich, wie bei den meisten Ketonen, die Ketonform fast die einzige ist, die es gibt.
Synthese
"Natürlich"
Indoxyl kann aus einer natürlichen Substanz, Indican , einem aus dem Indigotier extrahierten Heterosid , synthetisiert werden . Letzteres besteht aus einem β-D- Glucosering und einem Indoxylring. Eine einfache Hydrolyse reicht aus, um die beiden Verbindungen zu trennen.
Industriell
Die Gruppen BASF und Hoechst AG haben eine industrielle Synthese von Indoxyl aus Anthranilsäure entwickelt , die als Heumann-Pfleger-Synthese bezeichnet wird.
Anmerkungen und Referenzen
- Thieme-Chemie (Hrsg.): Römpp Online . Version 3.1. Georg Thieme Verlag, Stuttgart 2007.
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- Wittko Francke und Wolfgang Walter: Lehrbuch der Organischen Chemie . S. Hirzel Verlag Stuttgart; 24. überarb Auflage 2004 ( ISBN 3-7776-1221-9 ) ; S. 776
- (de) Dieser Artikel teilweise oder vollständig aus dem Wikipedia - Artikel in genommen deutschen Titeln „ Indoxyl “ ( siehe Liste der Autoren ) .