Kalziumhydroxid
| Kalziumhydroxid | |||
| |||
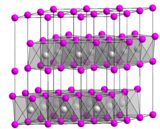
| Kristallstruktur. __ Ca 2+ __ OH - |
|||
| Identifizierung | |||
|---|---|---|---|
| Synonyme |
Calciumdihydroxid, Calciumhydrat |
||
| N o CAS | |||
| N o ECHA | 100.013.762 | ||
| N o EG | 215-137-3 | ||
| PubChem | 14777 | ||
| N o E | E526 | ||
| LÄCHELN |
[Ca] (O) O , |
||
| InChI |
InChI: InChI = 1 / Ca.2H2O / h 2 * 1H2 / q + 2 ;; / p-2 / rCaH2O2 / c2-1-3 / h2-3H |
||
| Aussehen | farblose Kristalle oder weißes Pulver | ||
| Chemische Eigenschaften | |||
| Formel | Ca(OH) 2 | ||
| Molmasse | 74,093 ± 0,005 g / mol H 2,72 %, Ca 54,09 %, O 43,19 %, |
||
| Physikalische Eigenschaften | |||
| T ° Fusion | (Zersetzung): 580 ° C | ||
| Löslichkeit |
1,85 g · L -1 (Wasser, 0 ° C ) 1,73 g · L -1 (Wasser, 20 ° C ) |
||
| Volumenmasse | 2,24 g · cm -3 | ||
| Kristallographie | |||
| Kristallsystem | trigonales Kristallsystem | ||
| Bravais-Netzwerk | sechseckiges Bravais- Gitter | ||
| Netzparameter |
a = 3,589 c = 4,911 Å Z = 1 |
||
| Volumen | 54,69 3 | ||
| Vorsichtsmaßnahmen | |||
| WHMIS | |||
 E, E : Ätzendes Material. Starke Base (pH einer gesättigten Lösung = 12,5). Offenlegung bei 1,0% gemäß der Inhaltsstoffoffenlegungsliste. |
|||
| Transport | |||
Unbekanntes Tag. Fehler melden: Discussion_Model: ADR- Label nicht erkannt. Fehler melden: Discussion_Model: ADR- Label nicht erkannt. Fehler melden: Discussion_Model: ADR |
|||
| Einheiten von SI und STP, sofern nicht anders angegeben. | |||
Das Calciumhydroxid ist eine chemische Substanz Mineral , ionische Verbindung des Kations Calcium und des Anions Hydroxid , Summenformel Ca (OH) 2. Diese Alkali antik wird auch als „ gelöschter Kalk “, „Fett Kalk“ und „Kalk“ , weil diese ätzend und hygroskopisch Pulver aus dem hergestellt wurde , gebranntem Kalk oder Calciumoxid durch den ehemaligen erzeugten Kalkofen von Kalkbrenner . Es ist auch ein seltenes natürliches Mineral, Dichte 2,23, von Mineralogen " Portlandit " genannt, weil es ein einfaches Produkt der Hydrolyse von Portlandzement ist .
Es ist der Hauptbestandteil in gelöstem Kalkwasser oder in Suspension in Kalkmilch . Tatsächlich ist dieses anorganische Erdalkalihydroxid sehr unlöslich in Wasser: je nach Zusammensetzung von Industriekalk, oft etwas magnesisch, zwischen 1,1 g · L -1 und 1,6 g · L -1 bis 20 ° C , zwischen etwa 0,6 g · L -1 und 0,7 g · L -1 bis 80 ° C . Die reine Verbindung im Labor ist kaum löslicher. Seine ohnehin sehr geringe Löslichkeit in Wasser nimmt mit der Temperatur leicht ab. Seine Löslichkeitsproduktkonstante liegt in der Größenordnung von 5,02 × 10 –6 bis 25 °C .
Vorbereitung
Der Löschkalk wurde nach der Schnellmethode der alten Kalkverkäufer durch Löschen von Branntkalk - CaO . hergestellt- durch Eintauchen in Wasser. Dies ist eine sehr exotherme Reaktion, die Hydratation von Calciumoxid erzeugt Calciumhydroxid:
Weißes festes CaO + H 2 Oflüssig → schwach gelöstes Ca (OH) 2 (wässrig), meist in Wasser suspendiert , mit ΔH = ~ 1 155 kJ · kg -1 Branntkalk.Der in Wasser suspendierte Feststoff in der Größenordnung von 100 g · L –1 bildet eine sogenannte "Kalkmilch", Calciumhydroxid ist der weiße Feststoff, der nach dem Trocknen in einem Ofen oder im Ofen erhalten wird. Die gefilterte Kalkmilch ergibt ein klares „Kalkwasser“. In feuchter Luft könnte eine Reaktion Luftkalk , tatsächlich Calciumhydroxid, ergeben, aber dies nur in Abwesenheit von Karbonisierung oder Fixierung von Kohlendioxid , was selten der Fall ist. Kalkwasser trübt sich in Gegenwart dieses letzten Gases: Es war für die alten Chemiker nach der Arbeit von Jean-Baptiste Van Helmont der erste Gasdetektor, der für das Vorhandensein dieses Waldgases bekannt ist .
Ein anderer radikaler Weg, absolut unrentabel, aber im Labor durchaus üblich, ist die Reaktion des Metalls Kalzium , die eine Gasfreisetzung erzeugt:
Ca festes Metall + 2 H 2 Oflüssig → wässrig Ca (OH) 2 , dann zu großen Teilen in Körnern ausgefällt + H 2 -GasEs ist wegen der potentiellen Reaktivität des Metalls und der Explosivität oder potentiellen Entflammbarkeit von Wasserstoffgas in der Luft gefährlich .
Toxikologie und Sicherheit
Es ist ein aggressives Alkali, das als ätzend und reizend auf Haut und Schleimhäute erkannt wird. Es kann bei Projektion und/oder Kontakt zu Reizungen und besonders schweren Augenschäden führen. Es reizt die Atemwege. Es stellt eine Toxikologie gegenüber bestimmten Organen des Körpers dar, ohne spezifische chemische Vorschriften. Chronische Toxizität ist noch unbekannt: Sie ist anfällig für Langzeitwirkungen, wie zum Beispiel die langsame Schwächung der Zähne.
Für die Umwelt stellt Löschkalk häufig eine alkalische Bedrohung dar, insbesondere für Fließgewässer und Gewässer sowie wässrige Ökosysteme.
Verwendet
Wenn Branntkalk CaO übernimmt die meisten Arbeitsplätze in der Stahlindustrie, öffentlichen Arbeiten und Straßen (Entwässerung des Gleisbettes seit der römischen Antike), Wasseraufbereitung und Landwirtschaft, Bau- und Bauwesen, Löschkalk wird als Mittel zur Aufnahme von Kohlendioxid verwendet, sowohl in Anästhesie- und Notfallbeatmungsgeräten, als auch in Lebensmitteln.
Calciumhydroxid ist ein Lebensmittelzusatzstoff ( E526 ), der in vielen Produkten als pH-Regulator und Festiger / Stabilisator für Lebensmittel verwendet wird.
Kalk wird auch bei der Herstellung von Industriefetten verwendet.
Verweise
- CALCIUM HYDROXIDE , Sicherheitsblatt(e) des International Program on Chemical Safety , eingesehen am 9. Mai 2009
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- „Calciumhydroxid“ in der Gefahrstoffdatenbank (Zugriff am 21. September 2009).
- " Calciumhydroxid " in der Datenbank für chemische Produkte Reptox des CSST (für Arbeitssicherheit und Gesundheitsschutz zuständige Organisation in Quebec), abgerufen am 25. April 2009
- Für das reine Laborprodukt beträgt die Löslichkeit in Wasser ca. 1,85 g · L -1 bei 0 °C ; 1,28 g · L -1 bis 50 °C ; 0,71 g · L -1 bis 100 ° C .
- Infobox
- Kalk bleibt dennoch und vor allem für Maurer oder Profis im Bau- und Rohbau ein hydraulischer Kalk oder Bindemittel mit hydraulischer Abbindung, also mit mehr oder weniger schneller Abbindung mit Wasser und ggf. dann an der Luft. Der ideale Mörtel wäre ein Kalk, der in einem Wasserstrahl fast augenblicklich abbinden würde.
- Unterschied zu letzterem Kalk, der durch Luft, Luftkalk oder Maurer und andere Fachleute gewonnen wird, ist vor allem ein Bindemittel auf der Basis von schwach angefeuchtetem Kalk oder Kalkmilch, das mehr oder weniger langsam an der Luft abbindet, insbesondere durch Karbonisierung oder Fixierung von Kohlenstoff Dioxid.
- Europäisches Parlament und der Europarat " Richtlinie 95/2 / EG über andere Lebensmittelzusatzstoffe als Farbstoffe und Süßungsmittel " Amtsblatt der Europäischen Union , n o L 61,20. Februar 1995, s. 1-56 ( online lesen [PDF] ).
- „ Klassennamen und internationales Nummerierungssystem für Lebensmittelzusatzstoffe “ [PDF] , CAC/GL 361989 , unter http://www.codexalimentarius.net , Codex alimentarius ,1989(Zugriff am 14. September 2008 ) , S. 1-35
- (in) Codex-Alimentarius-Kommission , " Aktualisiert bis zur 31. Sitzung der Codex-Alimentarius-Kommission für Calciumhydroxid (526) " , GSFA Online auf http://www.codexalimentarius.net , Codex Alimentarius,2008(Zugriff am 3. Oktober 2008 )
Siehe auch
Verwandter Artikel
Externe Links
- Kalkseite
- Toxikologisches Blatt , CNESST
- Kompaktes Sicherheitsdatenblatt , CDC ,10. September 2015
- Lucile Goupy , " Risiken im Zusammenhang mit der langfristigen Verwendung von Calciumhydroxid " [PDF] , auf cpeastudyclub.org , L'Information dentaire n o 16,16. April 2008