Phthalimid
| Phthalimid | ||
 | ||
| Struktur und Darstellung von Phthalimid | ||
| Identifizierung | ||
|---|---|---|
| IUPAC-Name | Benzol-1,2-dicarboximid | |
| N o CAS | ||
| N o ECHA | 100.001.458 | |
| N o EG | 201-603-3 | |
| LÄCHELN |
O = C2NC (C1 = CC = CC = C12) = O , |
|
| InChI |
InChI: InChI = 1 / C8H5NO2 / c10-7-5-3-1-2-4-6 (5) 8 (11) 9-7 / h1-4H, (H, 9,10,11) |
|
| Aussehen | solides Weiss | |
| Chemische Eigenschaften | ||
| Brute Formel |
C 8 H 5 N O 2 [Isomere] |
|
| Molmasse | 147,1308 ± 0,0076 g / mol C 65,31%, H 3,43%, N 9,52%, O 21,75%, |
|
| pKa | 8.3 | |
| Physikalische Eigenschaften | ||
| T ° Fusion | 238 ° C. | |
| T ° kochen | 336 ° C (Sublimation) | |
| Löslichkeit |
360 mg · L -1 (Wasser, 25 ° C ) 0,6 g · L & supmin ; ¹ (Wasser) |
|
| Volumenmasse | 1,21 g · cm -3 bis 20 ° C | |
| Flammpunkt | 165 ° C DIN 51758 | |
| Ökotoxikologie | ||
| LogP | 1.15 | |
| Verwandte Verbindungen | ||
| Andere Verbindungen |
Maleimid ( Amide ) und Phthalsäureanhydrid |
|
| Einheiten von SI und STP, sofern nicht anders angegeben. | ||
Das Phthalimid ist ein Imidaromat , dh eine organische Verbindung mit zwei Gruppen Carbonyl, die an ein Atom von Stickstoff trigonal gebunden sind . Es ist das Imid von Benzol-1,2-dicarbonsäure ( Phthalsäure ).
Eigenschaften
Phthalimid ist ein weißer Feststoff, der bei Raumtemperatur kristallisiert . Es ist in kaltem Wasser praktisch unlöslich, in Benzol und Petrolether sehr schwer löslich und in heißem Ethanol, Ethansäure und konzentrierten Basen gut löslich.
Erhalten
Phthalimid wird durch Heißreaktion von Phthalsäureanhydrid mit Ammoniak in wässriger Lösung erhalten.

Reaktivität
Gabriels Reaktion
Die Hauptreaktion unter Verwendung von Phthalimid ist die Gabriel-Synthese von Aminprimären . Diese Reaktion ist nach dem deutschen Chemiker Siegmund Gabriel benannt , der sie entwickelt hat.
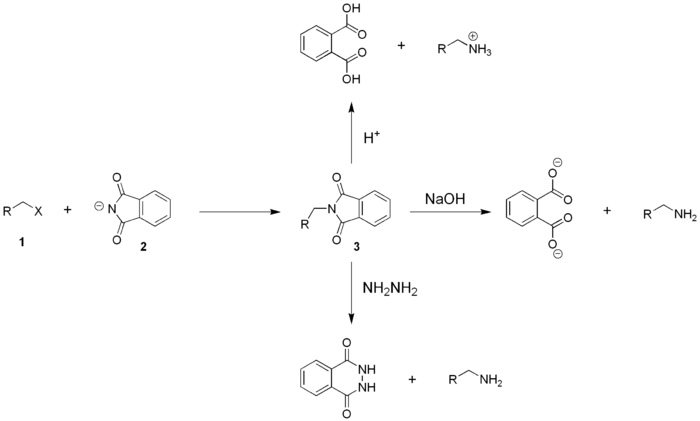
Diese Reaktion ermöglicht es auch, α-Aminosäuren aus Phthalimid und der entsprechenden α-bromierten Säure zu synthetisieren:

Hofmann-Umlagerung
Die Wirkung des Hypochlorition in wässriger Lösung führt durch Hofmann-Umlagerung zur Bildung von Anthranilsäure , einem Vorläufer bei der Synthese von Indigo .
Umweltkinetik
Diese Frage ist von ökotoxikologischer Bedeutung, da Phthalimid eines der Hauptabbauprodukte bestimmter fungizider Pestizide einschließlich Folpet ist .
Es wurde experimentell gezeigt, dass Phthalimid bei 25 ° C und pH 4 und bei pH 7 stabil ist, aber unter alkalischen Bedingungen (pH 9) schnell hydrolysiert wird (mit einer Halbwertszeit von 2 Stunden).
Verwendet
Phthalimid wird als Pflanzenschutzmittel , in der organischen Synthese , in der Forschung und in der Kunststoffindustrie eingesetzt .
In der Natur
Kladnoit ist ein natürlich vorkommendes Mineral ähnlich wie Phthalimid. Es ist ziemlich selten und wird an Kohlefeuerstellen gefunden.
Verweise
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- (in) " Phthalimid " auf ChemIDplus , abgerufen am 29. Juni 2009
- Eintrag "Phthalimid" in der Chemiedatenbank GESTIS der IFA (deutsch, für Arbeitssicherheit und Gesundheitsschutz zuständig) ( deutsch , englisch ), abgerufen am 29. Juni 2009 (JavaScript erforderlich)
- Arun Sethi, Systematische Laborexperimente in der organischen Chemie , 2003, hrsg. New Age International ( ISBN 978-81-224-1491-2 ) , p. 659
- S. Gabriel, S. Ber. 20, 2224 (1887)
- EFSA (2009), Schlussfolgerung zur Begutachtung der Pestizid-Risikobewertung des Wirkstoffs Folpet (Frage Nr. EFSA-Q-2009-605) Wissenschaftlicher Bericht der EFSA (2009) 297, 1-80: Neubewertungsdokument veröffentlicht im Jahr 2009 anstelle des vom 24. April 2006 (EFSA Scientific Report, 2006) PDF, 80 Seiten
Vogel's Lehrbuch für Praktische Organische Chemie (Longman).