Schwefelmonoxid
| Schwefelmonoxid | |
   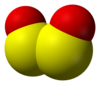 Struktur von Schwefelmonoxid. (unten: "Dimer" -Peroxid S 2 O 2) |
|
| Identifizierung | |
|---|---|
| N o CAS | |
| PubChem | 114845 |
| ChEBI | 45822 |
| LÄCHELN |
O = S , |
| InChI |
InChI: InChI = 1S / OS / c1-2 InChIKey: XTQHKBHJIVJGKJ-UHFFFAOYSA-N |
| Chemische Eigenschaften | |
| Brute Formel | S O. |
| Molmasse | 48,064 ± 0,005 g / mol O 33,29%, S 66,72%, |
| Einheiten von SI und STP, sofern nicht anders angegeben. | |
Das Schwefelmonoxid ist eine chemische Verbindung von der Formel SO. Dieses Molekül ist thermodynamisch instabil und existiert als solches nur im verdünnten gasförmigen Zustand ; es dimerisiert in S 2 O 2in einem kondensierten Zustand, manchmal Schwefelperoxid genannt . Dies ist der Grund, warum Schwefelmonoxid im Weltraum nachgewiesen wurde, aber auf der Erde nicht auf natürliche Weise existiert .
Das SO- Molekül ist wie das O 2 -Molekül durch einen Triplett- Grundzustand gekennzeichnet Das heißt, jedes Molekül hat zwei ungepaarte Elektronen mit parallelem Spin , jedes auf seinem eigenen Atomorbital . Die SO-Bindung ist 148,1 um lang und länger als die von S 2 O- Molekülen ( 146 Uhr ) , SO 2 ( 143,1 Uhr ) und SO 3 ( 142 Uhr ) .
Das Molekül kann angeregt in einem Singulett - Zustand durch Absorption eines Infrarotphotonen . Es wird angenommen, dass dieser Singulettzustand reaktiver ist als der Triplettzustand, wie für das O 2 -Molekül beobachtet .
Schwefelmonoxid kann im Labor hergestellt wird durch Glimmentladung durch Schwefeldämpfe gemischt mit Schwefeldioxid SO 2und konnte durch Sonolumineszenz in einer Lösung konzentrierter Schwefelsäure, die Edelgase enthielt, nachgewiesen werden . Basierend auf den Reaktionen wurde auch ein chemilumineszierender Schwefelmonoxiddetektor veröffentlicht:
SO + O 3→ SO 2 *+ O 2, SO 2 *→ SO 2+ h ν .Schwefelmonoxid kommt auf natürliche Weise in der Umgebung des Io- Satelliten des Planeten Jupiter sowohl in seiner Atmosphäre als auch in seiner Exosphäre vor und wurde in der Atmosphäre von Venus , Komet Hale-Bopp und dem interstellaren Medium nachgewiesen .
Anmerkungen und Referenzen
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- (in) Norman N. Greenwood, A. Earnshaw, " Chemie der Elemente ", Butterworth Heinemann, 2 e Ausgabe, Oxford, 1997 ( ISBN 0080379419 ) .
- (in) " Die Temperatur der Einzelblasen-Sonolumineszenz " KS Suslick und Flannigan DJ im Journal der Acoustical Society of America , (2004) 116 , 4, 2540.
-
(in) Richard L. Benner, Donald H. Stedman , " Chemischer Mechanismus und Effizienz des Schwefel-Chemilumineszenz-Detektors " , Applied Spectroscopy , Vol. 3, No. 48, n O 7,
Juli 1994, p. 14A-21A und 775-903 ( online lesen )
DOI : 10.1366 / 0003702944029901 -
(in) Lellouch , " Urey Prize Reading. Ios Atmosphäre: Noch nicht verstanden “ , Icarus , vol. 124, n o 1,
November 1996, p. 1-21 ( online lesen )
DOI : 10.1006 / icar.1996.0186 -
(in) CT Russell und MG Kivelson , " Detection of SO in Io's Exosphere " , Science , vol. 287, n o 5460,
17. März 2000, p. 1998-1999 ( ISSN 0036-8075 , online lesen )
DOI : 10.1126 / science.287.5460.1998 -
(in) Chan Y. Na, Thomas W. Skinner , Larry W. Esposito , " International Ultraviolet Explorer Observation of Venus SO 2
und SO ” , Journal of Geophysical Research - Atmospheres , vol. 95, n o D61990, p. 7485-7491 ( online lesen )
DOI : 10.1029 / JD095iD06p07485 -
(in) DC Lily, DM Mehringer, D. Benford, Gardner, TG Phillips, D. Bockelée-Morvan, N. Biver, P. Colom, J. und D. Crovisier Despois et al . , " Neue molekulare Spezies im Kometen C / 1995 O1 (Hale-Bopp), beobachtet mit dem Caltech Ssubmillimeter Observatory " , Earth, Moon and Planets , vol. 78, n Knochen 1-3,
1998, p. 13-20 ( online lesen )
DOI : 10.1023 / A: 1006281802554 -
(in) AC Gottlieb, Gottlieb EW, Herr Litvak, JA Ball und H. Penfield , " Beobachtungen von interstellarem Schwefelmonoxid " , Astrophysical Journal, Part 1 , Vol. 219,
1 st Januar 1978, p. 77-94
DOI : 10.1086 / 155757