Krypton-Difluorid
| Krypton-Difluorid | ||

| ||
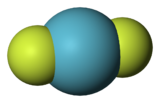 | ||
| Struktur von Krypton-Difluorid | ||
| Identifizierung | ||
|---|---|---|
| N o CAS | ||
| LÄCHELN |
[Kr] (F) F , |
|
| InChI |
InChI: InChI = 1 / F2Kr / c1-3-2 |
|
| Chemische Eigenschaften | ||
| Brute Formel | KrF 2 | |
| Molmasse | 121,795 ± 0,002 g / mol F 31,2%, Kr 68,8%, |
|
| Physikalische Eigenschaften | ||
| Volumenmasse | 3240 kg · m -3 bis 15 ° C | |
| Einheiten von SI und STP, sofern nicht anders angegeben. | ||
Das Krypton-Difluorid der Formel KrF 2ist die erste identifizierte Kryptonverbindung . Es ist ein farbloser flüchtiger Feststoff, dessen Molekül eine lineare F-Kr-F-Struktur mit 188,9- µm- Bindungen aufweist . Es bildet Salze von KrF- Kationen+ und Kr 2 F 3+ mit starken Lewis-Säuren .
Krypton-Difluorid ist ein starkes Fluorierungsmittel, das in der Lage ist, Xenon und Iod bzw. Xenonhexafluorid und Pentafluoridjod umzuwandeln :
Xe+ 3 KrF 2→ XeF 6 + 3 Kr I 2+ 5 KrF 2→ 2 WENN 5 + 5 KrDas KrF-Kation+ ist auch das einzige bekannte Mittel, das Gold in seine Oxidationsstufe +5 bringen kann :
8 KrF 2 + 2 bis → 2 KrF+ AuF 6- + 6 Kr+ F 2 KrF+ AuF 6- → AuF 5 + Kr+ F 2bei über 60 ° C.Anmerkungen und Referenzen
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- AV Grosse, AD Kirschenbaum, AG Stärke, LV Stärke, "Krypton Tetrafluorid: Herstellung und einige Eigenschaften", Science, 1963, Band 139, Seiten 1047-1048, DOI : 10.1126 / science.139.3559.1047
- JF Lehmann, DA Dixon, GJ Schrobilgen, "Röntgenkristallstrukturen von α-KrF 2, [KrF] [MF 6 ](M = As, Sb, Bi), [Kr 2 F 3 ] [SbF 6 ] • KrF 2, [Kr 2 F 3 ] 2 [SbF 6 ] 2 • KrF 2und [Kr 2 F 3 ] [AsF 6 ] • [KrF] [AsF 6 ];; Synthese und Charakterisierung von [Kr 2 F 3 ] [PF 6 ] • nKrF 2;; und theoretische Studien von KrF 2KrF+ , Kr 2 F 3+ und die [KrF] [MF 6 ](M = P, As, Sb, Bi) Ionenpaare ", Inorganic Chemistry 2001, Band 40, Seiten 3002-3017, DOI : 10.1021 / ic001167w