Sauerstoffdifluorid
| Sauerstoffdifluorid | |||
|
|||
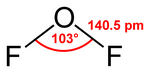
| Struktur von Sauerstoffdifluorid | |||
| Identifizierung | |||
|---|---|---|---|
| IUPAC-Name | Sauerstoffdifluorid | ||
| Synonyme |
Sauerstofffluorid |
||
| N o CAS | |||
| N o ECHA | 100,029,087 | ||
| N o EG | 231-996-7 | ||
| N o RTECS | RS2100000 | ||
| PubChem | 24547 | ||
| ChEBI | 30494 | ||
| LÄCHELN |
O (F) F , |
||
| InChI |
Std. InChI: InChI = 1S / F2O / c1-3-2 Std. InChIKey: UJMWVICAENGCRF-UHFFFAOYSA-N |
||
| Aussehen | farbloses Druckgas mit charakteristischem Geruch, im flüssigen Zustand gelblich bis braun | ||
| Chemische Eigenschaften | |||
| Brute Formel |
F 2 O. |
||
| Molmasse | 53,9962 ± 0,0003 g / mol F 70,37%, O 29,63%, |
||
| Physikalische Eigenschaften | |||
| T ° Fusion | -223,8 ° C. | ||
| T ° kochen | –144,75 ° C. | ||
| Löslichkeit | 68 cm 3 · L -1 in Wasser bei 0 ° C , langsame Reaktion | ||
| Volumenmasse | 2,421 g · cm -3 bis 0 ° C und 101,3 kPa | ||
| Kritischer Punkt | –58 ° C ; 4,95 MPa ; 0,5532 g · cm -3 | ||
| Vorsichtsmaßnahmen | |||
| SGH | |||
   Achtung H270, H314, H330, H270 : Kann Feuer verursachen oder verstärken ; Oxidationsmittel H314 : Verursacht schwere Hautverbrennungen und Augenschäden. H330 : Tödlich beim Einatmen |
|||
| WHMIS | |||
    A, C, D1A, E, A : Verdichtetes Gas kritische Temperatur = -58 ° C C : Oxidations Material verursacht oder fördert die Verbrennung eines anderen Materials durch Sauerstoff freisetz D1A : Sehr giftig Material schwerwiegende sofortige Wirkungen Transport gefährlicher Güter: Klasse 2.3 E : Ätzende Material Transport gefährlicher Güter : Klasse 8 Offenlegung zu 1,0% gemäß der Offenlegungsliste für Inhaltsstoffe |
|||
| Transport | |||
265 : giftiges und oxidierendes Gas (fördert das Feuer) UN-Nummer : 2190 : SAUERSTOFFDIFLUORID, KOMPRIMIERT Klasse: 2,3 Etiketten: 2,3 : Giftige Gase (entspricht den durch ein Großbuchstaben T bezeichneten Gruppen, d. H. T, TF, TC, TO, TFC und TOC). 5.1 : Oxidierende Substanzen 8 : Ätzende Substanzen Verpackung: -    |
|||
| Einheiten von SI und STP, sofern nicht anders angegeben. | |||
Das Sauerstoffdifluorid oder einfacher Fluoridsauerstoff ist die chemische Verbindung der Formel OF 2. Es ist ein farbloses, sehr oxidierendes Gas .
Vorbereitung
OF 2 Sauerstoffdifluoridwurde erstmals 1929 vom französischen Chemiker Paul Lebeau während seiner Fluoridforschung mit Augustin Damien beschrieben. Es wurde durch Elektrolyse von geschmolzenem Kaliumfluorid KF und Fluorwasserstoff HF mit Spuren von Wassermolekülen erhalten.
Die moderne Herstellungsmethode beinhaltet die Reaktion von Fluor F 2mit einer verdünnten wässrigen Lösung von Natriumhydroxid NaOH:
2 F 2+ 2 NaOH→ OF 2+ 2 NaF+ H 2 O.Reaktionen
Sauerstoffdifluorid zersetzt sich oberhalb von 200 ° C zu Difluor F 2und Sauerstoff O 2 durch einen radikalen Mechanismus. Es reagiert mit vielen Metallen zu Fluoriden und Oxiden sowie mit Nichtmetallen: OF 2reagiert beispielsweise mit Phosphor zu Phosphorpentafluorid PF 5und Phosphoroxytrifluorid POF 3und mit Schwefel , um Schwefeldioxid SO 2 zu ergebenund Schwefeltetrafluorid SF 4. Mit Xenon OF 2kann Xenontetrafluorid XeF 4 ergebensowie Xenon- Oxyfluoriden ( Xenon oxidifluoride XeOF 2und Xenon oxytetrafluoride XeOF 4 insbesondere).
Sauerstoffdifluorid reagiert langsam mit Wasser unter Bildung von Flusssäure :
VON 2 (aq)+ H 2 O (aq)→ 2 HF (aq)+ O 2 (g)Anmerkungen und Referenzen
- SAUERSTOFFDIFLUORID , Sicherheitsblatt (e) des Internationalen Programms für chemische Sicherheit , konsultiert am 9. Mai 2009
- berechnete Molekülmasse von „ Atomgewichte der Elemente 2007 “ auf www.chem.qmul.ac.uk .
- Eintrag "Oxygen Difluoride" in der Chemiedatenbank GESTIS der IFA (deutsch, für Arbeitssicherheit und Gesundheitsschutz zuständig) ( deutsch , englisch ), abgerufen am 26. Mai 2018 (JavaScript erforderlich)
- " Oxygen Difluoride " in der Datenbank chemischer Produkte Reptox der CSST (Quebec Organisation, die für Sicherheit und Gesundheitsschutz am Arbeitsplatz zuständig ist), abgerufen am 25. April 2009